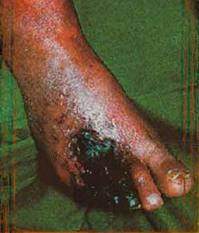
Mionecrosis por clostridio
Mionecrosis por clostridio. Se realizó una revisión bibliográfica exhaustiva sobre la gangrena gaseosa, con el fin de profundizar en los principales aspectos fisiopatológicos, microbiológicos, clínicos, de diagnóstico y terapéuticos de la mionecrosis por clostridio, dadas su prevalencia e incidencia elevadas, tanto en tiempos de paz como de guerra. Se ofrecen las consideraciones actuales sobre la evaluación de las principales complicaciones y cómo proceder para eliminarlas.
Sumario
- 1 Definición
- 2 Bioquímica de la lesión y la muerte celular
- 3 Factores favorecedores
- 4 Clostridios microbiología
- 5 Características clínicas
- 6 Antecedentes
- 7 Formas clínicas
- 8 Diagnostico
- 9 Complicaciones
- 10 Forma clínica espontánea
- 11 Tratamiento
- 12 Oxigenación hiperbarica
- 13 Tratamiento quirúrgico
- 14 Véase también
- 15 Fuentes
Definición
Popularmente, la gangrena es al parecer conocida. Se escucha con frecuencia decir que "a fulano le picó gangrena" y murió, lo que hace pensar en una relación directa entre esta y la muerte. No están muy lejos de la verdad si se tiene en cuenta que un paciente con esta afección (de cualquier tipo) va a perder, cuando menos, el área afectada, pero también puede ser la extremidad y la vida.
Se define como la muerte o necrosis de células individuales o tejidos de un organismo vivo. La causa fisiológica inmediata de esta es la obstrucción del aporte de sangre arterial y entre los síntomas fundamentales están la pérdida de la sensibilidad y de la función, donde la parte afectada, por lo general una extremidad, se vuelve fría y adquiere progresivamente una coloración más oscura y, por último, sufre descomposición. Tiene dos formas: la gangrena seca y la húmeda, entre las que se señalan la gangrena diabética y la gaseosa.
La gangrena seca o crónica se produce cuando existe una obstrucción gradual de las arterias y los tejidos quedan sin riego sanguíneo. Esta situación puede ser resultado de un proceso arterioesclerótico, una lesión por congelación, una herida, o el colapso vascular que puede acompañar a la diabetes mellitus. El paciente puede permanecer largos períodos sin tratamiento quirúrgico.
Si en un paciente con diabetes mellitus, las bacterias (generalmente gramnegativas) infectan los tejidos muertos o exangües, se produce una gangrena diabética con secreción, fetidez y pérdida de la estructura normal de la extremidad, cuyo tratamiento se espera que compense el desequilibrio metabólico ocurrido; si es una bacteria anaerobia Clostridium, el proceso se denomina gangrena húmeda o aguda. También se conoce por el término gangrena gaseosa, debido a su exudado gaseoso de olor pútrido. En estos casos la temperatura se eleva bruscamente, se experimenta gran dolor, anemia aguda y postración. La gangrena húmeda puede aparecer tras la contaminación de una herida, con tierra u otros materiales infectados, lo cual es frecuente en las heridas de guerra, y todavía sucede en las personas con diabetes mellitus y después de haberse efectuado un aborto en condiciones antihigiénicas. Este tipo de gangrena es mortal, a menos que se trate de forma enérgica con antibióticos; la cirugía constituye una emergencia médica.
Antes de Pasteur, la gangrena gaseosa parecía ser una característica inevitable de las operaciones quirúrgicas. Fue Joseph Lister (1827-1912), cirujano británico que con el descubrimiento de los antisépticos en 1865 contribuyó a reducir en gran medida el número de muertes por infecciones contraídas en el quirófano, logrando poner en práctica las terías de Pasteur, y eliminó de los hospitales la gangrena y las complicaciones quirúrgicas infecciosas. La incidencia de la gangrena, al comenzar la guerra de 1914-1918, era de 12 % en el número de heridos, donde moría de 20 a 25 % de estos. La elevada frecuencia de esta afección durante las guerras, se debe a los grandes traumas, a las importantes contaminaciones y al retraso en el desbridamiento quirúrgico.
El empleo de las técnicas de antisepsia, el desbridamiento y la limpieza de las heridas, así como el mayor conocimiento de los gérmenes que puede producir esta enfermedad, hizo que la incidencia al terminar la guerra descendiera a menos de 1 %. Bowby, por ejemplo, informó en 1919 que de 25 000 heridos atendidos por él en 1918, solo 84 de ellos se infectaron, lo que significó 0,34 %. En tiempo de paz, 50 % de las contaminaciones por Clostridium perfringens, septicum y oedematiens ,respectivamente, son secundarias a accidentes, mientras que los 50 % restantes complican tanto la cirugía intestinal como la de la vía biliar.
Las condiciones de supervivencia en el mundo reinante hacen que cada día las personas se expongan más a mecanismos que atentan contra su integridad o, con los factores de riesgo que genera la vida moderna, adquieran una enfermedad crónica que favorezca la afección.
Bioquímica de la lesión y la muerte celular
Varios elementos intervienen en la producción de la lesión y la muerte celular en los tejidos afectados por la isquemia y el Clostridium.
1. Oxígeno y radicales libres derivados del oxígeno. La isquemia produce perioxidación oxidativa.
2. Calcio intracelular y pérdida de la homeostasis del calcio. La isquemia y ciertas toxinas ocasionan un aumento precoz de calcio citosólico, debido a la afluencia neta de calcio++ a través de la membrana plasmática y la liberación de calcio desde la mitocondria y el retículo endotelial. Estos, a su vez, activan enzimas con efectos celulares potencialmente nocivos: fosfolipasas, que fomentan la lesión celular; las proteasas, que inhiben la acción de las proteínas; las adenosintrifosfatasas (ATPasas), que aceleran la depleción de adenosintrifosfato (ATP); y las endonucleasas, que fragmentan la cromatina.
3. Depleción de ATP. La isquemia y las toxinas producen disminución de la síntesis de ATP y pérdida de nucleótidos mitocondriales de piridina con depleción de ATP. Este es necesario para los procesos de síntesis y degradación de las células que comprenden.
Factores favorecedores
Para que se produzca una sepsis por clostridios es obligada la asociación de dos elementos esenciales:
La asociación del germen y la isquemia puede encontrarse en diversas situaciones, tales como: en la atrición de tejido muscular y conectivo, en la existencia de cuerpos extraños, en heridas contaminadas con tierra, en heridas anfractuosas y profundas que inducen a la falta de O2, en fracturas múltiples por accidentes del tránsito, en las heridas de guerra (potencialmente contaminadas por la pólvora, tierra, cuerpos extraños y otras), así como en la isquemia crónica de las extremidades, la fatiga, el hambre, la anemia, la hipoproteinemia, el alcoholismo, la inmunodeficiencia congénita, o adquirida por el virus de la inmunodeficiencia humana o medicamentos como la azatioprina, ciclosporina y los esteroides. La diabetes mellitus, las enfermedades neoplásicas (en particular del tubo digestivo y colon), la neutropenia, la aplasia medular y la leucosis, pueden desencadenar espontáneamente, sin traumatismos o cirugía previa, las sepsis por clostridios en tejidos blandos en cualquier localización.
Clostridios microbiología
Clostridio es el nombre común de un género de bacterias (anaerobias) caracterizadas por producir esporas terminales que deforman los bacilos. Estos microorganismos son importantes por los daños que pueden provocar en las personas y por los beneficios económicos que ocasionan. Algunas especies producen las toxinas más potentes que se conocen, afectan a las terminaciones nerviosas, conllevan a una parálisis generalizada y provocan la muerte; en el botulismo, la toxina se encuentra en alimentos, sobre todo en conservas; en el tétanos, esta es originada por los bacilos que contaminan una herida profunda. Para la identificación de los clostridios de forma indirecta se realiza la tinción de Gram. Este método de identificación recibe este nombre por ser el médico danés Hans Christian Joachim Gram quien lo desarrolló en 1884.
Tras la tinción, las bacterias grampositivas retienen el tinte y se colorean de violeta, mientras que las gramnegativas liberan el tinte y se tiñen de color rosado. Las primeras de estas tienen paredes celulares más gruesas que las segundas. Los clostridios en los tejidos blandos son bacilos grampositivos, esporulados que miden generalmente 1-5 µm de largo por 0,5 de ancho. Son anaerobios estrictos y movibles, característica que pierden en pocos segundos, por pequeñas cantidades de oxígeno.
Todos los clostridios son capaces de producir esporas. Estas constituyen su forma de reproducción y también un modo de resistencia al medio adverso. Cuando las condiciones ambientales son desfavorables, el clostridio en los tejidos blandos aglutina todo su material genético en una porción de su citoplasma y constituye la espora, una pequeña estructura ovalada, situada en posición subterminal, que no crea, como en otros clostridios, protrusión en el bacilo y que resulta viable, aún después de la destrucción de este.
Las esporas son extraordinariamente resistentes al frío, a la luz solar, al desecado y a muchos agentes químicos. Son muy termorresistentes: hasta 121 °C durante 3 minutos. Los clostridios o sus esporas se han encontrado en todas las muestras de tierra tomadas al azar, en deyecciones animales, en especial equinos, ropas de lana y otras; en humanos, se ha encontrado en la piel, en el tubo gastrointestinal (preferentemente en el colon y por lo tanto en sus heces), en la vesícula biliar y en el tracto genital femenino (en la vagina en particular).
Las toxinas que son secretadas por las bacterias vivas se denominan exotoxinas, mientras que las que se liberan por la ruptura de las paredes de las propias bacterias al morir son llamadas endotoxinas. Los clostridios producen varias clases de exotoxinas: alfa (α), beta (β), gamma (γ), delta (δ), épsilon (ε), eta (η), theta (θ), iota (ι), kappa (κ), lambda (λ), mi (μ) y ni (ν). Unas son hemolíticas y otras poseen poder enzimático para los lípidos. Las exotoxinas son responsables de la destrucción tisular, la hemólisis y la insuficiencia multiorgánica. Producen lecitinazas (entre las que se encuentran la hemolisina y el factor de necrosis mística), así como colagenasas e hialuronidasa, verdaderos factores de difusión.
Esta acción enzimática produce sustancias volátiles: amoníaco y gas sulfuroso, liberación de H2 y CO2 y de ácido acetoacético, betahidroxibutírico y otros ácidos grasos. Se produce trombosis de capilares, lo que ocasiona el edema que unido a los gases desencadenan intenso dolor y tumefacción. Las toxinas y los productos formados por la desintegración de las células, tejidos y órganos se diseminan por todo el organismo y provocan efectos deletéreos (sobre la sangre, el medio interno, el hígado, el riñón, el corazón) y causan la muerte.
En la práctica médica, los clostridios en tejidos blandos son numerosos, pero los que más se presentan son tres:
1. Clostridium perfringens, conocido también como Clostridium welchii. Esta bacteria, cuya secuencia genética fue completada en el 2002, es una de las especies que provoca mayor número de casos. Es el más frecuente (75 % de los pacientes) y el más grave, pues su mortalidad es de 56%. Se le encuentra de forma extraordinariamente común en los suelos, junto al Clostridium tetani. Es el único inmóvil, pero el más mortífero entre los clostridios en partes blandas. La bacteria se instala en heridas o en zonas donde el tejido estaba previamente dañado y produce burbujas de gas bajo la piel. Genera poderosas exotoxinas y otras enzimas que pueden originar vasoconstricción, necrosis de los tejidos sanos o destrucción de las células sanguíneas. Estas toxinas inducen las manifestaciones clínicas de la enfermedad, tales como: fiebre, sudoración u olor fétido de la herida. Se han decrito 4 tipos de Clostridium perfringens: el A, patógeno para el hombre y los tipos B, C y D que ocasionan otros tipos de enfermedades en animales. Es un huésped normal en el intestino del hombre.
2. Clostridium oedematiens o Clostridium novyi. Bacteria aislada por Novy en 1894 (en curieles). Es un bacilo grande, patógeno para el hombre, de movimientos lentos, esporas ovales y grandes centrales subterminales. Se han registrado en 26 % de los casos de la enfermedad, son pocos productores de gas y mueren 25 % de los afectados. Es un huésped normal en el intestino de animales. .
3. Clostridium septicum. Esta especie fue aislada en 1887 por Pasteur (de la sangre de un caballo muerto y de una vaca muerta) es el menos frecuente. La mortalidad también es de 25%. Se caracteriza por ser móvil, de espora oval central o subterminal. Es patógeno para el curiel, la paloma y el conejo. Produce poco gas y elabora exotoxina soluble y hemolítica. En procesos gangrenosos en los humanos pueden aparecer otros clostridios: Clostridium histoliticum (intensamente proteolítico), Clostridium fallax (moderadamente patógeno) y Clostridium bifermatans.
Características clínicas
El cuadro clínico de la enfermedad es diverso y puede variar desde una simple crepitación o un edema hasta la sepsis generalizada establecida, pues depende del tipo de anaerobio y de las condiciones del paciente. Su rápida identificación es de gran importancia para preservar la vida de quienes la padecen.
Antecedentes
Hay evidencia de traumatismo accidental o quirúrgico, inyecciones en instituciones de salud o no, cateterismos, punciones, lesiones autoinfringidas (convictos, psicópatas y drogadictos) y en úlcera crónica de los miembros inferiores. El período de incubación transcurre desde pocas horas del trauma a varias semanas (por lo general entre 2 y 4 días).
Formas clínicas
La gangrena gaseosa se ha denominado la enfermedad de las 3E: edema, enfisema y esfacelos, de ahí sus tres formas clínicas: 1. Crepitante 2. Edematosa 3. Tóxica
Examen general
El paciente se muestra con inquietud y angustia, sus ojos se ven hundidos y vidriosos. Si la infección es por Clostridium perfringens las mejillas frecuentemente están enrojecidas, como maquilladas con "colorete". Se observa palidez cérea de la cara facies y puede existir ictericia, además de fiebre elevada (de 38,5-39 oC).
Examen local
Piel: La zona afectada es muy dolorosa, se observa tensa y brillante, dada la tensión que producen el enfisema y el edema subyacentes. Existe dolor de gran intensidad y pueden encontrarse manchas bronceadas de Velpeau. Es característica, a la palpación, la crepitación del gas subyacente del enfisema. El edema y el enfisema se extienden desde la zona lesionada de la extremidad, en dirección centrípeta, en busca del tronco.
Si existe herida, sus bordes estarán necróticos y la secreción será escasa, turbia, pardusca, como lavado de carne, fétida, pútrida, con olor que muchos semejan a ratón muerto, acompañada de gas que brotará en forma de burbujas que dejarán oír una evidente crepitación, generalmente no hay pus y se observan los esfacelos y los músculos desvitalizados (como carne hervida).
Durante la intervención quirúrgica se observa el aspecto pálido de los músculos, como de carne cocida, exudación de abundante líquido y extravasación de sangre que se difunde por estos y le da un color oscuro como de jalea de grosellas, que además, no sangra al corte y no se contrae cuando se le pinza.
Exámenes complementarios
1. Hemograma • Hemoglobina: Anemia. Los glóbulos rojos estallan producto de las hemolisinas de los clostridios. • Leucocitosis: Puede alcanzar cifras 20 a 30x109/L, con predominio de neutrófilos, en ocasiones absoluto, casi siempre por encima de 90-95 %. Presencia de formas juveniles como células en banda, con desviación intensa hacia la izquierda y posible aparición de blastos en la periferia, caracterizados por una reacción leucemoide; todo ello acompañado de disminución de los linfocitos y ausencia de eosinófilos. 2. Coloración de Gram: Aparecen bacilos grampositivos, esporulados o no. También se tomará muestra de la secreción y se preservará introducida en thioglicolato u otro agente similar para preservar el medio anaerobio. Se hará la siembra y el cultivo mediante técnicas para anaerobios. 3. Cultivo y antibiograma para gérmenes aerobio y anaerobio, así como icológico. 4. Gasometría: Acidosis metabólica con disminución de la saturación de oxígeno. 5. Ionograma: El potasio se eleva por la liberación durante la hemólisis. 6. Bilirrubina elevada. 7. Hemocultivo: Debe realizarse siempre en los picos febriles. En la gangrena gaseosa solo 15 % de los pacientes hace una bacteriemia en los estadios finales. 8. Radiografía de la zona afectada: se realizará por la técnica de partes blandas, en dos vistas y de forma seriada, con intervalos de pocas horas. El gas exógeno, aire atrapado en una herida anfractuosa, o quizá agua oxigenada de una cura previa, tiende a desaparecer en los estudios seriados. Se observarán las burbujas de gas en forma de sartas de perlas, por debajo de la fascia y adyacente al hueso. 9. Ecografía y tomografía axial computarizada de abdomen, pelvis, tórax y cabeza: pueden mostrar el gas. 10. Aislamiento de los gérmenes por inmunofluorescencia. 11. La biopsia por congelación pone en evidencia la necrosis tisular y la presencia de bacilos en los casos de sepsis clostridiana.
Diagnostico
Diagnóstico positivo: Es necesario tener en cuenta los antecedentes del paciente, el examen físico y los resultados de los exámenes complementarios para la confirmación.
Diagnóstico diferencial
Es difícil de hacer por la similitud en la presentación clínica de los síntomas. Desde el punto de vista práctico, más que la identificación de estos procesos específicos, lo que realmente interesa es determinar precozmente, por la gravedad que entrañan, la extensión de la lesión, las estructuras afectadas y el grado de afectación general, de modo que pueden señalarse:
Contaminación simple: Puede existir antecedente traumático con herida contaminada (hierbas, deyecciones de animales o atrición muscular por arrancamiento, magulladura o aplastamiento). Si existen clostridios, esporas y todas las condiciones para su desencadenamiento, significa una conducta consecuente, de ahí la necesidad de plantearnos esta clasificación.
Celulitis anaeróbica: Es la irrupción de los clostridios en el tejido celular subcutáneo y el desarrollo de un cuadro clínico definido por encima de la aponeurosis o de sepsis suprafascial. Existe generalmente antecedente de ulceración o pinchazo. Aparece febrícula y toma moderada del estado general. En la zona afectada hay aumento de volumen, dolor y crepitación. En ocasiones, una radiografía hecha por la técnica de partes blandas, pudiera mostrar el gas limitado al tejido celular subcutáneo, sin invasión de los planos profundos, es decir, de los músculos. Solo el desbridamiento y la limpieza quirúrgica de la zona, en muchas ocasiones podrán dar la seguridad de su profundidad.
Miositis estreptocócica: Hay infección masiva de los músculos, con edema exudado seroso, dolor local, formación de gas y cuadro de toxemia generalizada. Existe un eritema cutáneo extenso acentuado, los músculos reaccionan a los estímulos, el olor es diferente y en la coloración de Gram no hay bacilos grampositivos, pero sí numerosos cocos entre el pus, lo cual la diferencia de la miositis por clostridios. Es un cuadro parecido a la gangrena gaseosa, pero de curso menos agudo y fulminante, producido por estreptococos que pueden asociarse con otros como los del grupo A y S aureus.
Gangrena estreptocócica hemolítica. En ocasiones aparece luego de una cirugía menor o traumas (en extremidades, periné, cara y otras partes). Puede ocasionar fiebre, taquicardia y toxemia. Desde el punto de vista local existe dolor, edema, eritema y crepitación con área de necrosis superficial que se dispone y sigue un trayecto lineal característico. En la coloración de Gram no hay bacilos grampositivos y en los cultivos se encuentra el estreptococo hemolítico.
Sepsis por estafilococo: De igual manera puede presentarse un cuadro séptico, toxémico y local inflamatorio. En la coloración de Gram no hay bacilos grampositivos y en el cultivo se encuentran el estafilococo dorado.
Mionecrosis por Aeromonas hydrophila: se origina como consecuencia de traumatismos ocurridos en medio acuático, de aguas dulces o relacionados con peces u otros animales de este hábitat.
Diagnóstico por radiografía
Se basa en la observación y distribución de los gases en las partes blandas y la clínica del paciente. Los gases se visualizan como sombras de mayor transparencia. Es necesario también diferenciarlo de la grasa que puede disponerse según la región, ya sea en forma areolar, de estría o circunscrita, como en los lipomas; pero lo fundamental es que el aire aparece más oscuro que la grasa por ser menor su poder de absorción. El gas, según su origen, suele ser exógeno, endógeno y bacteriano. Este diagnóstico no puede realizarse teniendo en cuenta la densidad radiográfica, pues resulta la misma para todas. Se debe tener en cuenta la historia clínica, los antecedentes, el examen físico, entre otros aspectos.
Gas exógeno: Se introduce del exterior por heridas abiertas, intervenciones quirúrgicas, punciones insuflaciones diagnósticas o terapéuticas: neumotórax, neumoperitoneo, retroneumoperitoneo y procedimientos para la video cirugía.
Gas endógeno: Tiene lugar en perforaciones de vísceras huecas.
Gas bacteriano: Se produce por bacterias aerobias y anaerobias como: Celulitis: El gas se dispone en el tejido celular subcutáneo o entre las fascias musculares sin infiltrar el músculo.
Miositis. Existe infiltración de gas entre los haces musculares, los cuales están disociados y necrosados.
Abscesos: Las burbujas gaseosas generalmente aparecen alrededor de los cuerpos extraños o hematomas.
En la práctica, resulta de gran importancia diferenciar el enfisema subcutáneo que se produce en las heridas abiertas y el gas bacteriano. En el enfisema, las burbujas gaseosas se introducen a través de una solución de continuidad de la piel, aparecen tempranamente, están situadas cerca del sitio de la herida, tienden a desaparecer con rapidez, a las 24 horas han disminuido considerablemente y desaparecen por lo general a las 72 horas, son de gran tamaño, de forma irregular y ocupan el intersticio del tejido raumatizado. En el bacteriano, las burbujas de gas aparecen más tardías, lejos del sitio de la herida, no desaparecen espontáneamente y aumentan de forma progresiva y rápida, son pequeñas (por estar expuestas a gran presión) y redondeadas u ovales "en sarta de perlas".
Las heridas cercanas a las articulaciones de gran movilidad, como codo y rodilla, que no se inmovilizan y que el ejercicio puede hacer progresar el gas entre los tejidos, resultan difíciles de diagnosticar.
Complicaciones
Entre las principales complicaciones prevalecen: delirio, daño tisular permanente, incapacitante y deformante, además de ictericia con daño hepático, insuficiencia renal, diseminación de la infección a través del cuerpo (sepsis), estupor, estado de choque, coma y muerte.
Forma clínica espontánea
La forma clínica espontánea de la miositis clostridiana puede presentarse en extremidades, en paredes torácicas o abdominales y es más frecuente que las que tienen un antecedente de una cirugía o de un trauma. La invasión del clostridio se produce por contigüidad, con diseminación hemática y residencia a distancia. Entre las vísceras más frecuentemente afectadas se encuentran la vesícula biliar, los riñones, el colon y el útero. Estas sepsis han recibido el apellido de enfisematosas, de modo que pueden mencionarse, entre otras: la colecistitis enfisematosa y la pielonefritis enfisematosa. También pudieran denominarse gaseosas. La afectación del útero se considera muy grave (por un aborto criminal realizado de forma ilegal y en condiciones higiénicas desfavorables). La invasión del germen se produce por contigüidad o diseminación hemática produciéndose la enfermedad a distancia. La diabetes mellitus, las enfermedades neoplásicas (en particular de tubo digestivo y colon), así como la aplasia medular constituyen las causas conocidas de las formas espontáneas.
Tratamiento
Será profiláctico, médico y quirúrgico
Tratamiento profiláctico
Limpiar cuidadosamente cualquier herida cutánea y observar la presencia de signos que revelen infección (enrojecimiento, dolor, drenaje o hinchazón alrededor de la herida). Resulta de vital importancia el desbridamiento quirúrgico y la extirpación del tejido desvitalizado, con extracción de cuerpos extraños como: ropa, hierbas, deyecciones, tierra, entre otros, así como el lavado con solución salina, agua oxigenada, agua ozonizada, permanganato de potasio e hibitane, por citar algunos.
No suturar las heridas de guerra, las anfractuosas, o las de más de 6 horas de evolución y prestar cuidado especial a las lesiones cubiertas por férulas o yesos.
No utilizar pomadas que conviertan la zona en un área de anaerobiosis y se prohíben las inyecciones con jeringuillas y agujas reutilizables fuera de las instituciones asistenciales.
Reactivar el toxoide tetánico o administrar 10 000 unidades de antitoxina tetánica en dosis total, dividida en 3, con intervalos de media hora a una hora. Es preciso efectuar previamente la prueba de sensibilidad si no ha sido vacunado con anterioridad. Realizar el seguimiento periódico de los pacientes con lesiones en los miembros inferiores, especialmente de quienes padecen insuficiencia arterial crónica, diabetes mellitus y de los que tienen muñones de amputación.
Oxigenación hiperbarica
El estudio clínico y experimental del efecto terapéutico del aire comprimido se pacticaba ampliamente en el siglo XIX y la primera barocámara medicinal se construyó en Inglaterra en 1662, pero la historia de la oxigenación hiperbárica comienza a partir de la segunda mitad del siglo XX.
En las condiciones habituales de la respiración, la oxigenación de la hemoglobina alcanza de 96-97 %. Para la saturación completa en la persona sana es necesario solo 35 % del oxígeno del aire que se respira. Los medios líquidos del cuerpo constituyen 70 % de la masa corporal y tienen una capacidad de oxígeno en presencia de oxigenación hiperbárica elevada, cuya cantidad es determinada por la ley de Henry Dalton.
La norma de la cantidad de oxígeno de la sangre constituye, en promedio, 20,3 % según el volumen, de los cuales 20 % está condicionado por el oxígeno ligado a la hemoglobina y 0,3 % por el oxígeno diluido en el plasma, lo cual tiene poca importancia energética. El aumento de la presión de oxígeno inesperado conduce a la disolución complementaria de casi 2,3 mL de oxígeno en 100 mL de sangre por cada atmósfera. Como consecuencia de esto la respiración con oxígeno a la presión de 3 ATA (atmósfera absoluta que representa la suma de las presiones atmosféricas y excesiva) condiciona el aumento de la presión de oxígeno en la sangre arterial de 6 % con respecto al volumen, lo que corresponde al consumo normal de oxígeno por los tejidos del organismo en reposo, o sea, la diferencia arteriovenosa del oxígeno.
La oxihemoglobina no se disocia, pues incluso sin la participación de la hemoglobina, la capacidad de oxígeno de la sangre es suficiente para mantener la vida, y es el llamado "fenómeno de la vida sin sangre". Durante la presión de oxígeno a 3 ATA la mayoría de los tejidos, excepto el miocárdico, satisfacerá la necesidad de oxígeno a expensa de su fracción diluida físicamente; y en eso radica el valor terapéutico de la oxigenación hiperbárica, lo que permite utilizarlo en estados patológicos cuando la hemoglobina se excluye por completo o parcialmente como en los procesos respiratorios, anemias y en las formas tóxicas de las hipoxemias.
Al aumentar la tensión de oxígeno de la sangre arterial, la oxigenación hiperbárica no conduce a la elevación lineal estricta de la presión de oxígeno en los tejidos y células. Petrovski BV plantea que el aumento de la capacidad de oxígeno, de los medios líquidos del organismo en oxigenación hiperbárica, crea condiciones determinadas para depositar oxígeno en los tejidos. Bajo la protección de la oxigenación hiperbárica es posible la desconexión más prolongada de la irrigación del encéfalo y de la médula espinal, lo que sirve de base para emplear este método en la cardiocirugía y en la neurocirugía.
El oxígeno hiperbárico aumenta el tenor de oxígeno a nivel tisular, revierte la deprimida capacidad fagocitaria de los leucocitos en el margen del tejido isquémico infectado y mejora la capacidad de regeneración mística y neutraliza, además, las toxinas de los clostridios, de ahí que se aconseje realizar una sesión de inmediato, antes del acto quirúrgico. En general la dosis es: exposición de 120 minutos 2 veces al día a 2 ó 3 atmósferas durante 7 días como mínimo.
Tratamiento quirúrgico
El tratamiento de esta afección es eminentemente quirúrgico. Al tenerse sospecha de esta, en el caso de las heridas, hay que abrirlas inmediatamente y eliminar suturas, drenajes y otras. Se considera de extrema urgencia: Limpiar intensamente la zona y hacer la resección de todo músculo con cambios de coloración (como carne hervida o jalea de grosellas), que no sangra o no se contrae.
Amputar la extremidad si se considera que no es viable, para lo cual se utilizará la técnica circular (en guillotina), con la incisión en el tejido sano. El muñón debe quedar abierto y dejarse una histoclisis o irrigación continua, con agua oxigenada, solución Dakin, o permanganato de potasio al 1 x 8000, que permitirá el lavado de los diferentes espacios musculares. La miositis por clostridio es una enfermedad que se presenta tanto en tiempo de paz como de guerra, por lo que el dominio en cuanto a diagnóstico y actualidad terapéutica debe resultar la mejor arma para disminuir la incapacidad y la mortalidad que esta ocasiona.