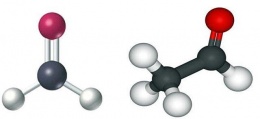
Aldehídos
| ||||||||||
El término Aldehídos proviene de la expresión “alcohol deshidrogenado”, ya que los aldehídos son compuestos intermedios obtenidos en la oxidación de alcoholes primarios a ácidos.
Sumario
Concepto
Son compuestos caracterizados por la presencia del grupo carbonilo (C=O). Presentan el grupo carbonilo en posición terminal mientras que las cetonas lo presentan en posición intermedia. El primer miembro de la familia química de los aldehídos es el metanal o formaldehído (aldehído fórmico).. Teóricamente se puede considerar a los aldehídos como derivados de los hidrocarburos al sustituir dos átomos de hidrógeno de un carbono terminal por un átomo de oxígeno. Su fórmula general es CnH2nO. Los aldehídos* se nombran añadiendo al nombre del hidrocarburo del que derivan el sufijo al o el sufijo dial, según que el grupo carbonilo, "C=O, ocupe uno o los dos extremos de la cadena.
El grupo carbonilo, "C=O, tiene preferencia sobre los radicales, las instauraciones y los alcoholes, debiéndose empezar a numerar el compuesto por el extremo donde se encuentra dicho grupo carbonilo. Solo cuando existen grupos carbonilo en los dos extremos se tienen en cuenta los criterios sobre alcoholes, insaturaciones y radicales para decidir por donde se comienza a numerar la cadena.
Nomenclatura
La terminación ol de los alcoholes se sustituye por al. Sin embargo los primeros de la serie son más conocidos por sus nombres comunes.
Metanal : formaldehido
Etanal: acetaldehído
El aldehído aromático se llama benzaldehído.
Fuentes naturales
Los aldehídos están ampliamente presentes en la naturaleza. El importante carbohidrato glucosa, es un polihidroxialdehído. La vanillina, saborizante principal de la vainilla es otro ejemplo de aldehído natural.
Probablemente desde el punto de vista industrial el más importante de los aldehídos sea el formaldehido, un gas de olor picante y medianamente tóxico, que se usa en grandes cantidades para la producción de plásticos termoestables como la bakelita.
La solución acuosa de formaldehido se conoce como formol o formalina y se usa ampliamente como desinfectante, en la industria textil y como preservador de tejidos a la descomposición.
Propiedades físicas
Los primeros aldehídos de la clase presentan un olor picante y penetrante, fácilmente distinguible por los seres humanos.
El punto de ebullición de los aldehídos es en general, mas alto que el de los hidrocarburos de peso molecular comparable; mientras que sucede lo contrario para el caso de los alcoholes, así, el acetaldehído con un peso molecular 44 tiene un punto de ebullición de 21°C, mientras que el etanol de peso 46 hierve a 78°C.
La solubilidad en agua de los aldehídos depende de la longitud de la cadena, hasta 5 átomos de carbono tienen una solubilidad significativa como sucede en los alcoholes, ácidos carboxílicos y éteres. A partir de 5 átomos la insolubilidad típica de la cadena de hidrocarburos que forma parte de la estructura comienza a ser dominante y la solubilidad cae bruscamente.
El metanal es un gas de olor penetrante que al ser aspirado produce irritación y lagrimeo. El etanal tiene un agradable olor a frutas. A partir del etanal y hasta el de doce átomos de carbono son líquidos. Los restantes son sólidos.
Todos los aldehídos son menos densos que el agua. Los primeros de la serie son solubles en agua pero la solubilidad disminuye a medida que aumenta el número de átomos de carbono. Hierven a menor temperatura que los respectivos alcoholes.
Punto de Ebullición: los puntos de ebullición de los aldehídos y cetonas son mayores que el de los alcanos del mismo peso molecular, pero menores que el de los alcoholes y ácidos carboxílicos comparables. Esto se debe a la formación de dipolos y a la ausencia de formación de puentes de hidrógeno intramoleculares en éstos compuestos.
(Constantes físicas de algunas aldehídos)
Los aldehídos pueden ser alifáticos o aromáticos en dependencia de si el grupo funcional se acopla a un radical alquilo (R) o arilo (Ar) respectivamente, por el otro enlace disponible.
El primer miembro de la clase de los aldehídos alifáticos es el formaldehído (CH2O), y es el único que posee dos átomos de carbono acoplados al grupo carbonilo. Esta diferencia estructural hace que tenga ciertas características que lo distinguen del resto de la clase. El segundo miembro se llama acetaldehído (CH3CHO) de estructura.
En los aldehídos aromáticos el primer miembro es el benzaldehído, con un anillo bencénico acoplado al grupo carbonilo.
Propiedades químicas
Debido a la diferencia de electronegatividad entre el oxígeno y el hidrógeno del grupo, se produce una polarización lo que los vuelve muy reactivos.
Se oxidan con facilidad transformándose en los ácidos carboxílicos respectivos. El carácter reductor de los aldehídos se verifica con la reacción de Tollens (nitrato de plata amoniacal); los productos de esta reacción son el ácido respectivo y un vistoso espejo de plata que permite identificar al grupo.
El grupo carbonilo de los aldehídos en fuertemente reactivo y participa en una amplia variedad de importantes transformaciones, que hacen de la química de los aldehídos un tema extenso y complejo. Aqui solo no limitaremos a tratar someramente algunas de sus reacciones características.
Reducción a alcoholes
Por contacto con hidrógeno en presencia de ciertos catalizadores el doble enlace carbono - oxígeno del grupo carbonilo se rompe y un átomo de hidrógeno se acopla a uno de los enlaces para formar el grupo hidroxilo típico de los alcoholes.
Reducción a hidrocarburos
Los aldehídos pueden ser reducidos a hidrocarburos al interactuar con ciertos reactivos y en presencia de catalizadores. En la reducción Wolff-Kishner el acetaldehído se trata con hidrazina como agente reductor y etóxido de sodio como catalizador. El resultado de la reacción produce una mezcla de etano, agua y nitrógeno.
Polimerización
Los primeros aldehídos de la clase tienen un marcada tendencia a polimerizar. El formaldehido por ejemplo, polimeriza de forma espontánea a temperatura ligeramente superior a la de congelación (-92°C).
Del mismo modo, cuando se evapora una solución al 37% de formaldehido en agua que contenga de 10 a 15% de metanol se produce un polímero sólido que se conoce como parafolmaldehído. Si se calienta el parafolmaldehído se vuleve a producir el formaldehido en forma gaseosa.
También se forman polímeros cuando las soluciones de formaldehido o acetaldehído se acidifican ligeramente con ácido sulfúrico.
Reacciones de adición
Los aldehídos también sufren reacciones de adición, en las cuales se rompe la estructura molecular del aldehído y el agente reaccionante se agrega a la molécula para la formación de un nuevo compuesto.
Los aldehídos se comportan como ácidos debido a la presencia del grupo carbonilo, esto hace que presenten reacciones típicas de adición nucleofílica.
Reacciones de adición nucleofílica: Estas reacciones se producen frente al (reactivo de Grignard), para dar origen a un oxihaluro de alquil-magnesio que al ser tratado con agua da origen a un alcohol. El metanal forma alcoholes primarios y los demás aldehídos forman alcoholes secundarios.
Otras reacciones de adición nucleofílica pueden producirse con el ácido cianhídrico, el sulfito ácido de sodio, la hidroxilamina, hidracina, semicarbacida, fenilhidracina y con el 2,4 dinitrofenilhidracina, para dar origen a diferentes compuestos químicos.
Los aldehídos también pueden dar origen a otros compuestos mediante reacciones de sustitución halogenada, al reaccionar con los halógenos sustituyen uno o varios hidrógenos del carbono unido al carbonilo.Este método permite obtener la monobromoactona que es un poderoso gas lacrimógeno.
Reacciones de condensación aldólica: En esta reacción se produce la unión de dos aldehídos o dos cetonas en presencia de una solución de NaOH formando un polímero, denominado aldol.
Reacciones de oxidación: Los aldehídos se oxidan con facilidad frente a oxidantes débiles produciendo ácidos. Mientras que las cetonas sólo se oxidan ante oxidantes muy enérgicos que puedan romper sus cadenas carbonadas. Es así que las reacciones de oxidación permiten diferenciar los aldehídos de las cetonas en el Laboratorio. Síntesis y obtención de aldehídos y cetonas alifáticas:
La hidratación de alquinos en presencia de ácido sulfúrico en solución acuosa y sulfato mercúrico permite obtener aldehídos.
Obtención: se preparan básicamente por oxidación suave de alcoholes primarios.
Usos: el aldehído más utilizado es el metanal o formaldehido. En solución acuosa al 40 % se lo conoce con el nombre de formol. Se utiliza en la industria para conservar maderas, cueros y en taxidermia. Debido a la posibilidad de polimerizarse se utiliza en la industria de plásticos como la baquelita.
El etanal se utiliza en la fabricación de espejos (reacción de Tollens y en la preparación de ácido acético.
El benzaldehído se emplea en la preparación de medicamentos, colorantes y en la industria de los perfumes.
Usos
El metanal o aldehído fórmico es el aldehído con mayor uso en la industria, se utiliza fundamentalmente para la obtención de resinas fenólicas y en la elaboración de explosivos (pentaeritrol y el tetranitrato de pentaeritrol, TNPE) así como en la elaboración de resinas alquídicas y poliuretano expandido.
También se utiliza en la elaboración de uno de los llamados plásticos técnicos que se utilizan fundamentalmente en la sustitución de piezas metálicas en automóviles y maquinaria, así como para cubiertas resistentes a los choques en la manufactura de aparatos eléctricos. Estos plásticos reciben el nombre de POM (polioximetileno)
Muchos aldehídos y cetonas forman parte de los aromas naturales de flores y frutas, por lo cual se emplean en la perfumería para la elaboración de aromas como es el caso del benzaldehído (olor de almendras amargas), el aldehído anísico (esencia de anís), la vainillina, el piperonal (esencia de sasafrás), el aldehído cinámico (esencia de canela). De origen animal existe la muscona y la civetona que son utilizados como fijadores porque evitan la evaporación de los aromas además de potenciarlos por lo cual se utilizan en la industria de la perfumería.
Fuente
- Química orgánica