Aminas
| ||||||||||
Aminas: Proviene de la sustitución de un hidrógeno del amoniaco por un radical de hidrocarburo.
Sumario
Aminas
Las aminas están clasificadas dependiendo el número de carbonos directamente unidos al nitrógeno, se dividen en primaria secundarias y terciarias.
Primarias R-NH2
Secundarias R-NH-R’
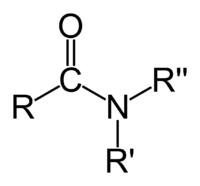
Terciarias R,R´,R” N
Estructura y enlace
Las aminas son compuestos nitrogenados con estructura piramidal, similar al amoniaco. El nitrógeno forma tres enlaces simples a través de los orbitales con hibridación sp3. El par solitario ocupa el cuarto orbital con hibridación sp3 y es el responsable del comportamiento básico y nucleófilo de las aminas.
Nomenclatura
Las aminas se pueden nombrar como derivados de alquilaminas o alcanoaminas.
Si un radical está repetido varias veces, se indica con los prefijos di-, tri-,...
Si la amina lleva radicales diferentes, se nombran alfabéticamente.
Los sustituyentes unidos directamente al nitrógeno llevan el localizador N. Si en la molécula hay dos grupos amino sustituidos se emplea N, N'.
Cuando la amina no es el grupo funcional pasa a nombrarse como amino-. La mayor parte de los grupos funcionales tienen prioridad sobre la amina (ácidos y derivados, carbonilos, alcoholes)
Veamos algunos ejemplos.
Propiedades Físicas
Las aminas son compuestos incoloros que se oxidan con facilidad lo que permite que se encuentren como compuestos coloreados. Los primeros miembros de esta serie son gases con olor similar al amoníaco. A medida que aumenta el número de átomos de carbono en la molécula, el olor se hace similar al del pescado. Las aminas aromáticas son muy tóxicas se absorben a través de la piel.
Solubilidad: Las aminas primarias y secundarias son compuestos polares, capaces de formar puentes de hidrógeno entre sí y con el agua, esto las hace solubles en ella. La solubilidad disminuye en las moléculas con más de 6 átomos de carbono y en las que poseen el anillo aromático.
Punto de Ebullición: El punto de ebullición de las aminas es más alto que el de los compuestos apolares que presentan el mismo peso molecular de las aminas. El nitrógeno es menos electronegativo que el oxígeno, esto hace que los puentes de hidrógeno entre las aminas se den en menor grado que en los alcoholes. Esto hace que el punto de ebullición de las aminas sea más bajo que el de los alcoholes del mismo peso molecular.
(Constantes físicas de algunas Aminas)
Las aminas presentan puntos de fusión y ebullición más bajos que los alcoholes. Así, la etilamina hierve a 17ºC, mientras que el punto de ebullición del etanol es de 78ºC.
CH3CH2OH P.eb. = 78ºC
CH3CH2NH2 P. eb. = 17ºC
La menor electronegatividad del nitrógeno, comparada con la del oxígeno, hace que los puentes de hidrógeno que forman las aminas sean más débiles que los formados por los alcoholes.
Propiedades Químicas
Las aminas se comportan como bases. Cuando una amina se disuelve en agua, acepta un protón formando un ión alquil-amonio.
Propiedades ácido-base
Las aminas presentan hidrógenos ácidos en el grupo amino. Estos hidrógenos se pueden sustraer empleando bases fuertes (organometálicos, hidruros metálicos) formando los amiduros (bases de las aminas).
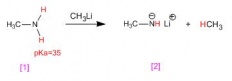
Las aminas se comportan como bases a través del par libre del nitrógeno. También se comportan como ácidos débiles pudiendo desprotonarlas mediante el empleo de bases muy fuertes (organolíticos)
La metilamina [1] reacciona con metillitio, transformándose en su base conjugada, el metilamiduro de litio [2]. Por su parte, el metillitio se transforma en su ácido conjugado, el metano.
Identificación en el laboratorio
Para diferenciar las aminas entre sí en el laboratorio se hacen reaccionar con una solución de nitrito de sodio y ácido clorhídrico, esto da origen a ácido nitroso inestable. Cada tipo de amina tendrá un comportamiento diferente frente al ácido nitroso, dependiendo además de la temperatura a la cual se lleve a cabo la reacción.
Métodos de obtención
a) Reducción de compuestos de nitrógeno insaturados
Los compuestos insaturados de nitrógeno, como son los nitrocompuestos, nitrilos y amidas, pueden reducirse hasta aminas primarias mediante hidrógeno en presencia de catalizadores o bien con reductores químicos (hidruro de litio y aluminio, estaño o hierro y ácido clorhídrico). La reducción de nitrocompuestos es de gran utilidad para la obtención de aminas aromáticas, dada la facilidad de nitración de los anillos aromáticos. Así se prepara por ejemplo, la anilina, por reducción del nitrobenceno:
En el laboratorio suele llevarse a cabo esta reducción mediante estaño y ácido clorhídrico, mientras que en la industria se emplean limaduras de hierro en presencia de agua y una pequeña cantidad de ácido clorhídrico.
b) Reacción de amoniaco con halogenuros de alquilo.
El amoniaco reacciona con los halogenuros de alquilo para formar, en primer lugar, una sal de alquilamonio, de la que puede liberarse la amina (base débil), por tratamiento con hidróxido sódico (base fuerte)
Sin embargo, la reacción no es tan sencilla, porque las aminas pueden atacar, a su vez, al halogenuro de alquilo, formándose así, sucesivamente, sales de di-, tris y tetra-alquilamonio. Por ello en la práctica se obtiene una mezcla de aminas primarias, secundarias y terciarias, que pueden separarse por destilación fraccionada. Por otro lado, se puede favorecer el rendimiento en el tipo de amina deseado, modificando la relación de concentraciones de los reactivos iniciales: así, empleando un gran exceso de amoniaco predomina, como es lógico, la formación de amina primaria, mientras que un exceso de halogenuro de alquilo favorece la formación de amina terciaria.
Reacciones de las aminas
a) Las aminas presentan un carácter marcadamente básico que se pone de manifiesto en la formación de sales. Estas sales son sólidos incoloros, no volátiles, solubles en agua e insolubles en disolventes orgánicos.
b) La reacción con el ácido nitroso permite diferenciar entre aminas primarias, secundarias y terciarias. Así:
• Las aminas primarias reaccionan con desprendimiento de nitrógeno
• Las aminas secundarias reaccionan lentamente en caliente con el ácido nitroso formando nitrosaminas con apariencia aceitosa:
• Las aminas terciarias tratadas con exceso de ácido nitroso conducen a la formación de nitritos.
Aplicaciones
Se encuentran formando parte de la naturaleza, en los aminoácidos que conforman las proteínas que son un componente esencial del organismo de los seres vivos. Al degradarse las proteínas se descomponen en distintas aminas. Unas emiten olor desagradable.
Las aminas como compuestos son muy importantes y reconocidas en industrias como las cosméticas y textiles por el uso o aplicación de la p-Fenilendiamina y algunos derivados se usan en composiciones para teñir el pelo y como antioxidantes para caucho.
Fuente
Química Orgánica
Referencia Bibliográfica
Enlaces externos