Dermatomicosis
| ||||
Dermatomicosis. La dermatomicosis es una enfermedad infecciosa y contagiosa que afecta la piel y pelos, caracterizada por la producción de zonas alopécicas costrosas y que es producida varios tipos de hongos de patogenicidad variable, que afecta a casi todas las especies animales y el hombre.
Sumario
Sinonimias
Tiña, pelada, favus, dermatofitosis, herpes.
Historia y distribución geográfica
Las dermatomicosis comenzaron a aparecer en el siglo pasa como una entidad criptogámica de los pelos, la piel y el cuero cabelludo, designada como herpes circinado o Dermatofitia cutánea a las localizaciones en las regiones cutáneas no pilosas del cuerpo, siendo descubierta la etiología de estas lesiones a mediados del siglo pasado.
Ya en 1839 Remark observó filamentos de un hongo en el favus, mientras que Gruby en 1941 descubrió la mayoría de los parásitos de las tiñas. Así mismo Malmstein en 1845 dio el nombre de Trichophyton a los parásitos vegetales que invaden los pelos y producen Tiña tonsurante.
Las dermatomicosis son enfermedades reportadas en todo el mundo, aunque su frecuencia es variable, en dependencia de múltiples factores zootécnicos y climáticos. La enfermedad en Cuba ha sido reportada en todas las provincias, encontrándose principalmente en los bovinos, especialmente en los terneros. Afecta a todos los rebaños, independientemente del propósito productivo, estando más extendida en las unidades con grandes poblaciones de animales jóvenes, como las recrías y centros de desarrollo.
Se presenta con mayor incidencia en las unidades de peores condiciones higiénicas y en la época de seca y frío, aunque se presentan casos durante todo el año.
Importancia socio económica
Desde el punto de vista social la enfermedad constituye por sí sola una zoonosis, lo que se traduce en un riesgo profesional gastos en tratamientos en medidas de protección y en días de licencia en que los trabajadores no concurren al trabajo.
Los factores que contribuyen a diseminar la Tiña, propiciando la transmisión de la enfermedad de los animales al hombre son, entre otros, los siguientes:
- Hábitos higiénicos inadecuados, por el personal que trabaja con los animales afectados.
- Estado inmunológico deficiente.
- Número de fuentes de infección y posibilidades de transmisión existentes en las unidades.
- Distribución geográfica del hongo y el hospedero.
- Intensidad de la infección en los animales.
- Afinidad de los dermatofitos zoófilos para el hombre.
- La existencia de varias formas indirectas de transmisión del animal al hombre.
Desde el punto de vista económico, aunque la enfermedad no causa la muerte de los animales, sí se producen pérdidas considerables, ya que los animales afectados disminuyen la conversión (retraso en el desarrollo), además de los decomisos o devaluaciones que sufren las pieles de dichos animales cuando son sacrificados. Por otra parte es necesario considerar los gastos en tratamientos, medidas de saneamiento y otros utilizados en la recuperación o prevención) de los rebaños (sanos) afectados.
Etiología
Como agentes etiológicos de esta enfermedad se han reportado los siguientes agentes:
- Microsporum canis (perros, gatos y conejos)
- Microsporum gypseum (perros, cerdos y conejos)
- Microsporum audouini (niños)
- Microsporum nanum (cerdo y hombre)
- Microsporum distortum (patógeno ocasional de perros, hombres y primates).
- Trichophyton mentagrophytes (bovinos, cerdos, conejos, aves, ovinos, caprinos, gatos, caballos y hombre.
- Trichophyton equinum (caballo, ocasionalmente en perros verrucosum (bovinos, ovinos y caprinos y de manera ocasional otras especies).
- Trichophyton gallinae (aves, especialmente gallinas, y rara vez al hombre).
- Trichophyton tonsurans (equinos y hombre).
- Trichophyton simii (aves, perros y hombre).
- Trichophyton violaceum (bovinos).
- Trichophyton crateriforme (bovinos).
- Trichophyton faviforme (bovinos).
La etiología de la dermatomicosis es muy variada, ya sea en agentes etiológicos productores de la misma como los animales susceptibles a ellos. Como se comprenderá existen enormes diferencias entre especies en cuanto a la patogenicidad, espectro de especies susceptibles a cada uno de ellos, tenacidad, y otras características del hábitat, los medios de nutrición y cultivo, etcétera, que hacen de los mismos un grupo de agentes de gran complejidad.
En general, a estos hongos se les halla en el suelo y los vegetales, allí viven y se reproducen como cualquiera de las especies comunes, son saprofitos, no necesitan materia viviente, su poder patógeno está en potencia, con facilidades extraordinarias de adaptación. El suelo y las plantas son el reservorio del hongo, allí están cumpliendo una etapa de su ciclo.
La otra etapa de su evolución la lograrán cuando pasen al organismo animal o humano. Los animales que han enfermado de tiña, de acuerdo con pruebas de inmunidad, se mantienen inmunes por largo tiempo. Estudios del comportamiento de las inmunoglobulinas Igm e IgG en conejos inoculados con extractos de micelios de T. mentagrophytes demostraron que en la hemoaglutinación pasiva la mayor actividad fue mayor potencialidad para la inducción a la formación de anticuerpos que otros. Por ejemplo el T. mentagrophytes en los animales da lugar a mayor formación de anticuerpos que agentes del mismo género en el humano.
De acuerdo con el criterio de los investigadores, los hongos, (por ejemplo, el T. verrucosum) tienen tendencia específica por la epidermis y tejidos querantinizados, con tropismo positivo para el estrato corneo, porción queratinizada del pelo y folículos pilosos.
La resistencia de los hongos depende de que forma sea sometida a las determinadas condiciones, ya que las esporas resisten mucho más que las formas vegetativas. Las esporas son capaces de conservar su vida durante muchos años incluso bajo condiciones ambientales desfavorables. Las escamas y costras desprendidas en los establos o pastos resultan infecciosas hasta 2 años después.
De las 80 000 especies de hongos descritas, solamente un centenar se consideran patógenas. Entre estas especies patógenas, el género Triohophyton del grupo dermatofitos, tiene la capacidad mayor de provocar la enfermedad en la mayoría de los animales.
Epizootiología
Se consideran susceptibles a la tiña toda las especies de mamíferos, aves e incluso reptiles. Debido al desarrollo, número y concentración de la masa ganadera bovina (especialmente los terneros), ovinos, porcinos, y aves en todo el mundo, y en particular en el país, es que se hace más evidente la enfermedad en estas especies. No obstante padecen la enfermedad los equinos, caprinos, conejos, perros, gatos, e incluso se han reportado ofidios afectados por distintos hongos.
La tiña es más frecuente en meses de frío, de poca humedad escasa precipitación pluvial. La estabulación en establos calientes, húmedos, sucios, con gruesas capas de estiércol favorece la infección. De igual forma el hacinamiento en explotaciones intensivas hace a los animales más receptivos.
El hecho de que se haya encontrado mayor incidencia en terneros que en otras categorías de edad pudiera deberse aquellos bovinos que enferman a edades tempranas alcanzan un prolongado nivel de inmunidad y a que con el aumento del grosor de la piel disminuye la receptividad al hongo no se han hallado referencias que indiquen que el sexo y la raza sean influyentes en la susceptibilidad a la infección.
En el origen y propagación de la dermatomicosis influyen “muchos factores como son: la humedad, temperatura, lluvia, presiones y condiciones zoohigiénicas como altas concentraciones de CO2, SH2 y amoniaco, modo de manejo, capacidad del establo, desequilibrio mineral (zinc), hipovitaminosis (A y E), etcétera, son factores los que favorecen las condiciones para la actuación queratolítica y proteolítica de las enzimas de los hongos, así como también la actuación del “estrés”, la resistencia inespecífica del animal y la alta susceptibilidad frente a los hongos.
La transmisión se efectúa fundamentalmente por contacto directo, además es frecuente que se transmita por medio del contacto de animales enfermos y sanos con los comederos y bebederos, en los cepos, paredes, horcones, etcéte ra los que se contaminan con los enfermos y posteriormente estos contaminan a los sanos. Indirectamente se transmiten con las costras y pelos que caen y se desecan, las que quedan adheridas a paredes, postes, así como también mediante vectores como los roedores perros y gatos, y según criterios no confirmados, algunos artrópodos (moscas domésticas, piojos y otros). La enfermedad tiene una presentación enzoótica y marcadamente estacional desapareciendo con el inicio de las lluvias del verano.
Patogenia
Las condiciones más favorables para la germinación, crecimiento y multiplicación de las esporas de dermatofitos, tienen lugar en el folículo piloso entre las dos vainas de la raíz del pelo.
Las esporas del hongo se protegen en las grietas de la piel y en los folículos pilosos. Después de germinar las hifas del hongo crecen por el interior del pelo (endotrix). Las esporas llegadas a las excoriaciones de la piel germinan y se desarrollan en la superficie cutánea por debajo de la capa de células queratinizadas, desde la cual pueden alcanzar también los folículos pilosos introduciéndose en ellos.
Según trabajos de inoculación experimental realizados con Trichophyton verrucosum, la patogenia de la enfermedad puede considerarse en cuatro fases:
- Incubación.
- Maduración.
- Clímax.
- regresión.
Curso clínico
El período de incubación y las manifestaciones clínicas están en dependencia del número de células viables del inoculo en el momento de la invasión, observándose los primeros signos clínicos de la infección entre 7 y 35 días post—infección experimental en bovinos agrupados en distintos grupos de edades y con distintos planos nutricionales.
- En bovinos las lesiones se localizan en la cabeza y cuello, y en ocasiones en miembros anteriores y posteriores y la región escrotal. Dichas lesiones se presentan como placas de tendencia circular, de color blanco grisáceo, secas y bien delimitadas.
- En los terneros es común la costra peri ocular, peri bucal en las orejas. Estas lesiones dificultan la succión de che o la aprensión de los alimentos y le producen escozor. La lesión produce un aspecto quebradizo en el pelo, seguido de la costra.
- En la descripción clínica de la dermatomicosis se plantea que primero surge un nódulo pequeño oculto entre los pelos que a simple vista resulta imposible de diagnosticar. Estos nódulos se cubren de escaras (exudado y células inflamatorias) y posteriormente se convierten en gruesas costras color grisáceo.
- En los equinos se presentan lesiones circulares de 20 — 30 mm de diámetro, extendiéndose desde la cara interna de las patas traseras y menudillo hasta la región escrotal, pasando a todas las regiones del cuerpo, excepto la cabeza, que es invadida posteriormente. En estas zonas pueden originarse lesiones eritematosas, además pueden ser presa de infecciones bacterianas, lo que daría lugar a trastornos de mayor consideración.
- En los porcinos se han observado clínicamente lesiones cuya apariencia difiere de la de los animales de largo pelaje, no siendo típicas, ni representativas muchas veces.
- En los caninos las lesiones se localizan en las superficies ventral del torax, cubiertas con escamas y rodeadas por estrechas bandas de pústulas. También se ha observado como lesiones típicas zonas escamosas bien delimitadas, circulares, de preferencia en la cabeza, pecho y abdomen, y menos frecuentemente en piernas y dorso.
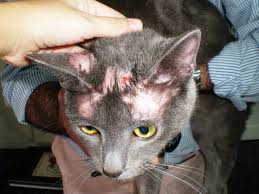
- En los felinos las lesiones son de tipo costrosas, de bordes redondeados y circunscritas y como síntomas característico, áreas depiladas en la cara.
- En los conejos se produce pérdida de pelos y zonas de inflamación con costras y escamas sobre la piel. El T. verruscosum sólo produce inflamación al conejo. Las lesiones se localizan especialmente en la cabeza y orejas.
- En ovejas y cabras al comienzo de la infección se produce una pequeña zona enrojecida en los puntos de la infección, que permanece oculta entre los pelos, posteriormente en ellos se produce una escara que los cubre, la que más tarde se convierte en gruesas elevaciones furfúreas y costrosas de color grisáseo, hay prúpito intenso; lo pelos se tornan sin b y frgiles, y las costras son removibles, similares a la los bovinos.
Lesiones anatomopatológicas
La descripción macroscópica de la lesiones fueron expuestas en los síntomas.
En esta enfermedad se observa un exudado seroso masivo producto de la dilatación de capilares dérmicos, masas polimorfonucleares acompañadas de acantosis e hiperqueratosis en la dermis, posteriormente con formación de costras, el folículo piloso es similarmente infiltrado con formación de microabscasos, los capilares de la dermis son rodeados de masas de las mononucleares, siendo el pelo fragmentado rodeado de masas de artrosporas.
Se presenta hipertrofja de la epidermis que afecta a todas las capas, aunque principalmente al estrato córneo, afectando las porciones proximales de los folículos pilosos, apareciendo los pelos rodeados de escamas queratinizadas y hongos; estando los poros foliculares dilatados y cónicos, el epitelio de los folículos tiende a la hiperqueratosis y la de las áreas intertriginosas sobre las papilas dérmicas a la paraqueratosis, formándose microabscesos en las capas superficiales de la epidermis con folículos supurativa.
Diagnóstico
El diagnóstico clínico se realiza de forma fácil en algunas especies, pero en todos los casos es necesario tener en cuenta el tipo de lesión, su localización, los antecedentes del caso etcétera.
El diagnóstico de laboratorio consiste en: primero se rea4 examen directo, el que se realiza colocando material sospechoso entre dos cubre objetos (o porta y cubre) con hidróxido de sodio y potasio ligeramente calentado, con lo que se pueden observar hifas y artrosporas, La otra forma de diagnóstico más empleada en laboratorio es la siembra para él aislamiento del agente, en medios selectivos para hongos.
El método de fluorescencia se emplea para hacer diagnóstico M. canis, ya que es el único zoofílico que fluorece (ver amarillento). Es preciso realizar el diagnóstico diferencial con otros proceso patológicos cutáneos como las forunculosis, las sarnas, los herpes de origen viral, etcétera. El herpes de etiología viral se diferencia por ser éste productor de una lesión lisa no pruriginoso. Las forunculosis bacterianas presentan el fornúnculo y zonas de inflamación, es circunscripto y supurante. Las sarnas son mucho más pruriginosas y en zonas determinadas la economía, sobre todo en partes de pjel fina.
El diagnóstico epizoótico se basa en los conocimientos que sobre la epizoótica se tengan, como son los datos sobre la incubación, propagación lenta, la morbilidad, la edad de los animales afectados, la estación del año, así como el resultado de las investigaciones realizadas en el laboratorio.
Medidas contraepizoóticas preventivas
Es imposible una prevención de la dermatomicosis, y menos la erradicación usando solamente terapia y la desinfección, sin el constante control de los rebaños y separación de los afectados, además de las restantes medidas. La principal medida preventiva es la vacunación con la vacuna LTF-130 de fabricación soviética, la cual se aplica en los terneros acorde al siguiente esquema: Se administran 5ml de la vacuna por vía intramuscular a los terneros de 28-30 días de nacidos, la que se repite a los 12-15 días de la primera. En caso de comenzar el plan de vacunación en un rebaño por primera vez se vacunará toda la masa menor de un año, pero en este caso se administrarán 10 ó 15 ml de acuerdo al tamaño del animal.
El resto de las medidas preventivas son las mismas usadas en la recuperación (excepto la separación de los enfermos y su tratamiento).
Medidas de recuperación
La primera medida que debe aplicarse en un brote es la separación inmediata de los animales enfermos de los sanos e instaurar el tratamiento indicado al final. El personal que trabaja con los enfermos no debe tener contacto con los animales sanos.
Todo el rebaño debe ser objeto de una revisión diaria minuciosa por personal profesional para detectar nuevos enfermos. Es importante tener presente que las lesiones al principio son pequeñas y están ocultas entre el pelo, lo que a simple vista es difícil de observar. Se situarán cajuelas de desinfección (activadas) entrada de la unidad y en la entrada de cada nave.
Junto con las anteriores medidas se llevará a cabo una limpieza profunda acompañada de desinfecciones periódicas con hidróxido de sodio al 2 % en caliente o con formol al 3 %, haciendo énfasis en los comedores y bebederos, así como en paredes y horcones hasta la altura de los animales. Estas medidas deben complementarse con la incidencia de toda la basura y desperdicios que pueden existir en la unidad.
Finalmente, luego de un período de aproximadamente 60 días de haber desaparecido el último caso se procede a cerrar el foco, para lo que debe realizarse una inspección o evaluación epizoótica del mismo y una desinfección final profunda con hidróxido de sodio al 2 % en caliente o formol al 3 %.
Tratamiento
Se utilizan en el mundo un gran número de medicamentos unos con acción local y otros con efectos sistémicos. La Griseofulvina se emplea en animales afectivos, en dosis de 10- 20 mg/kg de peso, e incluso dosis mayores, durante 3-4 semanas. Por vía oral, no se emplea en animales de objetivos económicos por resultar muy costosa y emplear mucho tiempo de tratamiento. La mayor parte de los medicamentos utilizados para el tratamiento de esta enfermedad son de uso tópico, como por ejemplo: El Micocidín, producto a base de formol y que se emplea previo raspado de las lesiones, generalmente es necesario la repetición del tratamiento 3 ó más veces, con intervalos de 3 días entre una aplicación y la otra. Se emplean ácidos grasos como el ác. Undecilénico, Caprílico, Propiónico, etcétera, el Ácido acetil salicílico, (2-10 %), aunque su efectividad no es muy elevada en los animales.