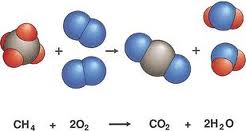
Ley de conservación de la materia
| ||||||
La ley de conservación de la materia, ley de conservación de la masa, o ley de Lomonósov-Lavoisier es una de las leyes fundamentales de las ciencias naturales.
Fue elaborada por Mijaíl Lomonósov (1711-1765) en 1748 y descubierta independientemente cuatro décadas después por Antoine Lavoisier (1743-1794) en 1785. Se puede enunciar de la siguiente manera:
«La masa de un sistema permanece invariable cualquiera que sea la transformación que ocurra dentro de él»; esto es, «en términos químicos, la masa de los cuerpos reaccionantes es igual a la masa de los productos en reacción».
Así fue enunciada en el año 1748 por Mijaíl Lomonosov (36). En 1785, y de manera independiente, el químico Antoine Lavoisier (42) propone que «la materia no se crea ni se destruye: solo se transforma». Es por esto que muchas veces la ley de conservación de la materia es conocida como ley de Lavoisier-Lomonosov.
Establece un punto muy importante: «En toda reacción química la masa se conserva, es decir, la masa total de los reactivos es igual a la masa total de los productos».
Generalidades
La combustión, uno de los grandes problemas de la química del siglo XVIII, despertó el interés de Lavoisier porque este trabajaba en un ensayo sobre la mejora de las técnicas del alumbrado público de París.
Comprobó que al calentar metales como el estaño y el plomo en recipientes cerrados con una cantidad limitada de aire, estos se recubrían con una capa de calcinado hasta un momento determinado en que esta no avanzaba más.
Si se pesaba el conjunto [metal, calcinado, aire, etc.) después del calentamiento, el resultado era igual al peso antes de comenzar el proceso. Si el metal había ganado peso al calcinarse, era evidente que algo del recipiente debía haber perdido la misma cantidad de masa.
Ese algo era el aire. Por tanto, Lavoisier demostró que la calcinación de un metal no era el resultado de la pérdida del misterioso flogisto, sino la ganancia de algo muy material: una parte de aire.
La experiencia anterior y otras más realizadas por Lavoisier; pusieron de manifiesto que si tenemos en cuenta todas las sustancias que forman parte en una reacción química y todos los productos formados, nunca varía la masa. Esta es la ley de la conservación de la materia.
Características
La ley se puede enunciar como «En una reacción química ordinaria la masa permanece constante, es decir, la masa consumida de los reactivos es igual a la masa obtenida de los productos».
Una salvedad que hay que tener en cuenta es la existencia de las reacciones nucleares, en las que la masa sí se modifica de forma sutil, en estos casos en la suma de masas hay que tener en cuenta la equivalencia entre masa y energía.
Esta ley es fundamental para una adecuada comprensión de la química. Está detrás de la descripción habitual de las reacciones químicas mediante la ecuación química, y de los métodos gravimétricos de la química analítica.
Estos científicos se referían a la materia másica. Más adelante se observó que en algunas reacciones nucleares existe una pequeña variación de masa. Sin embargo, esta variación se explica con la teoría de la relatividad de Albert Einstein, que propone una equivalencia entre masa y energía. De esta manera, la variación de masa en algunas reacciones nucleares estaría complementada por una variación de energía, en el sentido contrario, de manera que si se observa una disminución de la masa, es que ésta se transformó en energía, y si la masa aumenta, es que la energía se transformó en masa.
Teniendo es cuenta la ley de conservación de la materia, cuando escribimos una ecuación química, debemos ajustarla de manera que cumpla con esta ley. El número de átomos en los reactivos debe ser igual al número de átomos en los productos. El ajuste de la ecuación se logra colocando índices estequiométricos delante de cada molécula. El índice estequiométrico es un número multiplica a los átomos de la sustancia delante de la cual está colocado.
Fuentes
- La Química: un universo a su alcance (multimedia).
- Babor, Joseph A.; e Ibarz, José (1978): Química general moderna (tomo I). La Habana: Editora Científico-Técnica, 1978.