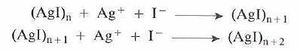Precipitado
| ||||||
Un precipitado es el sólido que se produce en una disolución por efecto de cristalización o de una reacción química. Dicha reacción puede ocurrir cuando una sustancia insoluble se forma en la disolución debido a una reacción química o a que la disolución ha sido sobresaturada por algún compuesto, esto es, que no acepta más soluto y que al no poder ser disuelto, dicho soluto forma el precipitado.
Sumario
Formación
En la mayoría de los casos, el precipitado (el sólido formado) cae al fondo de la disolución, aunque esto depende de la densidad del precipitado: si el precipitado es más denso que el resto de la disolución, cae. Si es menos denso, flota, y si tiene una densidad similar, se queda en suspensión.
El efecto de la precipitación es muy útil en muchas aplicaciones, tanto industriales como científicas, en las que una reacción química produce sólidos que después puedan ser recogidos por diversos métodos, como la filtración, la decantación o por un proceso de centrifugado.
Solubilidad
Definir a la solubilidad como la cantidad de una sustancia que se disuelve en una cantidad de solvente a una temperatura específica, da pauta a una identificación de los compuestos que servirán para formar una solución saturada. Y así distinguirlos de un precipitado, el cual se define como una sustancia insoluble que se forma en una solución y se separa de ella.
Los precipitados, tienen cierto tratamiento para ser separados, procedimiento que inicia con la digestión, en este proceso se ponen en contacto los precipitados con sus aguas madres. La digestión de la mayor parte de los precipitados a lugar a su purificación, por quedar las impurezas en la solución durante el proceso de recristalización. De esta forma, después de la digestión, debe procederse al filtrado de un precipitado, el cual comprende tres fases:
a)Decantación: Consiste en pasar a través del filtro tanto líquido sea posible, manteniendo el sólido precipitado prácticamente sin perturbar el vaso donde se formó.
Procediendo así, se acorta el tiempo total de filtración y se retrasa la obstrucción de los poros del medio filtrante con el precipitado.
b) Lavado: Proceso en el cual se añade una cantidad pequeña del líquido de lavado adecuado al precipitado, la mayor parte del cual debe quedar en el vaso después de que el líquido en que se formó se ha vertido sobre el filtro. El líquido de lavado debe cumplir con los siguientes requisitos.
1-. EL disolvente debe tener un coeficiente de temperatura amplio respecto a la solubilidad de la sustancia .
2-. Las impurezas deben ser o insolubles en caliente o solubles en frío
3-. La volatilidad del disolvente debe ser moderada.
4-. El disolvente debe ser químicamente inerte respecto a la sustancia.
Desde el punto de vista práctico el éxito de las separaciones por precipitación depende en gran manera de la última etapa de las fases que, generalmente, se realiza por algún procedimiento de filtración.
c)Transvase: El grueso de precipitado se pasa del vaso al filtro mediante adecuadas corrientes del líquido de lavado convenientemente dirigidas.
En ésta última etapa, el agua será combinada con alcohol para desechar el exceso de líquido. Sin embargo, la contaminación de los precipitados es un aspecto importante a considerar en los procesos de separación por precipitación, puesto que debido a las múltiples formas de manifestarse, es difícil tener un precipitado totalmente puro.
La contaminación según Kolthaff
- Coprecipitación: El precipitado fundamental y el contaminante se originan al mismo tiempo, pudiéndose distinguir entre dos tipos: por adsorción y por oclusión. Por adsorción consiste en un arrastre de impurezas en la superficie del precipitado, mientras que en la oclusión, el arrastre de las impurezas se realiza en el interior de las partículas primarias del precipitado.
- Posprecipitación: El precipitado fundamental estaba inicialmente puro, produciéndose la contaminación después que la precipitación ha terminado. Este fenómeno se favorece con el tiempo de agitación y con la elevación de la temperatura, pudiendo llegar a aun aumento del 100% en el peso del precipitado puro.
En la cristalización la fase sólida se forma por precipitación de la solución, al constituirse el cristal hay una gran tendencia a formar una red organizada de una sola sustancia, quedando las impurezas en la fase líquida.
Los mejores cristales se obtienen por enfriamiento lento de la solución. Mientras menor sea la temperatura final mayor será el rendimiento. El enfriamiento lento se logra, en general, dejando el matraz en reposo, simplemente, sin tocarlo. Cuando se tienen cristales de la sustancia, de otra procedencia, generalmente es posible iniciar la cristalización “sembrando”, es decir, añadiendo algunos cristalitos a la solución sobresaturada.
Tipos de precipitados
Precipitado coloidal
Está formado por partículas muy pequeñas, que no precipitan por efecto de la gravedad, por lo cual, la disolución tiene un aspecto turbio. Estas partículas no pueden separarse del disovente mediante el papel de filtro, ya que, debido a su pequeño tamaño, atraviesan la trama de éste. Este tipo de precipitado se forma si la sobresaturación es grande, puesto que la velocidad de nucleación también lo es, y se forman muchos núcleos que crecen poco.
Precipitado cristalino
Las partículas que forman el precipitado son grandes y la disolución queda transparente. Este precipitado se forma si la sobresaturación es pequeña, porque la velocidad también lo es, y se forman pocos núcleos que crecen mucho.
Mecanismo
La formación de un precipitado, a partir de sus iones en disolución, sigue un mecanismo constituido por dos etapas:
a)Nucleación Si disponemos de una disolución sobresaturada, se forman unas partículas diminutas, pero lo suficientemente grandes como para considerarse fase sólida, llamadas núcleos. Esto tiene lugar por la unión de un determinado número de iones de signo opuesto: Cuanto mayor es la sobresaturación, mayor es la velocidad...
Cuanto mayor es la sobresaturación, mayor es la velocidad de formación de núcleos.
b)Crecimiento del cristal
Una vez formados los núcleos, se sigue adicionando sobre ellos más iones, y estos núcleos crecen:
Enlace externos
Fuentes
- D. A. Skoog, "Fundamentos de Química Analítica", Reverte, Barcelona, 1988, pp. 981.
- R. L. Pecsok, "Métodos Modernos de Análisis Químicos", Limusa México, 1983 p. 32 a 34.
- R. A. Day, "Química analítica cuantitativa", Prentice-Hall, México, 1989, pp. 841.
- G. H. Ayres, "Análisis Químico Cuantitativo", Ed. Harla, México, 1978
- R. L. Pecsok, "Métodos Modernos de Análisis Químicos", Limusa México, 1983 p. 32 a 34