Suspenciones Celulares Embriogénicas (Biotecnología Vegetal)
| ||||||
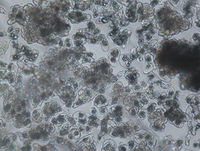
Suspensiones celulares embriogénicas: Consiste en un conjunto de células aisladas, así como de agregados celulares (de 2.0 a 100 células), distribuidos en un medio de cultivo líquido en constante movimiento.
Sumario
Sistema de Cultivo
Este sistema de cultivo es un poderoso implemento para llevar a cabo estudios sobre la inducción de la embriogénesis somática, crecimiento y diferenciación, organogénesis, ciclo celular, genética, nutrición, bioquímica y metabolismo, así como la obtención de diversos productos secundarios tales como algunos fenoles, antiquinonas, antocianina y nicotina entre otros.
Además las células en suspensión pueden ser empleadas en el mejoramiento genético, especialmente por la posibilidad que ofrece esta técnica de regenerar plantas a partir de las células mutadas y formar, por consiguiente, plantas mejoradas que pueden ser seleccionadas posteriormente por métodos tradicionales o mediante métodos biotecnológicos.
La formación de embriones somáticos en suspensiones celulares fue observada por primera vez en zanahoria (Daucus carota L.) y alfalfa (Medicago sativa L.), estas son las dos especies en las que se han realizado más estudios.
Las suspensiones celulares se han obtenido en múltiples especies vegetales, la regeneración de plantas a partir de ellas puede ser vía organogénesis y/o embriogénesis.
Establecimiento de suspensiones celulares
El establecimiento de un cultivo de células en suspensión puede lograrse directamente a partir de inóculos tales como: mesófilo de hojas o fragmentos de cotiledones, transfiriendo porciones de callos al medio de cultivo líquido y embriones inmaduros como en el plátano.
El primero de ellos tiene la desventaja de que las suspensiones no pueden ser mantenidas en cultivo por largos períodos de tiempo, siendo necesario prepararlas frescas para cada experimento.
El establecimiento de un cultivo de células en suspensión a partir de fragmentos de callos depende de la calidad del tejido calloso. Al combinar la calidad del callo y la velocidad de agitación las células se separan unas de otras con relativa facilidad.
La utilización de callos como material vegetal inicial para el establecimiento de suspensiones celulares embriogénicas ha impedido la exitosa explotación de esta tecnología (embriogénesis somática). Por ello, se ha comenzado a implementar una nueva técnica en la que se utiliza directamente el medio de cultivo líquido per se y la adición de cantidades de auxina o mezclas de ellas, lo que ha hecho posible la formación de masas proembriogénicas y la multiplicación de éstas. El tejido utilizado puede ser seleccionado a partir de hojas, tallos, secciones de hipocotilo, pétalos, meristemos apicales, ovarios y embriones cigóticos, tubérculos y filamentos de anteras. Esta técnica ha sido utilizada fundamentalmente en plantas aunque en especies monocotiledóneas como caña de azúcar y bananos se han empleado también.
Según Gómez (1998) el medio de cultivo más empleado en el mundo para el crecimiento y desarrollo de las células en suspensión es el propuesto por Murashige y Skoog (1962) (se continuará refiriendo como MS) el cual se utiliza en cultivos como la caña de azúcar, cafeto, bananos, plátanos, papa etc. También el medio de cultivo propuesto por Gamborg et al. (1968) (B5) se reconoce por su aplicación en el cultivo in Vitro de especies de importancia agrícola.
Mantenimiento de la suspensión celular
Una vez establecida la suspensión celular es indispensable determinar cuál es el momento donde las células han agotado los componentes del medio de cultivo, o al menos algunos de ellos.
Debido a su crecimiento y metabolismo, se hace necesario en este momento adicionar medio de cultivo fresco para continuar sus procesos fisiológicos normales. A esto se le denomina subcultivo. El momento en que debe de realizarse el subcultivo se determina a través de la curva de crecimiento de la suspensión, donde la células muestran una dinámica de crecimiento o división similar a la de los microorganismos y vive independiente del tejido que le dio origen (Gómez, 1998).
Fases de crecimiento
Las fases de crecimiento son:
- Fase inicial o de latencia: el inóculo no presenta ninguna señal de división celular, ya que únicamente se está adaptando a las nuevas condiciones nutricionales para posteriormente iniciar e incrementar la velocidad de división celular.
- Fase exponencial: a medida que el crecimiento continúa, las células alcanzan su máxima división; las células son jóvenes y biológicamente activas
- Fase lineal.
- Fase estacionaria: el alto número de células determina que se vayan agotando los nutrientes del medio de cultivo, las materias residuales tóxicas se acumulan, el pH se modifica, la transferencia de energía disminuye y las células se obstaculizan mutuamente, la velocidad de división va disminuyendo gradualmente hasta dar inicio a la fase estacionaria, momento en que se han agotado los nutrientes, o al menos algunos de ellos.
Procesos de formación
Formación de agregados embriogénicos
La formación de agregados embriogénicos es influenciada por factores como la densidad celular, la disposición de nutrientes y los reguladores del crecimiento que se le adicionan al medio de cultivo.
Frecuentes transferencias de medio de cultivo ocasionan una activa división celular, lo cual puede resultar en un incremento de la formación de agregados celulares embriogénicos. El incremento de la formación de agregados celulares durante el período de máxima división celular se debe al alto índice de mitosis en los agregados celulares y la menor división de las células aisladas.
El patrón de crecimiento de una suspensión celular depende de la densidad celular por mililitros de medio de cultivo a inocular. Con una densidad de inóculo baja, el crecimiento es muy lento o no ocurre. Por otra parte, si la densidad es muy alta la fase estacionaria se reduce, pero con esto el porcentaje de crecimiento cesa tempranamente, comienzan a morir rápidamente muchas células (Falco et al., 1996). La exacta relación entre densidad de inóculo y patrón de crecimiento varía entre las distintas especies.
Formación de embriones somáticos
Para inducir la formación del embrión somático a partir de los proembriones es necesario adicionar al medio de cultivo bajas concentraciones de auxina o auxinas menos fuertes e incluso no adicionar auxinas, especialmente cuando se trabaja con plantas monocotiledóneas. La densidad celular utilizada en una suspensión influye, además, en el comportamiento asincrónico de los embriones somáticos, siendo esto uno de los aspectos más importantes a resolver pues como se conoce, sólo los embriones que se encuentran en etapas más avanzadas del proceso de histodiferenciación, son capaces de germinar y dar lugar a plantas completas. De Jong et al. (1992) señalaron algunos aspectos que influyen en la asincronía, ellos son: *La cantidad de nutrientes que un embrión somático puede tomar del medio de cultivo
- La posible interacción entre los embriones y la concentración en que se encuentren los elementos de acondicionamiento liberados por los propios embriones somáticos al medio de cultivo.
Maduración de embriones somáticos
La etapa de maduración es un complejo período de desarrollo del embrión somático en el cual ocurre la expansión de la célula, la acumulación de sustancias de reserva y se adquieren tolerancia a la desecación.
La correcta acumulación de reservas conlleva a un incremento en la masa seca de los embriones somáticos lo que indica una alta calidad en el vigor e influye positivamente en su posterior germinación.
La adición de ABA durante la etapa de maduración del embrión promueve la acumulación de sustancias de reserva; esto, seguido de un apropiado tiempo de secado, puede lograr un mejor crecimiento y desarrollo del embrión somático.
Germinación y conversión en plantas de embriones somáticos
La germinación solo se refiere al desarrollo de la raíz y/o el brote.
Pocos análisis bioquímicos y fisiológicos han sido hechos para comparar los patrones de germinación de embriones cigóticos y somáticos. Las reservas de proteínas y lípidos en el embrión somático declinan sustancialmente a partir del primer día en condiciones de imbibición o bien antes de la elongación de la raíz.
La degradación tan rápida de las sustancias de reserva en el embrión somático es probablemente el resultado de la falta del tejido nutritivo que rodea a la semilla; es por esto que las plantas de embriones somáticos son más pequeñas y débiles que las de semilla.
También juegan un papel importante en la germinación la adición de citoquininas en el medio de cultivo, las cuales contrarrestan el efecto provocado por las auxinas durante la inducción y la proliferación.
Al proceso de desarrollo de plantas completas en condiciones ex vitro a partir de embriones somáticos se le denomina conversión y es esencial para los últimos eventos de un sistema basado en la embriogénesis somática. La conversión de los embriones somáticos difiere entre los genotipos, las especies y los sistemas de cultivo.
Aplicación
En el Laboratorio de Biotecnología vegetal del Instituto de Investigaciones de Viandas Tropicales (INIVIT) se logró el establecimiento de suspensiones celulares embriogénicas del cultivar de plátano ‘FHIA-25’, como parte de una metodología de regeneración de plantas a nivel celular como la embriogénesis somática que complementada a técnicas biotecnológicas de transformación genética, permitirá la mejora de la calidad del fruto ya que este cultivar cuenta con excelentes rendimientos y altamente resistentes a ‘Sigatoka negra’ pero con la limitante del bajo contenido de azúcar en su fruto. Las SCE se caracterizaron por la presencia de una alta proporción de agregados de células embriogénicas proliferantes cambio de color de amarillo brillante a pálido y la rápida sedimentación de células al ser retirada la suspensión del vibrador orbital, parámetros indicativos de una SCE de buena calidad.
Beneficios alcanzados
Los investigadores que trabajan el mejoramiento genético de plátano en Cuba dispondrán de suspensiones celulares embriogénicas como material inicial ideal para establecer un protocolo de transformación genética, garantizando elevados índices de supervivencia de las plantas transformadas.
Fuentes
- Dudits, D, Boger L y Gyorgyey J (1991) Molecular and cellular apporoches to the análisis of plant embryo development from somatic cells in vitro, J, Cell Sci. 9: 475-484
- Barranco LA (2001) Embriogénesis somática en banano (Musa AAAB, cv. FHIA-18) empleando medios de cultivo líquidos. Tesis para aspirar por el grado científico de Doctor en Ciencias Agrícolas. UCLV. IBP. Santa Clara
- Gómez, R (1998) Embriogénesis somática. En: Pérez Ponce, JN (Ed) Propagación y Mejora Genética de Plantas por Biotecnología. pp. 57-77. IBP, Santa Clara