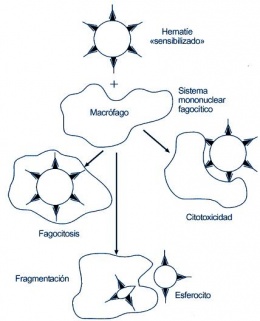
Anemia hemolítica autoinmune por anticuerpos calientes
Anemia hemolítica autoinmune por anticuerpos calientes. Es más frecuente en mujeres adultas que en otros grupos, en enfermedades inmunes (Lupus Eritematoso Sistémico) aunque suele ser idiopática. Los eritrocitos marcados por los autoanticuerpos (opsonización) son destruidos en el bazo por fagocitos y por activación del complemento (C3b y C4b), por lo que la hemólisis puede ser intravascular como extravascular. La enfermedad varía de pacientes asintomáticos a su forma más grave de hemólisis fulminante. La Prueba de Coombs Directa es Positiva en más del 98% de los casos.
Etiología
Se caracteriza porque los autoanticuerpos actúan a la temperatura del organismo (37 ºC), son de clase IgG y la hemólisis es predominantemente extravascular. Es el tipo de AHAI más frecuente. Puede ser idiopática o secundaria. La frecuencia de una y otra varía mucho según las series publicadas. Las enfermedades asociadas con mayor frecuencia son el Lupus Eritematoso Sistémico y otras enfermedades autoinmunes, la leucemia linfática crónica, linfomas y, excepcionalmente, el quiste de ovario entre otras menos comunes. Se presentan a cualquier edad (aunque son más frecuentes en los adultos) y predominan en el sexo femenino, sin que exista relación con el número de embarazos o de hijos.
Cuadro clínico
Es muy variado. El paciente se halla asintomático en algunas ocasiones. En otras, el comienzo puede ser insidioso, dado que la anemia se instaura lentamente. A veces se observa un ligero tinte ictérico. En los casos más graves la hemólisis es intensa, la anemia se instaura con rapidez y el enfermo presenta palidez de piel y mucosas, disnea, ansiedad e ictericia. Puede palparse esplenomegalia.
Diagnóstico
Se comprueban los signos generales de toda hemólisis. El examen morfológico de los hematíes revela anisocitosis,poiquilocitosis, policromasia y esferocitosis.
La haptoglobina está muy disminuida o es indetectable y en los hematíes del paciente se detecta una prueba de Coombs directa positiva con el suero antiglobulina humana poliespecífico. Si se emplean sueros antiglobulina humana monoespecíficos, los resultados son casi siempre positivos con el suero anti-IgG y, a veces, con el antisuero frente a la fracción C3 del complemento. Utilizando técnicas especiales (calor, disolventes orgánicos) es posible la separación (elución) del anticuerpo de los determinantes antigénicos del hematíe. En el suero del paciente se detecta también mediante la prueba de la antiglobulina indirecta un anticuerpo que, por regla general, reacciona con todos los hematíes del panel eritrocitario.
Es importante realizar la elución del anticuerpo y determinar su especificidad tanto en el eluido como en el suero, ya que ello permite la diferenciación entre un aloanticuerpo y un autoanticuerpo. Cuando la prueba de la antiglobulina directa e indirecta y el estudio del eluido y del suero dan resultados negativos se pueden utilizar técnicas más sensibles, como la de la antiglobulina ligada a una enzima o a una sustancia radiactiva, que detectan cantidades muy pequeñas de inmunoglobulinas fijadas al hematíe. También es útil conocer si la inmunoglobulina es de clase IgA o IgM, aun cuando estos tipos de AHAI son muy poco frecuentes. Algunos casos de AHAI se acompañan de trombocitopenia, que puede ser de origen inmune, en cuyo caso constituye el síndrome de Evans.
Pronóstico y tratamiento
El pronóstico de las AHAI por anticuerpos calientes secundarias se relaciona con la respuesta al tratamiento de la enfermedad de base. En las formas idiopáticas el pronóstico es muy variado. Aunque los pacientes tengan una buena respuesta al tratamiento se deben controlar de forma periódica, ya que es una enfermedad que evoluciona en brotes.
El tratamiento habitual en los pacientes con signos clínicos de hemólisis consiste en prednisona por vía oral, en dosis de 1-2 mg/kg y día. Suelen observarse mejorías notables en la primera semana. La falta de respuesta a la tercera semana sugiere que el tratamiento es ineficaz. Cuando se alcanzan cifras normales de hemoglobina se desciende paulatinamente la prednisona hasta hallar la dosis de mantenimiento, efectuando controles periódicos de hematócrito y reticulocitos.
La prueba de la antiglobulina directa e indirecta se efectúa como control a los 15 días del primer examen, repitiéndose después de manera periódica. Si se considera que ha habido una mala respuesta a los glucocorticoides o la dosis de mantenimiento de prednisona es superior a 15-20 mg/día deben plantearse otros tratamientos. La esplenectomía está indicada si los estudios con 51Cr demuestran que hay un índice elevado de captación esplénica. Se ha de tener en cuenta que en los pacientes en los que la sensibilización eritrocitaria es más importante por el componente C3b del complemento que por la misma IgG, el secuestro es más intenso en el hígado que en el bazo. También se pueden emplear fármacos inmunodepresores, como la azatioprina (2,5 mg/kg y día) o la ciclofosfamida (50-150 mg/día).
Los resultados son muy variables. Incluso se han intentado otras terapéuticas, como plasmaféresis, administración de plaquetas cargadas con vinblastina o inmunoadsorción de la IgG del plasma, pero los resultados son mucho más dudosos. En lo posible se deben evitar las transfusiones, aunque una incompatibilidad serológica no puede retrasar una transfusión si está clínicamente bien indicada. El mayor peligro de las transfusiones consiste en que el paciente esté sensibilizado a otros aloanticuerpos. Algunos autores también recomiendan efectuar transfusiones fraccionadas a los pacientes para evitar la sobrecarga de volumen.
Fuentes
• Ciril Ferreras Rozman, Medicina Interna, Ediciones Harcourt, 14 Edición, 2000.
• Delamore IW, ed. Multiple Myeloma and other Paraproteinaemias. Edimburgo, Churchill Livingstone, 1986. • Falk RH, Comenzo RL, Skinner M. The systemic amyloidoses. N Engl J Med 1997; 337:898-909.
• Freireich EJ, Kantarjian HM. Medical management of hematological malignant diseases. Marcel Dekker Inc., 1998.
• Harris N, Jaffe ES, Stein K, Banks PM, Chan JKC, Cleary M et al. A revised European-American classification of lymphoid neoplasms: A proposal from the International Lymphoma Study Group. Blood 1994; 84:1361-1392.
• Heim S, Mitelman F. Cancer cytogenetics. Nueva York, Alan R. Liss, 1995.