Arenavirus
| ||||||||||||
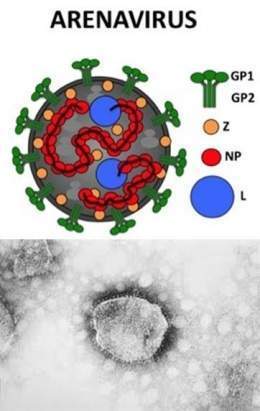
Los arenavirus son una familia de virus envueltos, pleomórficos que miden entre 60 y 300 nm, el tamaño promedio es alrededor de 92 nm, contienen un genoma ARN de una sola cadena segmentado, de sentido negativo o de ambos sentidos, rodeado por una envoltura con prolongaciones denominadas peplómeros en forma de raqueta. Dentro de la partícula viral pueden encontrarse de 2 a 10 partículas idénticas a los ribosomas, de alrededor de 20 nm que le dan aspecto arenoso en el microscopio electrónico y de donde se deriva su nombre.
Sumario
Introducción
Los virus pertenecientes a esta familia, son causantes de infecciones crónicas en roedores de Europa, África, América y posiblemente en otros continentes. Los animales infectados asintomáticamente invaden los habitats humanos, pudiendo afectar al hombre por contacto con los virus excretados por dichos animales. El mecanismo por el cual estos virus producen infección crónica en roedores y humanos puede ser complejo.
El primer arenavirus aislado fue el virus de la coriomeningitis linfocítica (CML) descubierto en el año 1933, por Lillie y Amstromg, durante el estudio de muestras provenientes de una epidemia de encefalitis de San Luís, el virus de la coriomeningitis linfocítica fue la causa de meningitis asépticas en estos pacientes. Más de 20 años transcurrieron para que fueran identificados otros arenavirus: el virus Junin aislado de pacientes con fiebre hemorrágica Argentina (FHA), en 1957, la fiebre hemorrágica boliviana (FHB, Machupo), en 1964 y la fiebre hemorrágica Venezolana (FHV, Guanarito). El virus Lassa aislado en el continente africano en 1969, constituye el único arenavirus patógeno para el hombre en ese continente. Los arenavirus poseen una composición simple de proteínas estructurales. Proteína no glicosilada (NP) de 63 a 72kDa, nucleoproteína unida al ARN viral. Glicoproteínas G1y G2 de 65 y 38 kDa respectivamente cuya función está asociada a la formación de la membrana del virión. Ambas contienen antígenos responsables de la inducción de anticuerpos neutralizantes. El ARN genómico consiste de 4 especies. Segmentos S (22 S) y L (31S).El segmento S codifica para la nucleoproteína (NP) y el precursor de la glicoproteína GP-C. Segmento L contiene el gen de la proteína L (polimerasa ARNp ARNd) y la proteína Z. Segmento 28 S ribosomal. Segmento 18 S ribosomal. Modificaciones postraduccionales del precursor de la glicoproteína (GP-C) conducen a la formación de las proteínas estructurales (GP1y GP2). La GP1 contiene determinantes que actúan con los receptores virales y la GP2 contiene sitios involucrados en la fusión de la membrana para la penetración del virus a la célula. Los arenavirus son inactivados por solventes orgánicos (cloroformo, éter, deoxicolato de sodio), igualmente se inactivan a pH ácido (< 5), luz ultravioleta y desinfectantes comunes como el hipoclorito, compuestos de amonio, la inactivación se puede obtener por tratamiento con b propiolactona. La infectividad viral es estable en muestras de suero mantenidas a temperatura ambiente por varias horas y declina lentamente a los pocos días. Son fácilmente inactivados por calentamiento a 56 °C por 30 min.
Replicación
La característica distintiva de los virus ARN de cadena negativa es que su genoma no sirve, directamente, como molde para la traducción de proteínas virales, esto ha sido comprobado, ya que los ARN genómicos purificados de los cuales las proteínas virales han sido eliminadas no tienen actividad en cuanto a sistemas de traducción invitro. Los virus de ARN de cadena negativa han trazado sus propias estrategias para poder traducir su información genómica, copian los ARN genómicos virales en moléculas complementarias lo que requiere una ARNpARNd que solo es codificada por el ARN viral genómico, por lo que estos virus cuando forman sus viriones empaquetan estas replicasas junto a su genoma.
El rango más distintivo de la replicación de arenavirus es la capacidad de producir altos títulos de progenie viral con una perturbación mínina de los procesos célula-hospedero, el ciclo de replicación es lento en comparación con otros virus de cadena negativa, requiriendo de 2 a 3 días para producir niveles máximos de virus. En general, los arenavirus se replican sin un disturbio significativo en la síntesis de macromoléculas célula hospedero y sin producir un efecto citopático, aunque este último se ha reportado en algunas células infectadas. El rango lento con el cual los arenavirus se replican y su incapacidad para redirigir una porción de la síntesis macromolecular de la célula hospedera hacia la producción de proteínas virales y ácidos nucleicos ha impedido dilucidar algunos detalles moleculares de su reproducción.
Analógicamente, con otros virus ARN envueltos, los procesos de unión a la superficie de la célula hospedera ocurren, probablemente, por una interacción entre una de las glicoproteínas virales de la envoltura y una protuberancia receptora de la membrana celular. La entrada del complejo de ribonucleoproteínas (RNP) dentro del citoplasma puede ocurrir por cualquiera de los siguientes mecanismos involucrando un evento de fusión con la membrana. Seguido a la unión, una de las glicoproteínas virales puede mediar la fusión de la envoltura viral con la membrana plasmática facilitando la deposición de la ribonucleoproteína (RNP) dentro del citoplasma de la célula hospedera. La célula hospedera puede internalizar el virión por fagocitosis durante la cual en el punto mediado por la fusión virus célula, la RNP es depositada dentro del citoplasma. Una vez dentro de la célula la transcriptasa específica viral (ARNpARNd) presumiblemente inicia la síntesis de ARN a partir de moldes genómicos de ARN. La estrategia codificadora doble sentido realizada a partir de análisis de secuencia de ARN genómico L y S de arenavirus facilita penetrar dentro del orden secuencial de transcripción de genes y eventos de replicación de ARN.
Análisis del virus
Los arenavirus frecuentemente se cuantifican por el método de placas en células Vero. La formación de placas puede requerir períodos largos de incubación (hasta 7 días) para los miembros del grupo Tacaribe. De manera general, las placas varían en talla y tiempo de aparición. En monocapas de células no se observa un efecto citopático típico, se caracteriza por un redondeamiento de las células y en casos excepcionales, se observa una total exfoliación del cultivo. Todos los arenavirus son mantenidos en la naturaleza por infección persistente de un grupo de especies de roedores. Aunque estos hospederos infectados crónicamente pueden no mostrar síntomas, contienen altos títulos de virus y excretan libremente virus infeccioso en sus orinas. Dado que pueden observarse títulos de hasta 105ufp/mL en orina, estas características deben tomarse en cuenta en el manejo de los roedores del laboratorio.
Patogenia y patología
La patogénesis de la enfermedad por arenavirus parece inducir una replicación inicial en el sitio de infección, el modo más común de infección no está bien dilucidado, aunque se piensa sea a través de la piel (cortaduras o abraciones por contacto con los fluidos contaminados) seguido del inicio de la infección, todos los arenavirus progresan a infecciones en múltiples órganos, especialmente, del sistema reticuloendotelial.
Los linfonodoshiliares son un sitio importante del crecimiento del virus, así como los pulmones y otros órganos parenquimatosos. Independientemente de la ruta de infección, los macrófagos son identificados como una célula temprana y prominentemente involucrada. Cuando la infección se disemina, otros tipos adicionales de células alcanzan igual prominencia. Se han identificado muchas estructuras epiteliales que contienen antígenos y ácidos nucleicos. Teniendo en cuenta la extensión a diferentes células del cuerpo los cambios patológicos son relativamente sutiles comparada con una franca necrosis pequeña. La repuesta inmune a arenavirus puede ser protectora, deletoria o ambas. La respuesta celular (hipersensibilidad retardada o DTH y linfocitos T citotóxicos) es medida fácilmente y se cree sean los mecanismos más importantes en la recuperación e inmunopatología.
Los anticuerpos aunque menos prominentemente involucrados son importantes igualmente en la protección. El balance relativo entre la protección y la patología, así como entre la respuesta celular y humoral está determinado por la cepa viral y el huésped.
Datos clínicos
La enfermedad por arenavirus tiene un patrón básico que comienza con fiebre y mialgia, seguido de anormalidades sistémicas y de las células hematopoyéticas. En las fiebres hemorrágicas virales, un período de viremia que dura de 1a 3 semanas está acompañado de un intenso impacto sistémico. Al menos seis arenavirus son causa de enfermedad en humanos virus Lassa, Junin, Machupo, Guanarito, Sabia y de la coriomeningitis linfocítica.
Tratamiento
Aunque muchos compuestos han mostrado eficacia invitro, solamente la guanosina análogo del ribavirin ha tenido aplicación práctica, no obstante el mecanismo de acción es desconocido. Todos los arenavirus probados han sido inhibidos en cultivo de células utilizando concentraciones similares de ribavirin. La ribavirina ha sido utilizada principalmente en la fiebre Lassa con un mal pronóstico, también se han obtenido buenos resultados en el tratamiento de FHA y los resultados preliminares en machupo y sabia son promisorios. Esta droga ha sido considerada para la profilaxis de personas expuestas a fiebres hemorrágicas arenovirales, la dosis no tóxica suele ser de 1,2 g/día vía oral.
Enlaces relacionados
Fuentes
- Libro: Microbiología y Parasitología Médicas Tomo I por Llop, Valdés-Dapena, Zuazo