Diferencia entre revisiones de «Exergía»
(Etiqueta: nuestro-nuestra) |
(Etiqueta: nuestro-nuestra) |
||
| Línea 1: | Línea 1: | ||
{{Definición | {{Definición | ||
| − | |nombre= | + | |nombre=Exergía |
| − | |imagen= | + | |imagen=Entalpia-300x225.jpg |
|tamaño= | |tamaño= | ||
| − | |concepto= | + | |concepto=La exergía es una medida de la disponibilidad de la energía. |
}} | }} | ||
La '''exergía''', término introducido por Rant en 1956, es la porción de energía que puede ser transformada en trabajo mecánico, la parte restante, sin utilidad práctica, recibe el nombre de anergía. | La '''exergía''', término introducido por Rant en 1956, es la porción de energía que puede ser transformada en trabajo mecánico, la parte restante, sin utilidad práctica, recibe el nombre de anergía. | ||
Revisión del 12:53 10 feb 2014
| ||||||
La exergía, término introducido por Rant en 1956, es la porción de energía que puede ser transformada en trabajo mecánico, la parte restante, sin utilidad práctica, recibe el nombre de anergía. La exergía es un parámetro que mide la calidad de la energía. Este parámetro puede emplearse para analizar la eficiencia energética de los procesos industriales. Con un análisis de exergía pueden compararse diferentes alternativas para comprobar cuál tiene el mayor rendimiento energético. Sin embargo, no proporciona soluciones por sí misma.
La idea es que parte de la energía de un sistema se puede aprovechar para realizar trabajo mecánico, eléctrico o de otro tipo. El segundo principio de la termodinámica nos establece limitaciones en cuanto a la cantidad de trabajo que podemos realizar. Pero existe además una limitación práctica en cuanto a que sólo se puede realizar trabajo si el sistema almacena una energía respecto al ambiente que le rodea.
La exergía determina de forma cuantitativa el valor termodinámico de cualquier recurso, y permite analizar rigurosamente el desperdicio de los recursos en las actividades de la sociedad, estableciendo pautas para su ahorro y uso eficiente.
El propósito principal de un análisis de exergía es descubrir las causas del bajo rendimiento de un proceso, y cuantificar estas causas. En ocasiones puede ayudar a tomar decisiones de diseño o modificación de un proceso.
Por ejemplo, un compuesto de combustible y aire, si se quema el combustible obteniendo una mezcla de aire y productos de combustión ligeramente calientes, aunque la energía asociada al sistema sea la misma, la exergía del sistema inicial es mucho mayor, ya que potencialmente es mucho más útil a la hora de obtener trabajo, de donde se deduce que la exergia al contrario que la energía no se conserva sino que se pierde por la evolución hacia el estado de equilibrio. Otro ejemplo es el agua de refrigeración de las centrales térmicas. Aunque la central cede una gran cantidad de energía al agua, esta solo eleva su temperatura unos grados por encima de la temperatura de su entorno, por tanto su utilidad potencial para obtener trabajo es prácticamente nula o lo que es lo mismo en términos técnicos, tiene una exergía asociada baja.
Sumario
Energía y Exergía
Los diferentes tipos de energía presentan también diferentes calidades. Estas diferencias radican en la posibilidad de producir trabajo o de transformar un tipo de energía en otro. Por ejemplo, la calidad del calor depende de su temperatura; a mayor temperatura, una fuente de calor puede transferir su energía con más posibilidades que a menor temperatura.
En general, se acepta como medida de la calidad de la energía, su capacidad para producir trabajo. El problema con esta definición es elegir el nivel de referencia adecuado. Hay que tener en cuenta, que para que una máquina térmica realice trabajo, debe tomar calor desde una fuente a alta temperatura, y ceder parte de ese calor a un sumidero a baja temperatura. Si la temperatura (fría) del sumidero es muy alta, muy pocas fuentes tendrán la temperatura necesaria como para que una máquina térmica puede transformar el calor de esta fuente en trabajo. Por tanto el nivel de referencia (es decir, el valor de la temperatura fría) es muy importante a la hora de definir la exergía. Como es habitual que las máquinas térmicas trabajen con el medio que las rodea como foco frío, se suele tomar el nivel de referencia en la temperatura ambiente.
Por tanto, a la hora de calcular la exergía es necesario especificar cuál es el entorno en el que trabaja la máquina térmica. Debido a la falta de un equilibrio termodinámico en la naturaleza6.3, no se puede especificar completamente cuál es el estado de referencia (debido a que, como ya se ha dicho, las condiciones del medio son cambiantes). Normalmente, es suficiente con definir el estado de equilibrio mediante la temperatura.
La capacidad de un medio energético para realizar trabajo expresa su potencial para transformarse en otros tipos de energía, y por tanto la exergía puede aplicarse al estudio de procesos tecnológicos6.4 además de para plantas de energía, ciclos termodinámicos, máquinas, etc.
A diferencia de la energía, no existe una ley de conservación para la exergía. Cualquier fenómeno irreversible causa una pérdida de exergía, lo que conlleva una reducción del potencial de los efectos útiles de la energía, o por el contrario a un aumento del consumo de energía proporcionado por el foco caliente (para lograr una generación de trabajo igual).
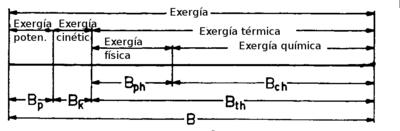
Si excluimos los efectos nucleares, magnéticos y eléctricos, la exergía, B , de una sustancia se puede dividir en cuatro componentes: exergía cinética Bk , exergía potencial Bp, exergía física Bf y exergía química Bq. La exergía cinética es igual a la energía cinética cuando la velocidad tiene como nivel de referencia la superficie de la Tierra. Lo mismo ocurre con la exergía potencial. En la figura se muestran los diferentes tipos de exergía.
B = Bk + Bp + Bf + Bq
La exergía física es el trabajo que se puede obtener sometiendo a la sustancia a procesos físicos reversibles desde la temperatura y presión iniciales, hasta el estado determinado por la presión y la temperatura del entorno.
La exergía química es el trabajo que se puede obtener de una sustancia que se encuentra a la presión y temperatura del entorno, si alcanza un estado de equilibrio termodinámico mediante reacciones químicas.
En ocasiones, a la suma de la exergías física y química se le denomina exergía térmica, Bt.
Bt = Bf + Bp
Estado muerto
Dos sistemas en condiciones termodinámicas diferentes, que entren en contacto, evolucionarán espontáneamente, por medio de transferencias de masa y energía, hacia un estado intermedio de equilibrio (el que tenga mínima exergía y entropía máxima). A este estado de equilibrio se le denomina estado muerto. Cuanto mayor sean las diferencias entre sus magnitudes termodinámicas (presión, temperatura...) más trabajo podremos obtener de la interacción entre sistema y entorno.
La energía utilizable o exergía está asociada al desequilibrio entre un sistema y su entorno, es decir que depende de la variable de dos sistemas como mínimo.
Un ejemplo de ello para entender lo anterior es: supóngase una lámina metálica que se encuentra a 80ºC, y es sumergida en agua a 4ºC, es decir relativamente mucho más fría, en este caso la reacción, manifestación y el nivel de exergía será mayor que si la lámina hubiese sido sumergida en agua que se encuentra a 80ºC, es decir que la temperatura del sistema (lámina metálica) y de su entorno (agua) es la misma (80ºC), en este caso no pasaría nada y este estado se denomina estado muerto ya que tenemos cero exergía y máxima entropía. Esto también es aplicable a otros desequilibrios como pueden ser de presión y otros.
Desde el punto de vista de la obtención del trabajo máximo que podemos obtener de un sistema termodinámico, uno de los sistemas se considera el universo, y otro nuestro dispositivo. El estado muerto sería el estado del universo, nuestro sistema nos puede proporcionar trabajo, como máximo, la diferencia de energía entre el estado del universo y su estado inicial. Este trabajo máximo es la exergía de nuestro sistema. En general, como el universo es muy grande respecto a nuestro sistema se aplican las siguientes simplificaciones, el estado muerto no varía con la cesión de energía de nuestro sistema y como universo se toma el medio ambiente que rodea a nuestro sistema, por ejemplo, la temperatura y la presión atmosférica del lugar en el que se encuentra nuestro sistema (densidad y temperatura del aire que rodea el motor de un coche...). Resumiendo, el estado muerto marca el estado del que nos es imposible extraer trabajo de un sistema y este depende del medio ambiente que le rodea.
Balances
En realidad un balance de exergía no es más que la combinación de un balance de energía y de entropía, que derivan a su vez del primer y segundo principio de la termodinámica. No es por tanto un resultado independiente, pero puede utilizarse como formulación alternativa de la segunda ley de la termodinámica.
Como alternativa al principio de incremento de entropía, se puede formular la segunda ley estableciendo que, los únicos procesos que puede experimentar un sistema aislado son aquellos en los que la exergía del sistema disminuye.
El balance de exergía es un método de análisis muy útil a la hora de valorar el rendimiento energético de una instalación, nos da una visión más amplia que el rendimiento térmico. Permite valorar las pérdidas de energía en un proceso, la energía que sería aprovechable de flujos salientes en sistemas abiertos y las ventajas de métodos regenerativos en instalaciones térmicas. Para todo esto la principal herramienta son los diagramas de Sankey
Además de los anteriores, existen otros tipos de desgaste comunmente encontrados en la literatura especializada como; Desgaste por impacto, por cavitación, difusivo y desgaste corrosivo.
Aplicaciones
Una de las princpales aplicaciones es el análisis exergético a nivel de proceso y componente. Éste permite identificar, localizar y cuantificar las principales causas de irreversibilidades termodinámicas de un sistema o proceso, mediante el estudio de la destrucción y eficiencia exergéticas. Siendo la exergía la parte disponible de la energía utilizada para producir trabajo útil, esta representa una poderosa herramienta para determinar potenciales mejorías y optimización de procesos, así como impactos ambientales y su mitigación (al ser una medida del desequilibrio con el medio ambiente). La termoeconomía, una área que combina el análisis exergético con el análisis económico es una disciplina recientemente adoptada para determinar los costos exergéticos que se derivan de la producción de diferentes productos en plantas de cogeneración, trigeneración y poligeneración.
Véase también
- Reología
- Abrasión
- tribómetro — equipo usado para medir el desgaste
Referencias
