Hidróxidos no metálicos
| ||||||
Hidróxidos no metálicos. Sustancias que se obtienen por la reacción del agua y un óxido no metálico. También son denominados ácidos oxigenados u oxoácidos.
Se obtienen por la combinación de un anhídrido (también llamado óxido ácido) con el agua.
Sumario
Fórmula
Óxido ácido + H2O ---------> (HXO)Hidróxido no metálico
H--representa al Hidrógeno
X--representa al no metal
O--representa al oxígeno
Ver Ejemplos
- SO3 (s) + H2O(l) = H2SO4 (ac)
- N2O5 (g) + H2O(l) = 2HNO3 (ac)
- P4O10 (s) + H2O(l) = 4 H3PO4 (ac)
Descripción
Los hidróxidos no metálicos son sustancias ternarias constituidas por oxígeno, hidrógeno y otro elemento no metálico.
Las disoluciones de los hidróxidos no metálicos tienen propiedades contrarias a las de los hidróxidos metálicos. Estas propiedades se conocen con el nombre de propiedades ácidas por lo que se leen con la palabra ácido y el nombre del no-metal.
Por ejemplo:
- Ácido sulfúrico, H2SO4. (El conocido ácido de acumulador es una disolución de esta sustancia).
- Ácido nítrico, HNO3.
- Ácido fosfórico, H2PO4.
- Ácido bórico, H2BO3.
Propiedades
- Los hidróxidos no metálicos son, a temperatura ambiente, sustancias líquidas o sólidas de relativamente bajas temperaturas de fusión y de ebullición y en general sustancias solubles en agua.
- Son compuestos moleculares, es decir, son compuestos que no tienen iones, sin embargo tienen la propiedad de formar iones hidrógenos positivos e iones halogénicos negativos, en el momento de disolverse en agua.
- No conducen la corriente eléctrica, sin embargo, sus disoluciones acuosas si la conducen.
- Cuando se disuelven en agua, originan iones poliatómicos oxigenados negativos e iones hidronio, H+ (ac)
- Tienen sabor ácido
Nomenclatura y notación química
Nomenclatura química
Para nombrar estos compuestos se usa la palabra genérica ácido y a continuación el nombre del anión poliatómica oxigenado cambiando su terminación ito por oso y ato por ico.
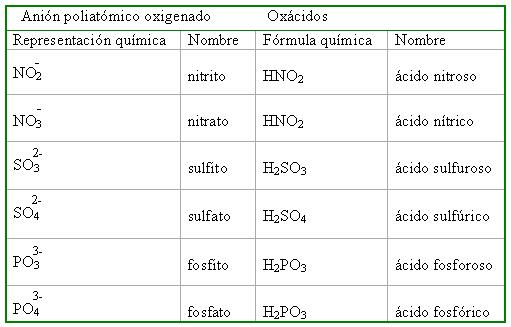
Notación química
Para escribir la fórmula química de un hidróxido no metálico se procede de la siguiente forma.
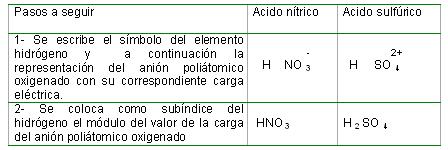
Aplicaciones
Los ácidos tienen gran aplicación en la industria.
- Se utilizan en la obtención de diversas sales, colorantes, medicamentos y otros productos de gran demanda.
- Los ácidos sulfúricos y clorhídricos son usados en soldaduras para eliminar las capas de óxidos que tienen algunos metales antes de recubrirlos con otros metales.
- Se utilizan además en la limpieza de objetos de metal, al tener la propiedad de reaccionar con los óxidos metálicos
- En la industria azucarera, se utilizan los ácidos, para limpiar las incrustaciones de carbonatos en las paredes de las calderas de vapor y en las tuberías.
- Otros ácidos se utilizan en la medicina, el ácido acetilsalicilico (La aspirina) como analgésico y anticoagulante.
Véase también.
Fuentes
- Libro de texto de Química. Parte 2. Secundaria Básica.


