Membrana basal
| ||||
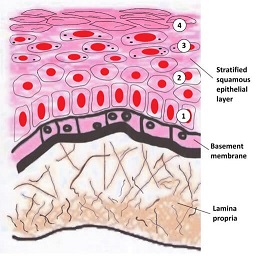
Membrana basal. Organizaciones especializadas como hojas de proteínas y de glucosaminoglucanos de la matriz extracelular que actúan como una interfase entre células parenquimales y tejido de soporte.
Sumario
Resumen
La membrana basal es una estructura extracelular que recubre los tejidos de casi todos los organismos pluricelulares. Está conformada principalmente por glucoproteínas colagénicas y no colagénicas. Esta estructura se encarga de separar el epitelio de un tejido del estroma de otro. Se encuentra generalmente en la región basolateral del tejido epitelial, en el endotelio, en la región periférica de los axones, en las células grasas y también en células musculares.
La membrana basal está constituida por grandes moléculas insolubles que se unen entre sí para formar una ultraestructura en forma de lámina a través de un proceso conocido como “autoensamblaje”. Este proceso es impulsado por el anclaje de diversos receptores propios de la superficie celular.
La mayoría de las células del cuerpo son capaces de producir el material necesario para la estructuración de la membrana basal dependiendo del tejido al que pertenezcan.
Enfermedades como el síndrome de Alport y el síndrome de Knobloch se asocian con mutaciones en los genes codificantes para las cadenas de colágeno de la membrana basal, por lo que el estudio de su estructura y propiedades se ha popularizado con el paso de los años.
La complejidad de la membrana basal no puede ser apreciada mediante microscopía electrónica, ya que dicha técnica no permite la distinción entre las diferentes membranas basales. Para su estudio, en cambio, son necesarias técnicas de caracterización más precisas como, por ejemplo, la microscopía de barrido.
Características
La membrana basal es una estructura densa y amorfa, similar a una hoja. Tiene de 50 a 100 nm de espesor, según lo determinado mediante microscopía electrónica de transmisión. El estudio de su estructura determina que esta posee características similares a la matriz celular, pero difiere en cuanto a su densidad y asociaciones celulares.
Dependiendo del órgano y tejido se observan diferencias en la composición y la estructura de la membrana basal, por lo que se piensa que existe un microentorno específico delimitado por la misma en cada tejido.
La especificidad de cada membrana basal puede deberse a la composición molecular y se cree que la variación bioquímica y molecular confiere una identidad única a cada tejido en cuestión.
Células epiteliales, endoteliales y muchas células mesenquimales producen membranas basales. Mucha de la plasticidad de estas células está conferida por esta estructura. Además, esta parece servir de soporte para las células que participan en el recubrimiento de los órganos.
Estructura
Una de las características más interesantes de la membrana basal es su capacidad de autoensamblaje a partir de los componentes que la conforman, estableciendo una estructura similar en forma a una lámina.
Varios tipos de colágeno, proteínas lamininas, proteoglicanos, proteínas de unión al calcio y otras proteínas estructurales son los componentes más comunes de las membranas basales. El perlecan y el nidogen/entactina son otras de las proteínas constituyentes de la membrana basal.
Entre las principales características arquitectónicas de las membranas basales se encuentra la presencia de dos redes independientes, una formada por colágeno y la otra por algunas isoformas de laminina.
La red de colágeno está altamente reticulada y es el componente que mantiene la estabilidad mecánica de la membrana basal. El colágeno de estas membranas es exclusivo de estas y se conoce como colágeno tipo IV.
Las redes de laminina no están unidas covalentemente y en algunas membranas llegan a ser más dinámicas que la red de colágeno IV.
Ambas redes están conectadas por las proteínas nidogen/entactina que son altamente flexibles y permiten unir, además de las dos redes, a otros componentes como las anclas de las proteínas receptoras de la superficie celular.
Ensamblaje
El autoensamblaje es estimulado por el acoplamiento entre el colágeno tipo IV y la laminina. Estas proteínas contienen en su secuencia la información necesaria para la unión primaria, lo que les permite iniciar el autoensamblaje intermolecular y formar una estructura basal en forma de lámina.
Las proteínas de la superficie celular como las integrinas (especialmente las integrinas β1) y los distroglicanos facilitan la deposición inicial de los polímeros de laminina gracias a interacciones sitio específicas.
Los polímeros de colágeno tipo IV se asocian con los polímeros de laminina en la superficie celular a través del puente nidogen/entactina. Este andamio luego proporciona sitios de interacción específicos para que otros constituyentes de la membrana basal interactúen y generen una membrana completamente funcional.
Se han identificado distintos tipos de unión nidogen/entactina en la membrana basal y todos promueven la formación de redes en la estructura.
Las proteínas nidogen/entactina, junto con las dos redes colágeno IV y laminina, estabilizan las redes y le otorgan rigidez a la estructura.
Funciones
La membrana basal siempre está en contacto con las células y sus funciones principales tienen que ver con proporcionar soporte estructural, dividir los tejidos en compartimentos y regular el comportamiento celular.
Las membranas basales continuas actúan como filtros moleculares selectivos entre los compartimientos de los tejidos, es decir, mantienen un control estricto del tránsito y movimiento de células y moléculas bioactivas en ambas direcciones.
A pesar de que las membranas basales actúan como puertas selectivas para impedir el libre tránsito de las células, parece que existen mecanismos específicos que permiten que las células inflamatorias y las células tumorales metastásicas atraviesen y degraden la barrera que supone la membrana basal.
En los últimos años se ha indagado mucho en la función que cumplen las membranas basales como reguladores en el crecimiento y la diferenciación celular, ya que la membrana basal posee receptores con la capacidad de unirse a citoquinas y factores de crecimiento.
Estos mismos receptores en la membrana basal pueden servir de reservorios para su liberación controlada durante los procesos de remodelación o reparación fisiológica.
Las membranas basales son componentes estructurales y funcionales importantes de todos los vasos sanguíneos y capilares, y tienen un papel crucial en la determinación de la progresión del cáncer, especialmente respecto a la metástasis o la migración celular.
Otra de las funciones que cumple esta estructura tienen que ver con la transducción de señales.
El músculo esquelético, por ejemplo, está rodeado por una membrana basal y posee pequeños parches característicos en los sitios de unión neuromuscular; estos parches son los responsables del envío de las señales desde el sistema nervioso.
Enfermedad por membrana basal delgada
La enfermedad por membrana basal delgada es un tipo de síndrome nefrítico. Es hereditaria y se transmite en forma autosómica dominante. No todas las mutaciones genéticas se han caracterizado, pero en algunas familias con este trastorno hay una mutación en el gen alfa-4 del colágeno de tipo IV. La prevalencia se estima entre el 5 y el 9%.
Signos y síntomas
La mayoría de los pacientes son asintomáticos, y se les detecta una hematuria microscópica por casualidad en un análisis de rutina, aunque en ocasiones se presentan proteinuria leve y hematuria grosera. Típicamente, la función renal es normal, pero unos pocos pacientes desarrollan insuficiencia renal progresiva por motivos desconocidos. Una manifestación infrecuente es el dolor recurrente en el flanco, similar al de la nefropatía por immunoglobulina A.
Diagnóstico
- Evaluación clínica
- A veces, biopsia renal
El diagnóstico se basa en los antecedentes familiares y el hallazgo de hematuria, sin otros síntomas o patología, en especial si los miembros asintomáticos de la familia presentan también hematuria. La biopsia renal no es necesaria, pero a menudo es realizada como parte de la evaluación de la hematuria. En las primeras etapas, esta enfermedad puede ser difícil de diferenciar de la nefritis hereditaria debido a sus similitudes histológicas. El análisis genético molecular puede ayudar a diferenciar estas 2 enfermedades.
Tratamiento
En la macrohematuria frecuente, el dolor en el flanco o la proteinuria, inhibidores de la enzima convertidora de angiotensina (ECA) o bloqueantes de los receptores de la angiotensina II (BRAII)
El pronóstico a largo plazo es excelente y en la mayoría de los casos no se requiere tratamiento. Los pacientes con hematuria grosera frecuente, dolor en el flanco o proteinuria (p. ej., relación proteinuria/creatinina > 0,2) pueden beneficiarse con la administración de inhibidores de la ECA o BRA, que pueden disminuir la presión intraglomerular.