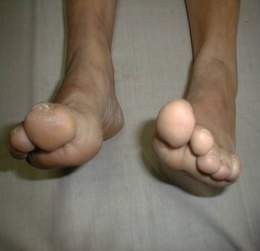
Neuropatía hereditaria
| ||||
Neuropatías hereditarias. Se clasifican en neuropatías sensitivo-motoras y neuropatías sensitivas. (Para las neuropatías hereditarias motoras, v. Trastornos de la neurona motora inferior y superior, más atrás).
La neuropatía hereditaria sensitivo-motora más frecuente es la enfermedad de Charcot-Marie-Tooth (v. más adelante). Otras menos comunes comienzan al nacimiento y dan lugar a una incapacidad grave. En las neuropatías sensitivas, que son infrecuentes, la pérdida de la sensibilidad distal al dolor y la temperatura es más importante que la alteración de la sensibilidad vibratoria y posicional. El principal problema es la amputación de los pies debido a la anestesia al dolor, con infecciones frecuentes, incluyendo osteomielitis.
Sumario
- 1 Características Tipo I y II
- 2 Interrogantes aún no resueltas por el genoma
- 3 Características Tipo III
- 4 Neurofibromatosis
- 5 Síntomas, signos y diagnóstico
- 6 Tratamiento
- 7 Síndrome de Proteus
- 8 Trastornos de la transmisión neuromuscular
- 9 Bloqueo de conducción nerviosa:
- 10 Enlaces Relacionados
- 11 Fuente
Características Tipo I y II
Es un trastorno relativamente frecuente, generalmente autosómico dominante, caracterizado por debilidad y atrofia muscular, fundamentalmente en los músculos peroneales y distales de las piernas. Los pacientes pueden presentar simultáneamente otros trastornos degenerativos (p. ej., ataxia de Friedreich) o antecedentes familiares de ellos. Los pacientes con neuropatía tipo I comienzan en la mitad de la infancia con pie caído y atrofia muscular distal lentamente progresiva, dando lugar a las «piernas en cigüeña». Posteriormente aparece atrofia de los músculos intrínsecos de las manos.
Además existe un déficit de la sensibilidad vibratoria y termoalgésica con un patrón de distribución «en guante y calcetín». Los reflejos tendinosos profundos están abolidos.
En los miembros de la familia portadores sin afectación clínica importante, los únicos signos pueden ser pies cavos o dedos en martillo en los pies. Las velocidades de conducción nerviosa son lentas y las latencias distales están prolongadas. Anatomopatológicamente existen desmielinización y remielinización segmentarias.
Los nervios periféricos engrosados a veces son palpables. El trastorno progresa lentamente y no afecta a la esperanza de vida. El tipo II sigue una evolución más lenta y la debilidad muscular suele aparecer en una época más tardía de la vida. Los pacientes presentan una velocidad de conducción relativamente normal, pero tienen una baja amplitud de los potenciales evocados. La biopsia del nervio muestra una degeneración walleriana.
Interrogantes aún no resueltas por el genoma
Privacidad y Justicia en el uso de la Interpretación de la Información Genética
Tiene que ver concretamente con cuestiones como: ¿De quién es la información genética? ¿Quién, cómo y para qué puede usarla? ¿Es posible patentar el genoma humano?13 ¿Hasta dónde llega la propiedad individual y la privacidad del paquete genético?14 Qué uso puede dársele a la información genética en el individuo en cuestiones de empleo, seguros, adopciones, paternidad, investigación criminal, etcétera.
Integración clínica de las nuevas tecnologías
Este aspecto, obviamente, tiene que ver más con la práctica clínica, y por eso apenas se enuncian las preguntas claves. ¿Es hora de iniciar las terapias génicas? ¿En enfermedades orgánicas y mentales? ¿A quiénes deben aplicarse? ¿Deben incluirse en los paquetes de atención? Cómo valorar los riesgos inevitables, evidenciados ya aún con la muerte reportada de algunos pacientes?
Implicaciones y retos del avance genético en la educación pública en salud, y en la formación profesional y técnica del sector
¿Qué debe saber la población general sobre genética y sus relaciones e implicaciones en la vida cotidiana? ¿Qué deben saber los médicos, las enfermeras, los odontólogos, los salubristas y las bacteriólogas sobre estos temas a un nivel más técnico y elaborado? ¿Qué estamos haciendo para introducir responsablemente estos temas, estas tecnologías y estas inquietudes en nuestros círculos académicos, profesionales y sociales?
Características Tipo III
Es un raro trastorno autosómico recesivo que comienza en la infancia con debilidad muscular progresiva, alteración de la sensibilidad y arreflexia. Inicialmente puede simular una enfermedad de Charcot-Marie-Tooth, pero la afectación motora progresa más rápidamente que en aquella. La biopsia de nervio muestra desmielinización y remielinización que dan lugar a un engrosamiento de los nervios periféricos «en bulbo de cebolla».
La distribución característica de la debilidad muscular, las deformidades del pie, los antecedentes familiares y las alteraciones electrofisiológicas confirman el diagnóstico. Es posible el estudio genético de la enfermedad, pero no existe un tratamiento específico. Puede ser útil el consejo profesional a los pacientes jóvenes para prepararlos ante la progresión de la enfermedad. Las medidas terapéuticas conservadoras consisten en refuerzos ortopédicos para corregir el pie caído y en ocasiones la cirugía para la estabilización ortopédica del pie.
Neurofibromatosis
Conjunto de trastornos hereditarios autosómicos dominantes designados como tipo 1 (neurofibromatosis periférica, enfermedad de von Recklinghausen) y el tipo 2, menos frecuente (neurofibromatosis central), caracterizado por neurinomas del acústico bilaterales.
El tipo 1 se transmite a través del cromosoma 17 y el tipo 2 con el cromosoma 22. En el tipo 1 existe una afectación o pérdida de las propiedades supresoras tumorales de la neurofibromina.
Síntomas, signos y diagnóstico
En la neurofibromatosis tipo 1, un tercio de los pacientes son asintomáticos y se identifican durante exploraciones de rutina, un tercio presenta alteraciones cutáneas y el otro tercio tiene alteraciones neurológicas.
Las lesiones cutáneas características consisten en máculas similares a pecas de color marrón claro (manchas café con leche) localizadas principalmente en el tronco, pelvis y cara flexora de los codos y rodillas; estas manchas son aparentes ya en el nacimiento o en la infancia en >90% de los pacientes. Los tumores cutáneos del color de la piel, de varias formas y tamaños aparecen en la infancia tardía; pueden existir desde unos pocos hasta varios miles.
Más raramente presentan nódulos subcutáneos por crecimiento amorfo de las células de Schwann -dando lugar a estructuras irregularmente engrosadas y distorsionadas (neuromas plexiformes)- o de los huesos subyacentes produciendo deformidades a veces grotescas. Las alteraciones esqueléticas incluyen displasia fibrosa, quistes óseos subperiósticos, vértebras festoneadas, escoliosis, seudoartrosis y ausencia del ala mayor del esfenoides (pared posterior de la órbita), con el consiguiente exoftalmos pulsátil.
Los neurofibromas (tumores formados por células de Schwann y fibroblastos neurales) raramente aparecen antes de la pubertad y pueden notarse a lo largo del trayecto subcutáneo de los nervios periféricos. Los neurofibromas pueden afectar a las raíces espinales y crecen de forma característica a través de los agujeros de conjunción formando una masa intra y extraespinal (tumores «en pesas»).
El componente intraespinal puede comprimir la médula. Los neuromas plexiformes pueden afectar a los nervios periféricos produciendo déficit distales a la lesión. Los tumores de los pares craneales incluyen gliomas ópticos, que producen ceguera progresiva, y neurinomas acústicos (schwannoma vestibular) que pueden dar lugar a vértigo, ataxia, cofosis y acufenos. Estos trastornos generalmente son progresivos.
En la neurofibromatosis tipo 2 suelen existir neurinomas acústicos bilaterales que suelen hacerse sintomáticos alrededor de los 20 años de edad. Los familiares de los pacientes pueden presentar gliomas o meningiomas y algunos padecen cataratas juveniles.
Tratamiento
Los neurofibromas que producen síntomas importantes pueden extirparse o irradiarse, aunque la cirugía puede impedir la función del nervio afectado. No existe ningún tratamiento general disponible. Es fundamental el consejo genético.
Síndrome de Proteus
Trastorno hereditario autosómico dominante caracterizado por macrocefalia, lipomas, hemangiomas, asimetría de los miembros superiores o inferiores y pies grandes y planos (pies en mocasín).
Este síndrome recibe su nombre por el dios griego Proteus, que se manifestaba con diferentes formas. Su causa es desconocida. Otras manifestaciones incluyen hipocalcemia, convulsiones y atrofia muscular. El tratamiento es sintomático.
Trastornos de la transmisión neuromuscular
La miastenia grave
Es el trastorno de la transmisión neuromuscular más frecuente. Una enfermedad autoinmune de la unión neuromuscular que se caracteriza por la variabilidad de la debilidad muscular, que empeora o está provocada por el ejercicio del músculo o de los grupos musculares implicados, mientras que el descanso la mejora.
El síndrome de Eaton-Lambert
Es un trastorno presináptico debido a alteración de la liberación de acetilcolina de las terminaciones nerviosas.
El botulismo
También es secundario a una disminución de la liberación de acetilcolina de las terminaciones presinápticas. La toxina producida por las esporas de Clostridium botulinum se une a las prolongaciones de la terminación colinérgica del nervio de forma irreversible. Como consecuencia aparece debilidad muscular grave, a veces con compromiso respiratorio, poco tiempo después de la ingestión de alimentos contaminados. Existe una leve disminución de la respuesta a la estimulación repetitiva, pero se produce un incremento pronunciado de la misma tras el ejercicio o con la estimulación repetitiva rápida (a 20 Hz).
Algunos fármacos y tóxicos pueden bloquear la unión neuromuscular. Los fármacos colinérgicos usados en el tratamiento de la miastenia grave, los insecticidas organofosforados y muchos gases bloquean la transmisión neuromuscular por depolarización de los receptores postsinápticos por un exceso de acetilcolina. Ello da lugar a miosis, broncorrea y debilidad muscular seudomiasténica. Los aminoglucósidos y los antibióticos polipeptídicos disminuyen la liberación presináptica de acetilcolina y la sensibilidad de la membrana postsináptica a la misma. Sobre todo con altos niveles séricos, estos antibióticos pueden aumentar el bloqueo neuromuscular en pacientes con defectos latentes o manifiestos de la transmisión neuromuscular. El tratamiento prolongado con penicilamina puede producir un síndrome reversible que recuerda clínica y electromiográficamente a la miastenia grave. El tratamiento consiste en la retirada del fármaco o agente tóxico y en el suministro de soporte respiratorio y cuidados intensivos. La atropina, a dosis de 0,4 a 0,6 mg v.o. 3 veces al día, disminuye la secreción bronquial en pacientes con hiperactividad colinérgica.
El síndrome del hombre rígido
Se caracteriza por el inicio insidioso de rigidez progresiva del tronco y, en menor grado, de los miembros inferiores y superiores. Los pacientes están, por lo demás, sanos y en la exploración sólo se detecta hipertrofia y rigidez muscular. La EMG muestra sólo la actividad eléctrica de la contracción normal. El síndrome puede ser autoinmune; se han encontrado autoanticuerpos contra la decarboxilasa del ácido glutámico. Sólo es posible un tratamiento sintomático. El diazepam es el único fármaco que disminuye la rigidez muscular de manera consistente. Los resultados de la plasmaféresis son objeto de discusión.
Bloqueo de conducción nerviosa:
En la evaluación diagnóstica de las neuropatías es muy importante conocer los resultados de los estudios de conducción nerviosa periférica y dentro de estos es bien conocida la utilidad que brindan variables electrofisiológicas como la latencia, velocidad de conducción y amplitud; sin embargo, dentro de las neuropatías existe un grupo (desmielinizantes adquiridas), en las que para su diagnóstico es importante definir la presencia o no de bloqueo de conducción nervioso.