Diferencia entre revisiones de «Punto isoeléctrico»
(Página creada con '{{Desarrollo}} {{Definición |nombre=Punto isoeléctrico |imagen= |tamaño= |concepto= PHdonde hay carga nula }}'''Punto isoeléctrico'''.El punto isoeléctrico se define como...') |
|||
| Línea 3: | Línea 3: | ||
|nombre=Punto isoeléctrico | |nombre=Punto isoeléctrico | ||
| − | |imagen= | + | |imagen=Punto_isoelectnuevarico.jpg |
|tamaño= | |tamaño= | ||
|concepto= PHdonde hay carga nula | |concepto= PHdonde hay carga nula | ||
| Línea 11: | Línea 11: | ||
En su calidad de proteína, la gelatina exhibe una conducta [[anfotérica]] debido a la presencia de grupos funcionales de [[aminoácidos]] y grupos amino y carboxil terminales. En medios acídicos, es decir en presencia de altas concentraciones de iones H+, la [[gelatina]] tiene carga positiva. En medios alcalinos, es decir en presencia de iones OH-, la gelatina tiene carga negativa. En el punto isoeléctrico (IEP) las cargas positivas de los radicales NH3+ igualan a las cargas negativas de los radicales COO-. | En su calidad de proteína, la gelatina exhibe una conducta [[anfotérica]] debido a la presencia de grupos funcionales de [[aminoácidos]] y grupos amino y carboxil terminales. En medios acídicos, es decir en presencia de altas concentraciones de iones H+, la [[gelatina]] tiene carga positiva. En medios alcalinos, es decir en presencia de iones OH-, la gelatina tiene carga negativa. En el punto isoeléctrico (IEP) las cargas positivas de los radicales NH3+ igualan a las cargas negativas de los radicales COO-. | ||
=== Punto isoeléctrico de aminoácidos y proteinas === | === Punto isoeléctrico de aminoácidos y proteinas === | ||
| − | Los puntos isoeléctricos proporcionan información útil para razonar sobre el comportamiento de los aminoácidos y proteínas en solución. Así, la presencia de grupos ionizables en éstas moléculas tiene importantes consecuencias sobre la solubilidad.<br /> | + | Los puntos isoeléctricos proporcionan información útil para razonar sobre el comportamiento de los [[aminoácidos]] y proteínas en solución. Así, la presencia de grupos ionizables en éstas moléculas tiene importantes consecuencias sobre la solubilidad.<br /> |
Los aminoácidos y las proteínas son menos solubles en su punto isoeléctrico si las demás condiciones permanecen iguales. Esto se debe a que los iones dipolares no presentan carga neta y cristalizan en forma de sales insolubles a ese pH. | Los aminoácidos y las proteínas son menos solubles en su punto isoeléctrico si las demás condiciones permanecen iguales. Esto se debe a que los iones dipolares no presentan carga neta y cristalizan en forma de sales insolubles a ese pH. | ||
| − | == IEP == | + | === IEP === |
El IEP es una propiedad intrínseca de la gelatina, determinada por los tratamientos de las materias primas y el tipo de proceso: | El IEP es una propiedad intrínseca de la gelatina, determinada por los tratamientos de las materias primas y el tipo de proceso: | ||
Las gelatinas Tipo A (ácidas) presentan un IEP que oscila entre 6 - 9.5. Sin embargo, el tratamiento previo de ciertas materias primas (como por ejemplo el proceso de depilado del cuero o piel) pueden bajar el IEP a menos de 6. | Las gelatinas Tipo A (ácidas) presentan un IEP que oscila entre 6 - 9.5. Sin embargo, el tratamiento previo de ciertas materias primas (como por ejemplo el proceso de depilado del cuero o piel) pueden bajar el IEP a menos de 6. | ||
Las gelatinas Tipo B (alcalinas) tienen un IEPque oscila entre 4.5 – 5.6. | Las gelatinas Tipo B (alcalinas) tienen un IEPque oscila entre 4.5 – 5.6. | ||
La gelatina con un IEP bajo se debe al fenómeno de deamidación de aminoácidos. Las gelatinas de Tipo A y B provenientes de materias primas tratadas o pre tratadas con sustancias alcalinas que eliminan los grupos de amidas, presentan un IEP bajo. | La gelatina con un IEP bajo se debe al fenómeno de deamidación de aminoácidos. Las gelatinas de Tipo A y B provenientes de materias primas tratadas o pre tratadas con sustancias alcalinas que eliminan los grupos de amidas, presentan un IEP bajo. | ||
| − | === Características === | + | ==== Características ==== |
| − | Las funcionalidades de las proteínas se ven afectadas cuando se aproximan al IEP, debido a la atracción electroestática de los grupos con carga opuesta. De esta manera, en el IEP las propiedades de la gelatina coinciden con los valores máximos o mínimos. Mínimos : hidratación, viscosidad y gelificación ; máximos: turbidez, fuerza de gel, poder de espumado y sinéresis- | + | Las funcionalidades de las [[proteínas]] se ven afectadas cuando se aproximan al IEP, debido a la atracción electroestática de los grupos con carga opuesta. De esta manera, en el IEP las propiedades de la gelatina coinciden con los valores máximos o mínimos. Mínimos : [[hidratación]], [[viscosidad]] y [[gelificación]] ; máximos: turbidez, fuerza de gel, poder de espumado y sinéresis- |
El IEP es útil para explicar las posibles interacciones de la gelatina con otros ingredientes, en particular los polímeros aniónicos. Por ejemplo, una gelatina Tipo B interactúa mejor con un polímero aniónico (ej. carrageninas en el mousse de chocolate) para evitar la precipitación por incompatibilidad, que depende de las condiciones de pH. | El IEP es útil para explicar las posibles interacciones de la gelatina con otros ingredientes, en particular los polímeros aniónicos. Por ejemplo, una gelatina Tipo B interactúa mejor con un polímero aniónico (ej. carrageninas en el mousse de chocolate) para evitar la precipitación por incompatibilidad, que depende de las condiciones de pH. | ||
| Línea 26: | Línea 26: | ||
*[http://bioqm.blogspot.com/2011/08/ punto-isoelectrico-de-aminoacidos-y.html] | *[http://bioqm.blogspot.com/2011/08/ punto-isoelectrico-de-aminoacidos-y.html] | ||
*[http://www.rousselot.com/es/gelatina-rousselot/caracteristicas-de-la-gelatina/definicion-descripcion/ punto-iso-electrico/] | *[http://www.rousselot.com/es/gelatina-rousselot/caracteristicas-de-la-gelatina/definicion-descripcion/ punto-iso-electrico/] | ||
| + | == Ver también == | ||
| + | *[[Bioquímica]] | ||
[[Category:Química]] | [[Category:Química]] | ||
Revisión del 17:32 20 mar 2014
| ||||||
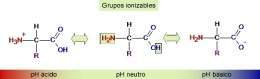
Punto isoeléctrico.El punto isoeléctrico se define como el pH en el cual el número de cargas positivas se iguala al número de cargas negativas que aportan los grupos ionizables de una molécula. En el punto isoeléctrico la carga neta de la molécula es cero (0). En los aminoácidos los grupos ionizables corresponden a grupos carboxilos, amino, fenólicos y tiólicos.
Sumario
Introducción
En su calidad de proteína, la gelatina exhibe una conducta anfotérica debido a la presencia de grupos funcionales de aminoácidos y grupos amino y carboxil terminales. En medios acídicos, es decir en presencia de altas concentraciones de iones H+, la gelatina tiene carga positiva. En medios alcalinos, es decir en presencia de iones OH-, la gelatina tiene carga negativa. En el punto isoeléctrico (IEP) las cargas positivas de los radicales NH3+ igualan a las cargas negativas de los radicales COO-.
Punto isoeléctrico de aminoácidos y proteinas
Los puntos isoeléctricos proporcionan información útil para razonar sobre el comportamiento de los aminoácidos y proteínas en solución. Así, la presencia de grupos ionizables en éstas moléculas tiene importantes consecuencias sobre la solubilidad.
Los aminoácidos y las proteínas son menos solubles en su punto isoeléctrico si las demás condiciones permanecen iguales. Esto se debe a que los iones dipolares no presentan carga neta y cristalizan en forma de sales insolubles a ese pH.
IEP
El IEP es una propiedad intrínseca de la gelatina, determinada por los tratamientos de las materias primas y el tipo de proceso: Las gelatinas Tipo A (ácidas) presentan un IEP que oscila entre 6 - 9.5. Sin embargo, el tratamiento previo de ciertas materias primas (como por ejemplo el proceso de depilado del cuero o piel) pueden bajar el IEP a menos de 6. Las gelatinas Tipo B (alcalinas) tienen un IEPque oscila entre 4.5 – 5.6. La gelatina con un IEP bajo se debe al fenómeno de deamidación de aminoácidos. Las gelatinas de Tipo A y B provenientes de materias primas tratadas o pre tratadas con sustancias alcalinas que eliminan los grupos de amidas, presentan un IEP bajo.
Características
Las funcionalidades de las proteínas se ven afectadas cuando se aproximan al IEP, debido a la atracción electroestática de los grupos con carga opuesta. De esta manera, en el IEP las propiedades de la gelatina coinciden con los valores máximos o mínimos. Mínimos : hidratación, viscosidad y gelificación ; máximos: turbidez, fuerza de gel, poder de espumado y sinéresis-
El IEP es útil para explicar las posibles interacciones de la gelatina con otros ingredientes, en particular los polímeros aniónicos. Por ejemplo, una gelatina Tipo B interactúa mejor con un polímero aniónico (ej. carrageninas en el mousse de chocolate) para evitar la precipitación por incompatibilidad, que depende de las condiciones de pH.