Teoría del campo cristalino
| ||||||
Teoría del campo cristalino. Considera la interacción entre un metal de transición y un grupo de ligandos deriva de la atracción entre el catión metálico positivamente cargado y la carga negativa de los pares de electrones no enlazantes de los ligandos.
Desarrollo
La teoría fue desarrollada bajo la suposición de que estos electrones no enlazantes de los ligandos producían repulsiónes sobre los electrones de los orbitales d del catión central que terminaban por deformar los cinco orbitales d degenerados (esto significa de iguales energías) del catión, alterando sus energías.
Orbital
Un orbital deformado posee mayor energía que un orbital nativo. Si se considera un campo repulsivo perfectamente esférico los cinco orbitales d deberían deformarse en la misma proporción y por lo tanto continuarían siendo degenerados, pero la TCC parte de la suposición de que los ligandos son cargas repulsivas puntuales, ubicadas en posiciones específicas del espacio, por lo tanto las repulsiones sobre los electrones de los orbitales d resultan asimétricas, lo que produce asimetrías en la manera en que deforman los orbitales causando que los cinco orbitales d de iguales energías (degenerados) se separen en varios grupos de diferente energía.
Consideraciones
Esta teoría considera sólo la geometría de los orbitales d de un catión central y su interacción con unos ligantes considerados como cargas negativas puntuales. Según este modelo los ligandos son atraídos por la carga positiva del metal, pero al aproximarse generan repulsiones sobre los electrones d del catión deformando los orbitales en los que estos se encuentran. Un orbital deformado presenta una mayor energía que uno con su forma "natural" por lo que los electrones tienden a ocupar posiciones en los orbitales "nativos" siempre que resulte posible, esto es siempre que la diferencia de energía entre los orbitales de mayor y los de menor energía no sea menor que la energía de apareamiento debida a la repulsión de los electrones en un mismo orbital.
Un ejemplo sencillo es lo que ocurre para un complejo octaédrico, si se hace la suposición de que los ligandos avanzan sobre los ejes de un sistema cartesiano tridimensional, los orbitales que se van a ver principalmente afectados son los que tienen componentes principales sobre estos ejes. al ver el gráfico de orbitales d se puede notar que estos orbitales son el d z2 y el dx2-y2. Como consecuencia aumentan su energía y se separan del resto de los orbitales d, formando dos subgrupos de orbitales: el grupo de alta energía eg y el grupo de baja energía t2g. El grado de separación entre orbitales eg y t2g va a depender de la fuerza de los ligantes, es decir del grado en que estos ligantes sean capaces de deformar los orbitales d. La serie espectroquímica es una tabla empírica que ordena los ligandos de acuerdo al grado de separacíon que causan en los orbitales d, de menor a mayor fuerza son:
I− < Br− < S2− < SCN− < Cl− < NO3− < N3- < F− < OH− < C2O42− < H2O < NCS− < CH3CN < py < NH3 < en < 2,2'-bipiridina < phen < NO2− < PPh3 < CN− < CO
Según este modelo las transiciones electrónicas entre estos orbitales d de diferente energía son las responsables de las absorciones de determinadas longitudes de onda que dan color a los complejos (a menor longitud de onda mayor energía y por tanto mayor fuerza del ligando). Cuando la separación entre orbitales de baja energía y de alta energía es mayor que la energía de apareamiento de los electrones, todos los electrones tienden a ocupar posiciones en los orbitales de baja energía de acuerdo al principio de Aufbau, formando lo que se conoce como un complejo de bajo espín. Por otro lado si la separación entre orbitales es menor que la energía de apareamiento, los electrones tienden a ocupar todos los orbitales (sean de baja o alta energía) antes de empezar a aparearse de acuerdo a la regla de Hund, formando lo que se conoce como un complejo de alto espín. De acuerdo a este modelo la cantidad de electrones en condiciones de espín apareado o desapareado, son las responsables de las propiedades magnéticas de los complejos.
Configuraciones
En inglés la palabra "spin" significa literalmente "giro" como el giro de un trompo sobre sí mismo, al hablar de orbitales atómicos o moleculares la palabra spin, castellanizada como espín hace referencia al cuarto número cuántico de los electrones, el número de momento angular intrínseco que brinda la noción de cómo "gira" un electrón sobre su eje. Ya que, como lo indica el principio de exclusión de Pauli, ningún electrón en un átomo puede tener sus cuatro números cuánticos iguales a otro cuando dos electrones ocupan un mismo orbital (es decir, ya tienen sus primeros tres números cuánticos iguales) deben hacerlo de modo que su cuarto número cuántico sea diferente, para el electrón solo existen dos estados cuánticos de espín posibles: -1/2 y +1/2, que comúnmente se llaman "espines opuestos"). Sin embargo existe, además, un cierto grado de repulsión entre electrones que ocupan un mismo orbital. Este grado de repulsión causa lo que se denomina energía de apareamiento, que es la energía que hay que entregarle a un electrón para que ocupe un orbital que ya se encuentra semilleno. Es por esto que un electrón, cuando tiene la posibilidad de optar entre varios orbitales degenerados (con la misma energía), tratará siempre de ocupar el mayor número posible de orbitales vacíos antes de empezar a completar orbitales semillenos. Esto que se conoce como regla de Hund es la base en la que se sustentan las propiedades magnéticas y algunas de las propiedades ópticas de los complejos.
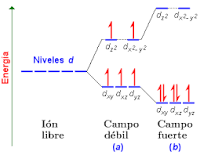
Los ligandos que causan una gran separación Δ en los orbitales atómicos d del metal se suelen referir como ligandos de campo fuerte, tales como por ejemplo el CN− y CO de la serie espectroquímica. En complejos formados por estos ligandos la separación en energía Δ entre el grupo de orbitales de mayor y menor energía resulta mayor que la energía de apareamiento de los electrones, esto causa que los orbitales de menor energía se completen, aún a costa del apareamiento de electrones, antes de comenzar a completar los de mayor energía (ocurre según el principio de Aufbau) este tipo de compuestos son llamados de "bajo espín", porque en ellos la suma de los momentos magnéticos causados por los electrones es la mínima posible. Por ejemplo, el NO2− es un ligando de campo fuerte y produce una gran Δ. El ion octaédrico Fe(NO2)6]3− que posee 5 electrones d, muestra un diagrama de campo octaédrico donde todos los electrones se encuentran en el nivel t2g, este ion es por lo tanto un complejo de espín bajo.
Por el contrario, ligandos como el I− y Br−, que causan un pequeño grado de separación Δ entre orbitales d son llamados "ligandos de campo débil". En estos complejos resulta energéticamente más rentable para los electrones ocupar todos los orbitales siguiendo la regla de Hund, es decir haciéndolo con espines desapareados. Esto ocurre así porque la energía de apareamiento es mayor que la separación Δ entre orbitales de baja y alta energía. Un complejo de este tipo se dice que es de "alto espín" porque la suma de los momentos magnéticos de todos sus electrones es la máxima posible. Por ejemplo, Br− es un ligando de campo débil y produce una Δoct pequeña. De modo que el ion [FeBr6]3−, que también posee cinco electrones d, muestra un diagrama de campo octaédrico con los cinco orbitales semillenos. Este ion por lo tanto es un complejo de espín alto.
Es decir que para que se forme un complejo de bajo espín, el costo energético de colocar un electrón en un orbital semilleno tiene que ser menor que el costo de colocar a ese mismo electrón desapareado en un orbital de mayor energía. Por otro lado si el costo energético de colocar un electrón en un orbital semilleno es mayor que la separación entre orbitales de menor y mayor energía, entonces se forma un complejo de alto espín. La brecha energética para un complejo metálico tetraédrico (con cuatro ligandos), Δtet es aproximadamente igual a 4/9 de Δoct. Esto significa que la energía requerida para aparear dos electrones en estos complejos es típicamente mayor que la energía requerida para colocar electrones en orbitales de alta energía. Por lo tanto, los complejos tetraédricos son, usualmente, de espín alto.
La utilización de estos diagramas de separación energética puede ayudar en la predicción de las propiedades magnéticas de los compuestos de coordinación. Un compuesto que en su diagrama de separación energética muestra electrones con espines desapareados será paramagnético y se verá atraído por los campos magnéticos, mientras que un compuesto que no posea electrones desapareados en su diagrama energético será diamagnético y se verá débilmente repelido por los campos magnéticos.
Fuentes
- Zumdahl, Steven S. Chemical Principles Fifth Edition. Boston: Houghton Mifflin Company, 2005. 550-551,957-964.
- Silberberg, Martin S. Chemistry: The Molecular Nature of Matter and Change, Fourth Edition. New York: McGraw Hill Company, 2006. 1028-1034.
- D. F. Shriver and P. W. Atkins Inorganic Chemistry 3rd edition, Oxford University Press, 2001. Pages: 227-236.