Cátodo
| ||||
Cátodo. Es el electrodo negativo, donde los iones (átomos cargados eléctricamente) que se dirigen del ánodo (electrodo positivo)al cátodo, reciben el nombre de cationes, y los iones que se dirigen del cátodo al ánodo tienen el nombre de aniones. En griego antiguo (kathodos) significa: camino hacia abajo, pero Faraday la utilizó para referirse a un electrodo con carga negativa del cual fluye la corriente.
Etimología del término
La palabra Cátodo es un neologismo acuñado por Michael Faraday (1791-1867) usando las raíces griegas: cata = hacia abajo, como en catarata y catástrofe y odos = camino, como en éxodo y período.
Faraday también acuñó la palabra electrodo formada de eléctrico y odos, o sea: camino eléctrico.
Descripción
| Cátodo | Ánodo | Catión | Anión |
|---|---|---|---|
| Electrodo negativo | Electrodo positivo | Ion con carga positiva que se va del ánodo al cátodo | Ion con carga negativa que se va del cátodo al ánodo |
Un error muy extendido es pensar que la polaridad del cátodo es siempre negativa (-). La polaridad del cátodo depende del tipo de dispositivo, y a veces incluso en el modo que opera, según la dirección de la corriente eléctrica, basado en la definición de corriente eléctrica universal. En consecuencia, en un dispositivo que consume energía el cátodo es negativo, y en un dispositivo que proporciona energía el cátodo es positivo.
El término fue inventado por Faraday (serie VII de las Investigaciones experimentales sobre la electricidad), con el significado de camino descendente o de salida, pero referido exclusivamente al electrolito de una celda electroquímica. Su vinculación al polo negativo del correspondiente generador implica la suposición de que la corriente eléctrica que marcha por el circuito exterior desde el polo positivo al negativo, es decir, transportada por cargas positivas, convención que es la usual. Si el conductor externo fuera metálico, está demostrado que el sentido de la corriente realmente es el recorrido por los electrones hacia el positivo.
Sin embargo, en una célula electrolítica, el conductor es el electrolito, no un metal, y en él pueden coexistir iones negativos y positivos que tomarían sentidos opuestos al desplazarse. Por convenio se adopta que el sentido de la corriente es el del ánodo al cátodo o, lo que es lo mismo, del positivo al negativo.
En el caso de las válvulas termoiónicas, diodos, tiristores, fuentes eléctricas, pilas, etc. el cátodo es el electrodo o terminal de menor potencial y es la fuente primaria de emisión de electrones. Por ende, en una reacción redox corresponde al elemento que se reducirá.
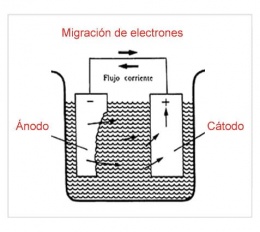
El flujo de electrones
El flujo de electrones es siempre del ánodo al cátodo exterior de la célula o dispositivo, independientemente del tipo celular o dispositivo y el modo de funcionamiento, con la excepción de los diodos en el electrodo de nombres supone siempre la corriente fluye en la dirección delantera, es decir, el flujo de electrones en la dirección opuesta, aun cuando el diodo inverso se lleva a cabo ya sea por accidente (rotura de un diodo normal) o por diseño (ruptura de un diodo Zener, la foto-corriente de un fotodiodo o células solares).
En química, un cátodo es el electrodo de una célula electroquímica en la que la reducción se produce.
El cátodo puede ser negativo como cuando la célula se electrolítico (donde la energía eléctrica suministrada a la célula se utiliza para descomponer los compuestos químicos), o positivos cuando la célula se galvánica (donde las reacciones químicas se utilizan para generar energía eléctrica).
El cátodo suministra electrones a la carga positiva que el flujo de cationes transmite a ella desde el electrolito (incluso si la celda es, es decir, galvánica, cuando el cátodo es positivo y por lo tanto se espera repeler la carga positiva de cationes, esto se debe al potencial de electrodo en relación a la solución de electrolitos diferentes para el ánodo y el cátodo de metal y sistemas de electrolitos en una pila galvánica).