Electrodinámica
Electrodinámica. Estudio de las relaciones entre los fenómenos eléctricos, magnéticos y mecánicos. Incluye el análisis de los campos magnéticos producidos por las corrientes, las fuerzas electromotrices inducidas por campos magnéticos variables, la fuerza sobre las corrientes en campos magnéticos, la propagación de las ondas electromagnéticas y el comportamiento de partículas cargadas en campos magnéticos y eléctricos.
La electrodinámica clásica se ocupa de los campos y las partículas cargadas en la forma original descrita sistemáticamente por James Clerk Maxwell, en tanto que la electrodinámica cuántica aplica los principios de la mecánica cuántica a los fenómenos eléctricos y magnéticos. La electrodinámica relativista trata de la conducta de las partículas cargadas y de los campos, cuando la velocidad de ellas se aproxima a la de la luz.
Reseña histórica
En 1831, luego de una larga serie de experimentos, Michael Faraday encontró una relación nueva entre efectos eléctricos y magnéticos. Se sabía, luego de los trabajos de Oersted y Ampère, entre otros, que una corriente eléctrica (un campo eléctrico) crea efectos magnéticos. Faraday estaba convencido de la simetría en las leyes de la naturaleza, y de la observación de la inducción electrostática y la "inducción" de efectos magnéticos por corrientes eléctricas creía que un campo magnético debía crear efectos eléctricos. Sin embargo, la relación era más sutil: son las variaciones en el tiempo del campo magnético las que crean un campo eléctrico. Citamos las propias palabras de Faraday, en su presentación ante la Royal Institución, de Londres. En la introducción a la primera serie de experimentos, relacionados con la inducción electromagnética, Faraday presenta los objetivos y antecedentes de estas investigaciones:
Electrodinámica
La electrodinámica se fundamenta, precisamente, en el movimiento de los electrones o cargas eléctricas que emplean como soporte un material conductor de la corriente eléctrica para desplazarse.
Todos los cuerpos conocidos en la naturaleza, ya sean sólidos, líquidos o gaseosos, se componen de átomos o moléculas de elementos químicos simples o compuestos. Las moléculas del agua que tomamos para aliviar la sed, por ejemplo, están formadas por dos átomos de hidrógeno y uno de oxígeno (H2O).
En un vaso de agua están presentes miles de millones de moléculas formadas por esos dos elementos químicos.
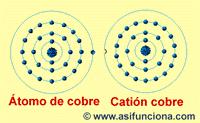
Todos los átomos o moléculas simples se componen de un núcleo formado por protones y neutrones, y alrededor de ese núcleo gira constantemente una nube de electrones situados en una o en varias órbitas, según el elemento químico de que se trate, de forma similar a como giran los planetas alrededor del sol. Es decir, que cada átomo viene siendo un sistema solar en miniatura, tal como se puede ver en la ilustración del átomo de cobre (Cu), que aparece a la izquierda.
Los protones de los átomos poseen siempre carga eléctrica positiva, los neutrones carga neutra y los electrones carga eléctrica negativa.
La cantidad de protones presentes en el núcleo de un átomo neutro siempre es igual a la de los electrones que se encuentran girando en sus respectivas órbitas. Un átomo en estado neutro tiene el mismo número de cargas negativas que positivas.
Átomo
Un átomo puede ganar o ceder electrones de su última órbita empleando medios químicos o eléctricos y convertirse así en un ión negativo o positivo del elemento de que se trate, exceptuando los átomos de los gases nobles.
En ese caso podemos decir que se trata del ión de un elemento determinado como pudiera ser, por ejemplo, hidrógeno (H), cobre (Cu), zinc (Zn), plomo (Pb), etc.
Cuando el átomo cede o pierde electrones se convierte en un ión positivo o catión, pues la cantidad de protones con carga positiva superará a la de los electrones con carga negativa. Si por el contrario, el átomo en lugar de ceder electrones los capta o gana en su última órbita, se convierte en un ión negativo o anión, al ser superior la cantidad de electrones con carga negativa en relación con la carga positiva de los protones agrupados en el núcleo. Es necesario aclarar que el máximo de electrones que puede contener la última capa u órbita de un átomo son ocho.