Enlace metálico
| ||||||
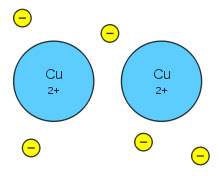
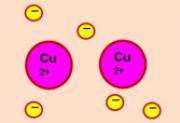
Enlace metálico:Es un enlace químico que ocurre entre los átomos de metales entre sí, (unión entre núcleos atómicos y los electrones de valencia, que se agrupan alrededor de éstos como una nube). Es un enlace fuerte, primario, que se forma entre elementos de la misma especie, en este enlace todos los átomos envueltos pierden electrones de sus capas más externas, que se trasladan más o menos libremente entre ellos, formando una nube electrónica (también conocida como mar de electrones).
Es el tipo de enlace que se produce cuando se combinan entre sí los elementos metálicos; es decir, elementos de electronegatividades bajas y que se diferencien poco.
Sumario
Estructura de la sustancia metálica
Los átomos de los metales se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de redes tridimensionales que adquieren estructuras tales como: la típica de empaquetamiento compacto de esferas ( hexagonal compacta ), cubica centrada en las caras o la cubica centrada en el cuerpo en las tres dimensiones, por lo que quedan los núcleosodeados de tales nubes
En este tipo de estructura cada átomo metálico está rodeado por otros doce átomos (seis en el mismo plano, tres por encima y tres por debajo). Además, debido a la baja electronegatividad que poseen los metales, los electrones de valencia son extraídos de sus orbitales y tienen la capacidad de moverse libremente a través del compuesto metálico, lo que otorga a éste las propiedades eléctricas y térmicas. Este enlace sólo puede presentarse en sustancias en estado sólido.
Los elementos con un enlace metálico están compartiendo un gran número de electrones de valencia, formando un mar de electrones rodeando un enrejado gigante de cationes. Muchos de los metales tienen puntos de fusión más altos que otros elementos no metálicos, por lo que se puede inferir que hay enlaces más fuertes entre los distintos átomos que los componen. La vinculación metálica es no polar, apenas hay diferencia de electronegatividad entre los átomos que participan en la interacción de la vinculación (en los metales elementales puros) o muy poca (en las aleaciones), y los electrones implicados en lo que constituye la interacción a través de la estructura cristalina del metal.
Propiedades de la sustancia metálica
El enlace metálico explica muchas características físicas de las sustancias metálicas, tales como fuerza, maleabilidad, ductilidad, conducción de calor y de la electricidad, y brillo o lustre (devuelven la mayor parte de la energía lumínica que reciben). La vinculación metálica es la atracción electrostática entre los átomos del metal o cationes y los electrones deslocalizados. Esta es la razón por la cual se puede explicar un deslizamiento de capas, dando por resultado su característica maleabilidad y ductilidad. Presentan el llamado "efecto fotoeléctrico"; es decir, cuando son sometidos a una radiación de determinada energía, emiten electrones. Se suelen disolver unos en otros formando disoluciones que reciben el nombre de aleaciones.
Los átomos del metal tienen por lo menos un electrón de valencia, no comparten estos electrones con los átomos vecinos, ni pierden electrones para formar los iones. En lugar los niveles de energía externos de los átomos del metal se traslapan. Son como enlaces covalentes identificados.
Modelo de enlace
Existen dos modelos que explican la formación del enlace metálico. El modelo de la nube de electrones y la teoría de bandas.
Modelo de la nube de electrones:
Según este modelo, los átomos metálicos ceden sus electrones de valencia a una nube electrónica que comprende todos los átomos del metal. Así pues, el enlace metálico resulta de las atracciones electrostáticas entre los restos positivos y los electrones móviles que pertenecen en su conjunto a la red metálica.
En el enlace metálico, los electrones no pertenecen a ningún átomo determinado. Además, es un enlace no dirigido, porque la nube electrónica es común a todos los restos atómicos que forman la red.
Hay que aclarar que los átomos cuando han cedido los electrones a la nube común, no son realmente iones, ya que los electrones quedan dentro de la red, perteneciendo a todos los restos positivos.
Este modelo es muy simple y sirve para interpretar muchas de las propiedades de los metales; aunque tiene ciertas limitaciones, principalmente en la explicación de la diferente conductividad de algunos metales.
Teoría de bandas:
Esta teoría representa un modelo más elaborado para explicar la formación del enlace metálico; se basa en la teoría de los orbitales moleculares. Esta teoría mantiene que cuando dos átomos enlazan, los orbitales de la capa de valencia se combinan para formar dos orbitales nuevos que pertenecen a toda la molécula, uno que se denomina enlazante (de menor energía) y otro antienlazante (de mayor energía). Si se combinasen 3 átomos se formarían 3 orbitales moleculares, con una diferencia de energía entre ellos menor que en el caso anterior. En general, cuando se combinan N orbitales, de otros tantos átomos, se obtienen N orbitales moleculares de energía muy próxima entre sí, constituyendo lo que se llama una banda
En los metales existe un número muy grande de orbitales atómicos para formar enlaces deslocalizados que pertenezcan a toda la red metálica (como si fuese una gran molécula). Como el número de orbitales moleculares es muy grande forman una banda en la que los niveles de energía, como se ha dicho anteriormente, están muy próximos.
En los metales se forman dos bandas. Una en la que se encuentran los electrones de la capa de valencia que se denomina "banda de valencia" y otra que se llama "banda de conducción" que es la primera capa vacía.
En las sustancias metálicas, la banda de valencia está llena o parcialmente llena; pero en estas sustancias, la diferencia energética entre la banda de valencia y la de conducción es nula; es decir están solapadas. Por ello, tanto si la banda de valencia está total o parcialmente llena, los electrones pueden moverse a lo largo de los orbitales vacios y conducir la corriente eléctrica al aplicar una diferencia de potencial.
En el caso de los aislantes la banda de valencia está completa y la de conducción vacía; pero a diferencia de los metales, no sólo no solapan sino que además hay una importante diferencia de energía entre una y otra (hay una zona prohibida) por lo que no pueden producirse sa
ltos electrónicos de una a otra. Es decir, los electrones no gozan de la movilidad que tienen en los metales y, por ello, estas sustancias no conducen la corriente eléctrica.
Un caso intermedio lo constituyen los semiconductores, en el caso de las sustancias de este tipo, la banda de valencia también está llena y hay una separación entre las dos bandas, pero la zona prohibida no es tan grande, energéticamente hablando, y algunos electrones pueden saltar a la banda de conducción. Estos electrones y los huecos dejados en la banda de valencia permiten que haya cierta conductividad eléctrica. La conductividad en los semiconductores aumenta con la temperatura, ya que se facilitan los saltos de los electrones a la banda de conducción. Son ejemplos de semiconductores: Ge, Si, Ga,As y InSb.
Referencias
- Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Materiales Complementarios de Química para Ingenieros. Ed. Pueblo y Educación. . Ciudad de La Habana, Cuba. 1987.
- León Ramírez, R.: Química General. Ed. Pueblo y Educación. . Ciudad de La Habana, Cuba. 1985.
Fuentes
- http://iesdolmendesoto.org/zonatic/el_enlace_quimico/enlace/enlace_metalico.html
- http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/enlaces/metalico.html.
Enlace externo