Diferencia entre revisiones de «Metano»
m (Texto reemplazado: «<div align="justify">» por «») |
|||
| (No se muestran 7 ediciones intermedias de 5 usuarios) | |||
| Línea 1: | Línea 1: | ||
| + | |||
| + | |||
{{Definición | {{Definición | ||
|nombre=Metano | |nombre=Metano | ||
|imagen=metano1.jpg | |imagen=metano1.jpg | ||
|tamaño= | |tamaño= | ||
| − | |concepto= Compuesto resultante de la fusión del [[Carbono]] y el [[Hidrógeno]], su fórmula es | + | |concepto= Compuesto resultante de la fusión del [[Carbono]] y el [[Hidrógeno]], su fórmula es CH<sub>4</sub>. |
| − | }}'''Metano.''' Compuesto de [[Carbono]] e [[Hidrógeno]], de fórmula | + | |etiq_cubadebate = metano |
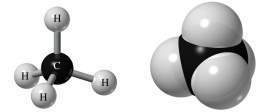
| + | }}'''Metano.''' Compuesto de [[Carbono]] e [[Hidrógeno]], de fórmula CH<sub>4</sub>, cada uno de los átomos de hidrógeno está unido al de carbono por medio de un enlace covalente. Es un hidrocarburo, el primer miembro de la serie de los alcanos. | ||
== Propiedades == | == Propiedades == | ||
| − | Es más ligero que el aire, incoloro, inodoro e inflamable. Alcanza un punto de fusión de -182,5 °C y un punto de ebullición de -161,5 °C. Esta sustancia | + | Es más ligero que el [[aire]], incoloro, inodoro e [[inflamable]]. Alcanza un punto de fusión de -182,5 °C y un punto de ebullición de -161,5 °C. Esta sustancia en su estado líquido no es [[combustible]]. |
== Obtención == | == Obtención == | ||
| − | Puede obtenerse mediante la hidrogenación de carbono o dióxido de carbono, por la acción del agua con carburo de aluminio o también al calentar etanoato de sodio con álcali. De forma natural se encuentra como gas grisú de las minas de carbón y como producto de la descomposición de la materia orgánica en los | + | Puede obtenerse mediante la hidrogenación de carbono o dióxido de carbono, por la acción del agua con [[carburo de aluminio]] o también al calentar [[etanoato de sodio]] con álcali. De forma natural se encuentra como gas grisú de las minas de [[carbón]] y como producto de la descomposición de la materia orgánica en los pantanos, así como en el producto final de la putrefacción anaeróbica de las [[plantas]]. Este proceso natural se puede aprovechar para producir [[biogás]]. |
== Usos == | == Usos == | ||
| − | Se emplea como combustible en la generación de electricidad, su principal uso es en actividades donde se necesite su combustión. | + | Se emplea como combustible en la generación de [[electricidad]], su principal uso es en actividades donde se necesite su combustión. |
| − | En la industria química, el metano es la materia prima elegida para la producción de hidrógeno, metanol, ácido acético y anhidro acético. | + | En la industria química, el metano es la materia prima elegida para la producción de [[hidrógeno]], [[metanol]], [[ácido acético]] y anhidro acético. |
== Fuentes == | == Fuentes == | ||
| Línea 22: | Línea 25: | ||
== Enlaces externos == | == Enlaces externos == | ||
| − | *[http://es.wikipedia.org/wiki/Metano] | + | *[http://es.wikipedia.org/wiki/Metano Metano] |
| − | *[http://html.rincondelvago.com/el-metano.html] | + | *[http://html.rincondelvago.com/el-metano.html El Metano] |
| − | [[ | + | [[category:gases]][[Categoría:Hidrocarburos_alifáticos]] |
última versión al 21:31 28 ago 2019
| ||||||||
Metano. Compuesto de Carbono e Hidrógeno, de fórmula CH4, cada uno de los átomos de hidrógeno está unido al de carbono por medio de un enlace covalente. Es un hidrocarburo, el primer miembro de la serie de los alcanos.
Propiedades
Es más ligero que el aire, incoloro, inodoro e inflamable. Alcanza un punto de fusión de -182,5 °C y un punto de ebullición de -161,5 °C. Esta sustancia en su estado líquido no es combustible.
Obtención
Puede obtenerse mediante la hidrogenación de carbono o dióxido de carbono, por la acción del agua con carburo de aluminio o también al calentar etanoato de sodio con álcali. De forma natural se encuentra como gas grisú de las minas de carbón y como producto de la descomposición de la materia orgánica en los pantanos, así como en el producto final de la putrefacción anaeróbica de las plantas. Este proceso natural se puede aprovechar para producir biogás.
Usos
Se emplea como combustible en la generación de electricidad, su principal uso es en actividades donde se necesite su combustión.
En la industria química, el metano es la materia prima elegida para la producción de hidrógeno, metanol, ácido acético y anhidro acético.