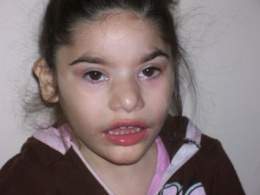
Síndrome de Angelman
| ||||||
Síndrome de Angelman. Es una enfermedad neuro-genética caracterizada por un retraso en el desarrollo, una capacidad lingüística reducida o nula, escasa receptividad comunicativa, escasa coordinación motriz, con problemas de equilibrio y movimiento, ataxia, estado aparente permanente de alegría, con risas y sonrisas en todo momento, siendo fácilmente excitables, hipermotricidad, déficit de atención. Tiene una incidencia estimada de una entre 15.000 y 30.000 nacimientos. Es un ejemplo clásico de enfermedad con herencia epigenética, dado que las mutaciones y defectos que lo causan implican o no el desarrollo de la enfermedad en función de si la copia del gen alterado proviene del padre o de la madre. La zona donde se encuentran estas mutaciones está en el cromosoma 15, en el mismo locus que el síndrome de Prader-Willi, el 15q11-q13.
Sumario
Descubrimiento y prevalencia actual
El pediatra Dr. Harry Angelman fue el primero en describir la enfermedad en tres niños en 1964. En aquel entonces fue considerada rara. En 1987, se descubrió que alrededor de la mitad de los niños que presentaban el síndrome tenían una pequeña deleción del brazo «q» del cromosoma 15, y se propuso además la relación entre éste síndrome y el de Prader-Willi. Las estimaciones más recientes sugieren una prevalencia entre 1/12,000 y 1/20,000.
Síntomas
El síndrome de Angelman no suele ser reconocido en los bebés recién nacidos, debido a que los problemas de desarrollo que ocasiona esta enfermedad no son específicos durante este período. Sí se produce un retraso en el desarrollo del niño entorno a los 6-12 meses de edad, aunque no hay una pérdida evidente de habilidades por parte del afectado. No aparece tampoco ninguna anomalía en los análisis metabólicos, hematológicos ni en los perfiles químicos de laboratorio. Tampoco se observa ninguna anomalía física. Sí puede haber una atrofia cortical leve o una desmielización. El síndrome suele ser diagnosticado entorno a los 3-7 años de edad, cuando aparecen en el niño conductas y rasgos que evidencian la enfermedad. No es necesario que un individuo presente todos los rasgos típicos de esta enfermedad para que le sea diagnosticada.
Síntomas universales
En todos los individuos afectados por la enfermedad se dan los siguientes síntomas:
- Retraso importante en el desarrollo.
- Capacidad lingüística reducida o nula.
- Escasa receptividad comunicativa, basándose la poca que hay principalmente en gestos y señales.
- Escasa coordinación motriz, con problemas de equilibrio y movimiento. Suele aparecer ataxia.
- Estado aparente permanente de alegría, con risas y sonrisas en todo momento, siendo fácilmente excitables.
- Hipermotricidad
- Falta de atención
Síntomas frecuentes
En un gran porcentaje de los afectados por la enfermedad, que ronda el 80%, se dan los siguientes síntomas:
- Retraso mental
- Tamaño inferior del perímetro cefálico respecto al de los no afectados, que suele derivar en microcefalia entorno a los 2 años de edad.
- Crisis convulsivas normalmente entorno a los 3 años de edad.
- Electroencefalograma anormal.
Síntomas raros
En menor frecuencia se dan los siguientes síntomas (entorno al 20% de los afectados los presentan):
- Estrabismo
- Dificultad al tragar
- Lengua prominente
- Mandíbula prominente
- Babeo frecuente
- Achatamiento posterior de la cabeza
- Atracción por el agua
- Hipersensibilidad al calor
- Insomnio
- Hipopigmentación en la piel y en los ojos
- Hiperactividad
Genética
Esta enfermedad es, junto con el síndrome de Prader-Willi, un ejemplo clásico de enfermedad genética cuyo origen y herencia depende del mecanismo de impronta genética. Ambas enfermedades se deben a la ausencia de expresión de genes que se encuentran en el mismo locus del cromosoma 15. Dentro de los genes que mapean en ese locus se encuentra el UBE3A (proteína ubiquitin-ligasa E3A). La expresión de este gen así como de otros cercanos depende de la regulación ejercida por un centro de impronta génica. Básicamente lo que ocurre es que si ese centro está metilado activa la expresión de unos genes, y si no, de otros. Si la diana falta, está mutada, o se metila de forma anormal, falta la expresión de UBE3A, así como si ocurre una deleción del gen. Por ello, las características clínicas observadas en el síndrome pueden ser causadas por diversas razones a nivel génico.
Principales causas genéticas
- Grandes deleciones en el locus: tienen lugar en el 70-75% de los individuos afectados.
- Otras anormalidades en cromosomas: tienen lugar en el 2% de los individuos afectados y se debe a reorganizaciones que causan ausencia de la región 15q11-13
- Disomía uniparental paterna: tiene lugar en el 4% de los individuos afectados, y se puede deber a varios eventos, pero supone que hay dos copias del cromosoma 15 paterno y ninguna del materno.
- Mutaciones en la diana de la impronta epigenética: sólo tienen lugar en el 1% de los individuos afectados.
- Mutaciones en UBE3A: tienen lugar en el 3-5% de los individuos afectados.
- Desconocidos: tienen lugar en el 15% de los individuos afectados. Agrupamos aquí aquellos casos que presentan la enfermedad pero ninguno de los anteriores defectos genéticos.
Recurrencia
Un incremento del riesgo de la recurrencia se puede producir en los casos de síndrome de Angelman que están asociados con un cromosoma 15 estructuralmente anormal. En dichos casos, el riesgo de recurrencia se debe anormalidad del cromosoma y lo que se sabe sobre su recurrencia. En estos casos, es posible el diagnóstico prenatal mediante análisis citónegeticos o moleculares.
Asimismo, un defecto en el mecanismo de metilación también tiene un posibilidad mayor de heredarse en toda la descendencia, pero hay muchas anormalidades de cáracter mayoritariamente espontáneo como las deleciones o la disomía uniparental cuyo riesgo de recurrencia es muy bajo (menor al 1%) o directamente desconocido (en el caso de ese porcentaje del 15% de casos sin causas genéticas definidas).
Diagnóstico
Existe un consenso sobre el diagnóstico de la enfermedad, que aparece reflejado en el trabajo de Williams et al. A nivel molecular, un primer análisis del cariotipo del individuo para detectar anomalías cromosómicas es la primera opción. Además también se realiza la prueba de FISH con la que gracias a los marcadores cromosómicos detectaremos si hay una deleción en el cromosoma 15. Algunos laboratorios además de estas dos pruebas realizan otra para obtener una fiabilidad mucho mayor, se trata del test de metilación del ADN. Este test permite identificar el tipo mas corriente de Síndrome de Angelman que es la deleción en la región el cromosoma 15. Alrededor del 80% de los pacientes que presentan Síndrome de Angelman se detectan con estas pruebas, pero el 20% necesitarán otro tipo de comprobación genética encaminada a los análisis para el gen UBE3A, y aún así no todos serán diagnosticados.
Tratamiento
Esta enfermedad solo puede curarse a través de la terapia génica. Pero si no, solo se pueden controlar algunos de sus síntomas. La epilepsia puede ser controlada mediante el uso de medicación anticonvulsionante, pero existen dificultades a la hora de definir los niveles de fármacos a suministrar. Además se suelen suministrar sustancias que incrementen el sueño ya que muchos afectados por el síndrome duermen como máximo 5 horas. En el tratamiento se utilizan principalmente intervenciones kinesiológicas y fonoaudiológicas, como asimismo diversas otras formas de terapia de apoyo (musicoterapia, hidroterapia, entre otras).
Pronóstico
La severidad de los síntomas asociados al síndrome de Angelman varían significativamente entre la población de personas afectadas. Algunos pueden hablar y tiene un alto grado de consciencia de si mismos e incluso muestran una profunda afectividad. Desafortunadamente, la capacidad de andar y el uso simplista del idioma pueden llevar al rechazo de un afecto mayor. La temprana y continua participación en terapias físicas, ocupacionales y comunicativas incrementan significativamente el pronóstico. Es más, existe todo un espectro en el grado de afección, que está relacionado desde la simple mutación del gen Ube3a hasta la pequeña deleción del brazo que del cromosoma 15. De esta forma, los afectados en la mutación presentan una afección menor que los que presentan la deleción.
Las características clínicas del síndrome se alteran con la edad. Cuando la edad adulta se aproxima, la hiperactividad y el insomnio se incrementan. Las convulsiones remiten e incluso cesan, y los electroencefalogramas son menos obvios. Las características faciales permanecen reconocibles pero muchos de estos adultos tienen un remarcado aspecto juvenil para su edad. La pubertad y la menstruación llegan a una edad normal, el desarrollo sexual es completo y se ha dado un caso en el que una mujer con síndrome de Angelman tuvo a una hija que también tuvo el síndrome. La mayoría de los adultos son capaces de comer con tenedor o cuchara. La salud es buena y tienen una esperanza de vida normal. Aunque se han descrito que algunos adultos, principalmente mujeres, tienen tendencia a la obesidad.
Algunos pueden presentar escoliosis. La afección natural que presentan estos individuos, que es un aspecto positivo en los niños, puede persistir durante su vida adulta, lo cual puede ocasionar problemas sociales.
Véase también
Enlaces externos
Fuentes
- Angelman, Harvey (1965). "'Puppet' Children: A report of three cases". Dev Med Child Neurol. 7: 681–688. doi:10.1111/j.1469-8749.1965.tb07844.x
- Magenis, RE; Brown MG, Lacy DA, Budden S, LaFranchi S. (1987). "Is Angelman syndrome an alternate result of del(15)(q11q13)?". Am J Med Genet. 28 (4): 829–38. doi:10.1002/ajmg.1320280407. PMID 3688021
- Steffenburg S, Gillberg CL, Steffenburg U, Kyllerman M (1996) Autism in Angelman syndrome: a population-based study. Pediatr Neurol 14:131-6
- Clayton-Smith J and Pembrey ME (1992) Angelman syndrome. J Med Genet 29:412-5
- Williams CA, Beaudet AL, Clayton-Smith J, et al. (2006). "Angelman syndrome 2005: updated consensus for diagnostic criteria". Am. J. Med. Genet. A 140 (5): 413–8. doi:10.1002/ajmg.a.31074. PMID 16470747.
- William Klug, "Conceptos de Genética", 8ª Edición.
- Angelman, H. "Puppet" children: A report on three cases. Dev Med Child Neurol.
- Lossie A, Driscoll D. «Transmission of Angelman syndrome by an affected mother.». Genet Med 1 (6): pp. 262-6. PMID 11258627.
- Weeber E, Levenson J, Sweatt J (2002). «Molecular genetics of human cognition.». Mol Interv 2 (6): pp. 376-91, 339. PMID 14993414.