Hidrocarburos
| ||||||
Hidrocarburos y sus derivados. Hay un número fantástico de compuestos de carbono e hidrógeno. Algunos de ellos, que solo constan de ambos elementos, se denominan hidrocarburos; otros contienen además elementos adicionales y son derivados de los hidrocarburos unos y otros forman en unión los compuestos orgánicos, así denominados porque en otro tiempo se creyó que solo los organismos vivos podían producirlos.
Sumario
Abundancia de los compuestos orgánicos
Se ha estimado que el número de hidrocarburos supera el medio millón. Hay varias razones para que este número sea tan elevado
- Los átomos de carbono pueden enlazarse consigo mismo para formar cadenas de diferente longitud.
- Es posible para los átomos contiguos de carbono compartir uno, dos o tres pares de electrones, con lo que una cadena carbonada de cierta longitud puede estar unida a números diferentes de átomos de hidrógeno.
- Cuantos más átomos contiene una molécula, más variadas son las formas en que aquellos pueden disponerse, originando compuestos de igual composición pero de diferente estructura
- Los átomos de hidrógeno son sustituibles por otros átomos o por grupos atómicos, lo que da lugar a un gran número de derivados.
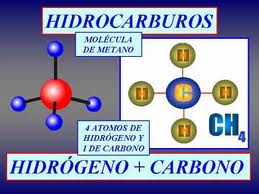
Tetravalencia del carbono
El átomo de carbono tiene cuatro electrones de valencia, por lo tanto puede formar cuatro enlaces covalentes dirigidos a los vértices de un tetraedro. Poco importa si estos enlaces van a otros átomos de carbono o a á tomos de hidrógeno, porque ambos elementos tienen casi la misma electronegatividad. Esto significa que en vez de un único hidrocarburo, el más sencillo de todos, el metano CH4 , es posible la formación de una serie de compuestos: etano (C2H6 ), propano (C3H8), butano (C4H10),etc. Sus fórmulas estructurales se suelen escribir como aparecen a continuación.
Son excelentes fuentes de hidrocarburos el gas natural y el petróleo, el primero constituido sobre todo por hidrocarburos ligeros (metano y etano en su mayor parte), y el último por hidrocarburos más pesados cuyas moléculas contienen un mínimo de 40 átomos de carbono. Dado que unos hidrocarburos difieren de otros en sus puntos de fusión es posible separarlos por destilación. A la temperatura ordinaria son químicamente inertes; pero al calentarlos, pueden arder en el aire formando óxidos de carbono (CO y CO2 y agua, y de aquí su uso como combustibles. La gasolina es una mezcla de hidrocarburos desde el heptano, C7H16, hasta el decano, C10H22 . A fin de mejorar la producción de gasolina a partir del petróleo, se rompen aquellas moléculas de más de 10 átomos de carbonos (proceso del cracking catalítico) o se juntan otras más pequeñas, con menos de siete átomos de carbono (proceso de síntesis catalítica)
Enlaces Múltiples
Los Hidrocarburos no saturados son los que poseen dobles o triples enlaces. Ejemplo de ellos son el etileno, C2H4; el acetileno C2 H2 y el butadieno, C4H6, cuyas formulas estructurales mostramos a continuación
En general son más activos que los hidrocarburos saturados, pues son capaces de sufrir reacciones de adición en las que átomos de hidrógeno o de otros elementos se unen a la molécula rompiendo los enlaces múltiples. En estas reacciones aditivas se funda la transformación de los aceites vegetales en grasas sintéticas mediante hidrogenación catalítica. Los hidrocarburos no saturados pueden experimentar reacciones de polimerización, en las que se acoplan moléculas pequeñas para formar largas cadenas. Así, el etileno se polimeriza para formar el polietileno, un plástico como se indica esquemáticamente a continuación
El doble enlace se desdobla formando un compuesto intermedio inestable que se desplaza consigo mismo para originar un polímero elevado. Esta expresión, polímero elevado se aplica a cualquier molécula grande que contenga grupos repetidos perfectamente reconocibles como tales.
Isomería
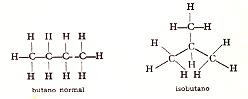
El tercer factor antes mencionado entre los que contribuyen a que haya un gran número de compuestos orgánicos es la isomería, esto es, la existencia de más de un compuesto con igual fórmula molecular. La fórmula C2H6O puede ser la del compuesto El primero de los cuales es el alcohol etílico (p.eb. =78.5 o C), y el segundo el éter dimetílico (p.eb. = -23,7 o C), de distintas propiedades en virtud de la distinta posición del átomo de oxígeno. Los compuestos que, como los dos citados, tienen igual composición, pero estructuras diferentes, se denominan isómeros. Hay numerosos ejemplos de isomería en la serie de los hidrocarburos saturados: cada miembro de ella, a partir del butano, presenta cuando menos dos isómeros (se ha calculado que el hidrocarburo C40H82 tiene unos 61 billones). En el caso del butano hay solo dos isómeros, el butano normal y el isobutano, cuyas fórmulas estructurales convencionales, en dos dimensiones son
Son estos los únicos isómeros del C4H10, aunque parezca posible la existencia de otros. Se pueden escribir otras fórmulas bidimensionales pero siempre resultan equivalentes a una de las escritas. Esto se debe a que tales fórmulas no tienen en cuenta el carácter tridimensional de las moléculas.
En un hidrocarburo saturado cada carbono está rodeado tetraédicamente por cuatro grupos, y las moléculas pueden adquirir distintas configuraciones por rotación en torno a los enlaces. Una circunstancia que hace aumentar el número de isómeros es la posibilidad de que los átomos se dispongan en anillos. El más común de estos compuestos es el benceno, C5H6, cuya molécula consta de seis átomos de carbono situada en los vértices de un hexágono, con un átomo de hidrógeno unido a cada uno de aquellos (en total, doce átomos en el mismo plano) Los enlaces carbono-carbono son todos equivalentes, por lo que la molécula debe considerarse como un hibrido de resonancia.
Derivados
La cuarta razón que abona el gran número de compuestos orgánicos existente en la formación de derivados. Estos presentan propiedades diferentes de las de los hidrocarburos que les han dado origen, y tales propiedades están determinadas principalmente por la naturaleza del sustituyente.
El radical hidrocarburo suele permanecer intacto a través de las reacciones químicas, por lo que conviene considerar a los derivados de los hidrocarburos como combinaciones de dichos radicales con los grupos sustiuyentes. Estos últimos se denominan grupos funcionales y cada uno comunica un conjunto de propiedades características a la molécula de que forma parte. Un ejemplo sencillo de grupo funcional es el grupo funcional alcohol, OH. En los alcoholes metílico (HC3OH) y etílico (C2H5OH), derivados respectivamente del metano (CH4) y del etano (C2H6), el grupo OH presta ciertas características semejantes a las del agua a lo que, sin él, era originalmente un hidrocarburo volátil pero inerte. En otros alcoholes superiores, esto es, con más átomos de carbono, el grupo OH influye menos en cuanto a provocar cambios en las propiedades.
La formula general de los alcoholes puede escribirse ROH, donde R es el radical del hidrocarburo: en el alcohol metílico, este radical es CH3; en el etílico, C2H5 reciben el nombre de alquilos. Un grupo funcional es el ácido, formado por un átomo de carbono unido a uno de oxígeno por un doble enlace y uno OH por un enlace simple. Los compuestos que contienen este grupo se denominan ácidos orgánicos, y su fórmula general es R–COOH; cuando R es CH3, el ácido acético, CH3–COOH, la constante de disociación (Kdis = 1,8 .10 -5), los demás ácidos orgánicos son generalmente electrólitos débiles. Como ácidos que son, neutralizan a las bases. Con los alcoholes dan una reacción completamente distinta, la esterificación, la cual se representa en general por la ecuación siguiente:
Donde se muestra la separación de una molécula de agua y la formación de un éter, RCOOR’. Aunque estas reacciones pueden parecer superficialmente neutralizaciones ácido-base, difieren de ellas por tres cosas:
- Son lentas pudiendo incluso requerir varias horas a elevada temperatura.
- No se producen entre los iones H+ y OH-. 3. el agua resultante está formada por el OH del ácido y el H del alcohol, como se demuestra experimentando con isótopo trazadores. Por su lentitud y porque solo intervienen partes de las moléculas (no iones), las esterificaciones son reacciones orgánicas típicas.
Los ésteres son más frecuentes en la naturaleza. Las grasas animales y los aceites vegetales son mezclas de ésteres, como la estearina (principal componente de la grasa animal).
Cuando se hierve con hidróxido de sodio, sufre la reacción llamada saponificación que descompone la molécula en un polialcohol y en una sal de ácido estéarico (estearato sódico, NaOOCC17H35, un jabón) la ecuación general de la saponificación es
RCOOR’ + OH¯ - -> RCOO¯ + R’OH
éster anión del ácido alcohol
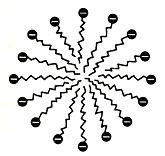
El jabón (que consideramos como estearato sódico. Aunque los hay que son sales de otros ácidos de cadenas largas)es notable porque origina aniones constituidos esencialmente por un hidrocarburo modificado en un extremo por el grupo negativamente cargado _ COO ¯ cuando se hecha el jabón en el agua, en realidad no se disuelven estos aniones, porque los hidrocarburos son insolubles en los disolventes polares. En su lugar se forman micelas, constituidas por muchos aniones estearatos unidos por sus extremos hidrocarburados. Como muestra la figura
Las cargas negativas superficiales de las micelas se disuelven en el agua, mientras que las cadenas interiores de hidrocarburos se disuelven unas en otras.
Además de las grasas hay otras dos sustancias que constituyen la base de la materia viva: los carbohidratos y las proteínas, los carbohidratos fueron así denominados porque los más corrientes se pueden formular Cx(H2 )y, es decir, que contienen átomos de hidrógeno y de oxígeno en la proporción 2:1, como el agua. sin embargo, no se trata de hidratos en modo alguno, sino que son estructuras anulares complejas en las que los átomos de carbono está unidos a otros de hidrógeno y a grupos OH. Uno de los hidrocarburos más sencillos es la glucosa, C6H12O11 que se encuentra en numerosos frutos y en la sangre de muchos animales.
La Sacarosa C12H22O11 es el azúcar de mayor importancia comercial, y su molécula está formada por dos anillos. El almidón y la celulosa son carbohidratos polímeros existentes en la naturaleza y cuyas moléculas consisten en largas cadenas formadas por anillos de glucosa unidos unos a otros por puentes de oxígeno.
Las proteínas, de complicación extremada, también son polímeros naturales. Cuando se hierven en medio ácido o básico se hidrolizan, dando lugar a unas sustancias relativamente sencillas, llamadas aminoácidos (ácidos orgánicos con el grupo amina NH2 Se han identificado unos 20 de estos aminoácidos. Todas las proteínas, tanto del pelo como de la uñas, músculos, piel, tendones, sangre, etc, se consideran como productos de condensación de numerosas moléculas de dos o más clases de estos aminoácidos.
El rasgo característico de todas las proteínas es el grupo llamado enlace peptídico la figura muestra como se forma este enlace entre dos moléculas de aminoácidos, con separación de una de agua. La polimerización pudo continuar, puesto que el grupo libre NH2 a la izquierda y el grupo libre a la derecha son susceptibles de formar nuevos enlaces. La seda y la lana son proteínas cuyas moléculas, de enorme masa molecular, están por largas cadenas polipeptídicas.
Fuentes
- Michell J. Sienko y Robert A Plane. Química. Instituto cubano del libro. 1971.