Ley de Boyle-Mariotte
| ||||
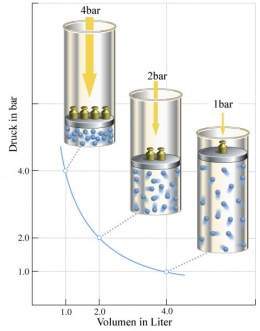
Ley de Boyle-Mariotte. La ley dice que: La presión ejercida por una fuerza física es inversamente proporcional al volumen de una masa gaseosa, siempre y cuando su temperatura se mantenga constante. O en términos más sencillos: A temperatura constante, el volumen de una masa fija de gas es inversamente proporcional a la presión que este ejerce. Matemáticamente se puede expresar así: PV = k donde k es cosntante si la temperatura y la masa del gas permanecen constantes.
Sumario
Historia
Fue descubierta por Robert Boyle en 1662. Edme Mariotte también llegó a la misma conclusión que Boyle, pero no publicó sus trabajos hasta 1676. Esta es la razón por la que en muchos libros encontramos esta ley con el nombre de Ley de Boyle y Mariotte.
La ley de Boyle establece que la presión de un gas en un recipiente cerrado es inversamente proporcional al volumen del recipiente, cuando la temperatura es constante.
La expresión matemática de la ley de Boyle indica que el producto de la presión de un gas por su volumen es constante:
PV= K
P1V1= P2V2
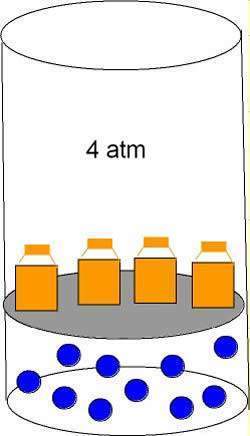
Como muestra la figura 1, Cuando se somete un gas a una presión de 4 atmósferas el volumen del gas disminuye. Por lo tanto, A mayor presión menor volumen
Figura 1. Gas sometido a presión de 4 atmosferas.
En la figura 2, se observa que cuando se disminuye la presión a 1 atmósfera, el volumen aumenta, debido a que los gases son compresibles. Por lo tanto A menor presión Mayor volumen.
Figura 2. Gas sometido a presión de 1 atmósfera.
Definición de la Ley Boyle - Mariotte
El volumen es inversamente proporcional a la presión: •Si la presión aumenta, el volumen disminuye. •Si la presión disminuye, el volumen aumenta.
¿Por qué ocurre esto?
Al aumentar el volumen, las partículas (átomos o moléculas) del gas tardan más en llegar a las paredes del recipiente y por lo tanto chocan menos veces por unidad de tiempo contra ellas. Esto significa que la presión será menor ya que ésta representa la frecuencia de choques del gas contra las paredes.
Cuando disminuye el volumen la distancia que tienen que recorrer las partículas es menor y por tanto se producen más choques en cada unidad de tiempo: aumenta la presión.
Lo que Boyle descubrió es que si la cantidad de gas y la temperatura permanecen constantes, el producto de la presión por el volumen siempre tiene el mismo valor.
Como hemos visto, la expresión matemática de esta ley es:
PV = k
(el producto de la presión por el volumen es constante)
Supongamos que tenemos un cierto volumen de gas V1 que se encuentra a una presión P1 al comienzo del experimento. Si variamos el volumen de gas hasta un nuevo valor V2, entonces la presión cambiará a P2, y se cumplirá:
P1V1 = P2V2
que es otra manera de expresar la ley de Boyle.
Ejemplo
4.0 L de un gas están a 600.0 mmHg de presión. ¿Cuál será su nuevo volumen si aumentamos la presión hasta 800.0 mmHg?
Solución: Sustituimos los valores en la ecuación P1V1 = P2V2.
(600.0 mmHg) (4.0 L) =(800.0 mmHg) (V2)
Si despejas V2 obtendrás un valor para el nuevo volumen de 3L.
Ejercicio
1. Se desea comprimir 10 litros de oxígeno, a temperatura ambiente y una presión de 30 kPa, hasta un volumen de 500 mL. ¿Qué presión en atmósferas hay que aplicar?
P1= 30 kPa (1 atm / 101.3kPa) = 0.3 atm
500 mL= 0.5L.
P1V1= P2V2
P1= 0.3 atm
V1= 10 L
V2= 0.50 L
Despejamos P2 y sustituímos.
P2= P1 (V1/V2)
P2= 0.3 atm (10L / 0.50L)= 6 atm
Experimento de Boyle
Para poder verificar su teoría introdujo un gas en un cilindro con un émbolo y comprobó las distintas presiones al bajar el émbolo. A continuación hay una tabla que muestra algunos de los resultados que obtuvo este fenómeno:
| x | p(atm) | V (L) | P.V |
|---|---|---|---|
| 0.5 | 60 | 30 | |
| 1.0 | 30 | 30 | |
| 1.5 | 20 | 30 | |
| 2.0 | 15 | 30 | |
| 2.5 | 12 | 30 | |
| 3.0 | 10 | 30 |
Si se observan los datos de la tabla se puede comprobar que al aumentar el volumen, la presión disminuye. Por ello se usa una diagonal isotérmica para representarlo en una gráfica. , aumenta y que al multiplicar y se obtiene atm·L.