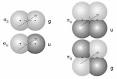
Orbitales moleculares
Orbitales moleculares que son orbitales que dejan de pertenecer a un solo núcleo para pasar a depender de dos o más núcleos. El tratamiento matemático que utiliza la Mecánica Cuántica para el cálculo de los orbitales moleculares es el método de la combinación lineal de orbitales atómicos, o método CLOA, que considera que el orbital molecular, y, es el resultado de la combinación lineal, es decir, una suma o una resta, de los dos orbitales atómicos implicados, F1y F2.
Sumario
Origen
El caso más sencillo es el de la interacción de dos átomos, cada uno con un solo orbital atómico ocupado por un único electrón, es decir, el caso ya considerado desde el punto de vista de la teoría del enlace de valencia, de la formación de la molécula de hidrógeno. Se verá que la descripción del enlace H-H es la misma, o al menos muy similar a la descripción de los enlaces en moléculas más complejas. Cuando los dos orbitales 1s de dos átomos de hidrógeno interaccionan se transforman en dos orbitales moleculares, uno enlazante, que queda ocupado por los dos electrones, que dejan de pertenecer a un solo núcleo para pasar a pertenecer a los dos núcleos atómicos, y otro antienlazante, que quedará vacío. El orbital molecular enlazante es de menor energía que los orbitales atómicos originales y el antienlazante de mayor energía que éstos. Por ello al formarse el enlace y pasar los electrones al orbital molecular enlazante se desprende una determinada energía que es la que se ha definido en la teoría del enlace de valencia como energía de disociación de enlace.
El orbital enlazante, yE, es el resultado de la suma, F1+ F2, de los dos orbitales atómicos: Los orbitales moleculares son funciones matemáticas que definen el comportamiento ondulatorio de los electrones dentro de las moléculas, siempre bajo el punto de vista de la química cuántica. Las funciones matemáticas se usan para hallar las propiedades fisicoquímicas, como por ejemplo, la probabilidad de encontrar al electrón en un espacio determinado. La palabra orbital se utilizó por Robert S. Mulliken por primera vez en1925, siendo la traducción de la palabra “ Eigenfunktion”, utilizada por el alemán Schrödinger. Los orbitales moleculares, están formados generalmente por un conjunto lineal de orbitales atómicos, en cada átomo de una molécula. La forma cuantitativa se puede hallar utilizando métodos como el conocido como Hartree-Fock.
Los orbitales moleculares se usan para determinar la configuración electrónica en las moléculas. Casi todos los métodos en química cuántica inician calculando los orbitales moleculares, para de este modo describir el comportamiento que tiene un electrón en el campo eléctrico que crean los núcleos entorno a sí mismos. Si dos electrones se encuentran en el mismo orbital, éstos están obligados a tener spines opuestos según el principio de exclusión de Pauli.
Clasificación
- Enlazantes: tienen menor energía que la que poseen los orbitales atómicos que contribuyeron a su formación. Colaboran en el enlace de manera que los núcleos positivos vencen las fuerzas electrostáticas de repulsión debido a la atracción que crea la nube electrónica negativa, entre ambos hay una distancia que se conoce como, longitud de enlace.
- Antienlazantes: Poseen mayor energía y por es por ello, crean repulsión, al contrario que los enlazantes.
Los tipos de orbitales son
- Orbitales σ enlazantes: Son los orbitales atómicos s y p, que se combinan entre sí de todas las maneras posibles ( s-s, p-p, s-p, p-s). Poseen enlaces sencillos
- Orbitales π enlazantes: Son aquellos que coordinan los orbitales atómicos p, perpendiculares al eje. Poseen electrones muy deslocalizados que interaccionan con gran facilidad.
- Orbitales σ* antienlazantes: se tratan de orbitales de mayor energía que en los orbitales enlazantes. Orbitales π* antienlazantes: Se trata de orbitales π de gran energía.
- Orbitales n: Se producen en moléculas heteroatómicas, como por ejemplo, el N o el O. Los electrones que se encuentran desapareados ocupan estos orbitales.
De igual manera que los orbitales atómicos, los orbitales moleculares se llenan de electrones, por orden creciente del nivel de energía, según el principio de exclusión de Pauli, o aplicando la regla de Hund.
Teoría de orbitale smoleculares
La teoría de los orbitales moleculares aplicada a la molécula de hidrógeno es relativamente sencilla por estar implicados solamente dos orbitales atómicos s y únicamente dos electrones. Pero en las moléculas poliatómicas con más de dos núcleos y varios orbitales atómicos, el tratamiento es mucho más complicado, pues, para llegar a conocer con exactitud la situación más estable del conjunto de los átomos de la molécula, habría que considerar orbitales moleculares que comprendieran a más de dos núcleos o, incluso, a la molécula entera.
Para obviar el estudio de una situación tan compleja, sobre todo desde el punto de vista matemático, se utilizan y admiten ciertas simplificaciones como la consideración de que, en general, los orbitales moleculares se localizan esencialmente entre dos únicos núcleos y que su forma y orientación mantienen cierta similitud con la forma y orientación de los correspondientes orbitales atómicos. Esta aproximación coincide con las ideas clásicas de considerar cada enlace como la fuerza de unión entre dos átomos, despreciando la influencia que el resto de la molécula pueda ejercer sobre el mismo. Con estas simplificaciones se pueden interpretar la mayoría de las moléculas, aunque no todas, y aproximarse a la interpretación que del enlace covalente da la teoría del enlace de valencia.
Orbitales moleculares S
El orbital molecular enlazante descrito para la molécula de hidrógeno, que tiene forma elipsoidal (simétrico respecto al eje de unión de los dos núcleos), recibe el nombre de orbital molecular s(sigma) y el enlace covalente resultante, enlaces. Análogamente el orbital molecular antienlazante correspondiente recibe el nombre de orbitals* (sigma estrella o sigma asterisco). Por solapamiento o interacción de dos orbitales atómicos de tipo s se forman siempre orbitales moleculares de tipo s. Pero también a partir de orbitales p se pueden formar orbitales y enlaces s. Así, por ejemplo, cuando un orbital p interacciona con un orbital s se llega a sendos orbitales moleculares s, uno enlazante:
Como en el caso de la combinación de dos orbitales s, en el orbital enlazante formado a partir de un orbital s y otro p, debido a la sensible disminución que experimenta el lóbulo no implicado en el solapamiento del orbital p, la mayor densidad electrónica se encuentra entre los dos núcleos y el orbital molecular resultante tiene prácticamente simetría elipsoidal respecto al eje que une los dos núcleos. Se trata pues de un orbital molecular s similar al de la molécula de hidrógeno.
Orbitales moleculares p
Pero a partir de dos orbitales atómicos p puede originarse otro tipo de orbitales moleculares. En efecto, el solapamiento o interacción entre los dos orbitales atómicos p puede tener lugar lateralmente para dar lugar a dos orbitales moleculares del tipo p(pi), uno enlazante, de menor energía que los atómicos de partida, y otro antienlazante, de mayor energía y con un nodo: Como los orbitales atómicos de partida, los orbitales moleculares de tipo p también poseen zonas de distinto signo separadas por un plano nodal. El orbital molecular p enlazante está formado por dos lóbulos de distinto signo en los que la probabilidad de encontrar a los electrones es máxima, separados por un plano nodal que pasa por los dos núcleos. Es decir, en el orbital enlazante, los dos núcleos de los átomos que aportan los orbitales p quedan unidos por dos zonas o nubes p, una superior y otra inferior de distinto signo. En el orbital antienlazante, las zonas nodales son dos, la del plano que pasa por los dos núcleos y la de un plano perpendicular al primero que hace que las zonas superior e inferior queden divididas a su vez en dos partes de distinto signo:
Electrones moleculares
Ya hemos visto que la manera "localizada" de describir los enlaces en base a electrones dirigidos hacia sitios específicos según la geometría de la molécula, es de gran utilidad para disponer de una interpretación de los enlaces. Sin embargo, existen algunos problemas que se arreglan mediante el uso de la Teoría de los Orbitales Moleculares , OM. Esta última difiere del tratamiento en base a Orbitales Híbridos en varios aspectos, el principal se refiere a que los Híbridos se construyen para mostrar la formación de enlaces " dirigidos", a diferencia de los OM que son más generales en su planteamiento para describir la configuración electrónica en moléculas. Permiten corregir varias dificultades presentes en los híbridos, como ser :
Los híbridos suponen que los e's son locales en los enlaces, lo cual no es totalmente correcto. Mas bien, lo que existe es una posibilidad alta que carga electrónica se ubique en la dirección de los enlaces, no descartando que también pueda ocupar otras regiones de la molécula. Esta anomalía es corregible mediante las llamadas " estructuras de resonancia" como ya se ha visto.
Para formar enlaces con participación de híbridos, es necesario disponer de pares de electrones , compartidos o no, para dirigirlos hacia posiciones específicas de la geometría de las moléculas. Pero , ¿Qué ocurre en las moléculas que presentan electrones no apareado?. Esta situación no la contempla el esquema de híbridos moleculares.
La Energía de Enlace tampoco es un concepto que aparece en los híbridos, en circunstancias que sabemos que hay enlaces más difíciles de romper que otros.
Enlaces externos
Fuente
1- LAIDLER. "Cinética de reacciones". Vol. 1 y 2. Editorial Alhambra.
2.- LEVINE, BERNSTEIN. "Molecular reaction dynarnics and chemical reactivity", Editorial Oxford University Press.
3.- GONZALEZ UREÑA. "Cinética y dinámica molecular de las reacciones químicas elementales. Editorial Albambra.
4.- LEVINE. "Fisicoquírnica". Vol. 2, capítulos 17 y 23. Editorial McGraw Hill.
5.- AVERY. "Cinética química básica y mecanismos de reacción". Editorial Reverté.
6.- SENENT PEREZ. "Química Física H". Vol 1, 2 y 3. Editorial UNED.