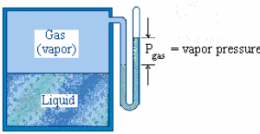
Presión de vapor
| ||||||
La Presión de vapor o más comúnmente presión de saturación es la presión a la que a cada temperatura las fases líquida y vapor se encuentran en equilibrio; su valor es independiente de las cantidades de líquido y vapor presentes mientras existan ambas. En la situación de equilibrio, las fases reciben la denominación de líquido saturado y vapor saturado.
Sumario
Introducción
Todos los sólidos ylíquidos producen vapores consistentes en átomos o moléculas que se han evaporado de sus formas condensadas. Si la sustancia, sólida o líquida, ocupa una parte de un recipiente cerrado, las moléculas que escapan no se pueden difundir ilimitadamente sino que se acumulan en el espacio libre por encima de la superficie del sólido o el líquido, y se establece un equilibrio dinámico entre los átomos y las moléculas que escapan del líquido o sólido y las que vuelven a él. La presión correspondiente a este equilibrio es la presión de vapor y depende sólo dela naturaleza del líquido o el sólido y de la temperatura. Se sabe que el agua no hierve a presión atmosférica y temperatura ambiente; sin embargo, cuando es calentada a 100 °C se presenta este fenómeno. Esto se debe a que la presión de vapor del agua a 100 °C es la presión atmosférica.
Cualquier líquido en un recipiente abierto, hierve cuando es calentado a un nivel tal que su presión de vapor es la presión atmosférica. Inversamente, un líquido no hierve mientras que su presión de vapor es menor que dicha presión. De este modo, si la presión de vapor del aceite crudo en un tanque es menor que la presión atmosférica, no se presenta evaporación.
Factores de que depende la Presión de vapor
- La naturaleza del líquido
- La temperatura
Influencia de la naturaleza del líquido
El valor de la presión de vapor saturado de un líquido, da una idea clara de su volatilidad, los líquidos mas volátiles (éter, gasolina, acetona etc) tienen una presión de vapor saturado mas alta, por lo que este tipo de líquidos, confinados en un recipiente cerrado, mantendrán a la misma temperatura, un presión mayor que otros menos volátiles. Eso explica porqué, a temperatura ambiente en verano, cuando destapamos un recipiente con gasolina, notamos que hay una presión considerable en el interior, mientras que si el líquido es por ejemplo; agua, cuya presión de vapor saturado es mas baja, apenas lo notamos cuando se destapa el recipiente. Si un soluto es no volátil la presión de vapor de su disolución es menor que la del disolvente puro. Así que la relación entre la presión de vapor y presión de vapor del disolvente depende de la concentración del soluto en la disolución. Esta relación está dada por la ley de Raoult, (un científico francés, Francois Raoult ), que establece que la presión parcial de un disolvente sobre una disolución está dada por la presión de vapor del disolvente puro, multiplicada por la fracción molar del disolvente en la disolución.
El cálculo de la presión se realiza mediante la fórmula que se muestra a la derecha.
Influencia de la temperatura
La presión de vapor en los líquidos crece rápidamente al aumentar la temperatura; así, cuando la presión de vapor es igual a 1 atmósfera, el líquido se encuentra en su punto de ebullición ya que el vapor, al vencer la presión exterior, se puede formar en toda la masa del líquido y no sólo en su superficie. La relación entre la temperatura y la presión de vapor saturado de las sustancias, no es una linea recta,en otras palabras, si se duplica la temperatura, no necesariamente se duplicará la presión, pero si se cumplirá siempre, que para cada valor de temperatura, habrá un valor fijo de presión de vapor saturado para cada líquido. La explicación de este fenómeno se basa en el aumento de energía de la moléculas al calentarse. Cuando un líquido se calienta, estamos suministrándole energía. Esta energía se traduce en aumento de velocidad de las moléculas que lo componen, lo que a su vez significa, que los choques entre ellas serán mas frecuentes y violentos. Es fácil darse cuenta entonces, que la cantidad de moléculas que alcanzarán suficiente velocidad para pasar al estado gaseoso será mucho mayor, y por tanto mayor también la presión.
Expresiones para relacionarla con la temperatura
La regla de fases establece que la presión del vapor de un líquido puro es función única de la temperatura de saturación. Pues la presión de vapor en la mayoría de los casos se puede expresar como.
Pvp= f (t)
La presión de vapor de un liquido se relaciona con la temperatura por medio de la Ecuación de Clausius-Clapeyron, sin embargo existen muchas ecuaciones que estudian esta propiedad de los fluidos, pero de todas maneras estas ecuaciones pueden referirse a la ecuación de Clapeyron:
Ln*P2/P1= (DH/R) vaporización (1/T1-1/T2)
Esta ecuación mediante pasos matemáticos, puede convertirse en:
LnPvp = A+B/T
se debe tener en cuenta que esta ecuación no es aplicable a temperaturas inferiores al punto de ebullición normal.
Estimación de la presión del vapor
En intervalos de baja presión: 10 a 1500 mmHg
- El método de estimación de Frost-Kalkwarf-Thodors, es el mejor para compuestos orgánicos, el cual se hace por medio de Cálculos de tipo iterativo, y arroja un máximo porcentaje de error medio de 5.1%.
- El método de Riedel-Plank-Miller es el mejor para compuestos inorgánicos y además es fácil de usar, este arroja un máximo porcentaje de error medio de 5.2%
En intervalos de alta presión: 1500 mmHg hasta la presión critica
- El método de estimación reducida de Kirchhoff, el cual no es muy exacto pero es muy fácil de usar, este arroja un máximo porcentaje de error medio de 3.2%
- El método de estimación de Frost-Kalkwarf-Thodors, para intervalos de alta presión también requiere de cálculos iterativos, sin embargo es muy bueno y arroja un máximo porcentaje de error medio de 1.5%.
Estos métodos anteriores son métodos trabajados con ecuaciones reducidas para los cuales era necesario conocer tc, pc, tb.. pero existen muchísimos método diferentes tanto con ecuaciones reducidas como con ecuaciones semirreducidas y sin reducir.
Uso de la presión de vapor
Las plantas productoras de petroquímicos y refinerías, requieren de muchos servicios como: vapor de agua (enfriamiento, servicio, proceso), aire de instrumentos, energía eléctrica; para ello estas plantas necesitan grandes sistemas de transformación de energía, y redes de distribución de varios kilómetros, en las cuales se incurre en perdidas de energía. Para lo que es necesario usar expresiones matemáticas para calcular dichas perdidas y llevar a cabo estudios sobre la recuperación de la inversión y la rentabilidad de acciones de ahorro de energía.
En la generación del vapor las plantas que lo generan, están formadas por dos o tres niveles de presión, los cuales son distribuidos según su uso o según la magnitud de la presión del vapor, de esta forma: para los bloques de generación eléctrica, turbinas para accionar bombas y compresores de plantas de procesos se usa el vapor de mayor presión; para turbogeneradores eléctricos y grandes turbocompresores, se usa por lo general extracciones de vapor media; las turbinas de menor capacidad normalmente descargan a la red de baja presión.
El control de la presión y la temperatura en las redes de distribución de vapor es sumamente importante, ya que excesos de estas presiones pueden causar un desgaste mas acelerado de la tubería y aparte de esto se pueden generar muchas perdidas de energía, lo cual no es conveniente para un proceso en el cual se esta tratando de aprovechar la energía al máximo.
Para controlar estos excesos o simplemente variantes de las presiones y temperaturas adecuadas se tienen controles de los generadores de vapor los cuales mantienen estos factores en los valores ajustados, esta regulación también se lleva a cabo durante todo el proceso ya que en las redes de media y baja presión, también se cuenta con reguladores de presión y temperatura en turbinas y otros aparatos que intervienen en este.
Para mantener el control en los sistemas de distribución de vapor, es necesario llevar una buena administración y una constante revisión de toda la red, a su ves mediante los dato recolectado durante las revisiones periódicas es necesario estar calculando las perdidas de energía ya que estas afecten directamente la eficiencia del proceso, por ultimo es necesario determinar los puntos de ajuste adecuados para la red. También es necesario analizar la posibilidad de operar la red a la menor presión posible para lo cual seria necesario consultar a los fabricantes de las turbinas y determinar si la tubería podría transportar los volúmenes necesarios.
Fuentes
- REID,Robert C y SHERWOOD, Thomas K. propiedades de los gases y líquidos.
Unión tipográfica editorial hispano-americana. México.1968.