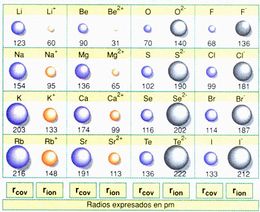
Radio iónico
| ||||||
El Radio iónico , como el propio nombre lo indica, se refiere al valor designado para el radio de un ión en un sólido cristalino, basado en el presupuesto de que los iones poseen una forma esférica.
Sumario
Efectos
Al igual que el radio atómico, la distancia entre el centro del núcleo del átomo y el electrón estable más alejado del mismo, pero haciendo referencia no al átomo, sino al ion. Éste aumenta en la tabla de derecha a izquierda por los períodos y de arriba hacia abajo en los grupos.
En el caso de los cationes, la ausencia de uno o varios electrones disminuye la fuerza eléctrica de repulsión mutua entre los electrones restantes, provocando el acercamiento de los mismos entre sí y al núcleo positivo del átomo del que resulta un radio iónico menor que el atómico. En el caso de los aniones, el fenómeno es el contrario, el exceso de carga eléctrica negativa obliga a los electrones a alejarse unos de otros para restablecer el equilibrio de fuerzas eléctricas, de modo que el radio iónico es mayor que el atómico.
Los radios iónicos están relacionados siempre con los atómicos de la siguiente manera: los iones negativos son más grandes que un átomo normal y los iones positivos mas pequeños. Así, si el yodo es más grande que el bromo en estado normal sus iones de igual carga también lo serán. Si dos iones no tienen la misma carga pero si la misma estructura electrónica el radio más grande será para el átomo del elemento con menor número atómico.
Que el elemento gane electrones
El electrón o electrones ganados se colocan en los orbitales vacíos, transformando el átomo en un anión. La ganancia de electrones por un átomo no metálico aislado es acompañada por un aumento de tamaño.
Por ejemplo los halógenos, situados en el grupo 17, presentan una configuración electrónica en su último nivel, igual a ns2p5 , por tanto pueden acercar un electrón a su último nivel para adquirir la configuración electrónica de un gas noble, ns2p6 con lo que el elemento gana estabilidad y se transforma en un anión (ion con carga negativa).
Al comparar el valor del radio atómico de cualquier elemento con el de su anión, éste es siempre mayor, debido a que la carga nuclear es constante en ambos casos, mientras que al aumentar el número de electrones en la capa mas externa, también aumenta la repulsión entre los mismos aumentando de tamaño el orbital correspondiente y por tanto también su radio iónico.
Que el elemento pierda electrones
Generalmente se pierden los electrones de valencia y el elemento se transforma en un catión. La pérdida de electrones por un átomo metálico aislado implica una disminución de su tamaño. Por ejemplo, los metales alcalinotérreos (grupo 2) presentan una configuración electrónica en su último nivel igual a ns2. Cuando pierden estos dos electrones externos adquieren la configuración electrónica del gas noble que les precede en la tabla periódica, aumentando su estabilidad y tranformándose en un catión con dos cargas positivas.
El valor del radio atómico del elemento es siempre mayor que el del correspondiente catión, ya que éste ha perdido todos los electrones de su capa de valencia y su radio efectivo es ahora el del orbital n-1, que es menor.
Podemos generalizar diciendo que los iones cargados negativamente (aniones) son siempre mayores que sus correspondientes átomos neutros, aumentando su tamaño con la carga negativa; los iones positivos (cationes), sin embargo, son siempre menores que los átomos de los que derivan, disminuyendo su tamaño al aumentar al carga positiva. Entre los iones con igual número de electrones (isoelectrónicos) tiene mayor radio el de menor número atómico, pues la fuerza atractiva del núcleo es menor al ser menor su carga.
Fuentes
- Química general -Libro de Ralph H. Petrucci
- Lic. Irene Vera, Maria: Química General, Unidad III: Distribución de electrones en los átomos. Disponible en: [http://exa.unne.edu.ar/quimica/quimgeneral/UnidadIIINumerosCuanticos.pdf
- Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
- León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985