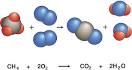
Ecuación química
| ||||||
Ecuación Química. Es una forma esquemática y sencilla de expresar, mediante símbolos y fórmulas, los cambios ocurridos en el transcurso de una reacción.
Sumario
Partes de una ecuación química
Sustancias reaccionantes o reactivos
Son las sustancias que reaccionan. Están colocadas antes de la flecha o el signo igual a.
Sustancias productos
Son las sustancias que se forman. Están colocadas después de la flecha o el signo igual a (=). Los científicos suelen representar las reacciones químicas mediante símbolos y fórmulas de las sustancias que intervienen y se producen.
- El símbolo "+" : entre las sustancias reaccionantes se lee como "reacciona con", entre las sustancias productos se lee como "y".
- La flecha o el signo igual a: separa a las sustancias reaccionantes de las sustancias productos. Se lee "produce".
- Un triángulo sobre la flecha o el signo igual a: significa "calor". Los reactivos deben calentarse para que la reacción se efectúe.
- Algunas veces, la ecuación muestra el estado de agregación de las sustancias que participan, indicando una letra minúscula entre paréntesis, después de cada sustancia:(s): sólido (l): líquido (g): gas, para la sustancia en disolución se usa el símbolo (ac) que significa acuoso.
- Coeficientes: Son los números colocados antes de cada sustancia. Indican el número de moles que reaccionan de cada reactivo y el número de moles que se forman de cada producto. Esto se hace siempre debido a la Ley de Conservación de la masa.
Se acostumbra a omitir el número 1. Esta operación se llama ajuste de la ecuación química. Nunca se debe de modificar los subíndices de las fórmulas. Siempre que esté ajustada una ecuación se coloca un signo de igualdad, si se pone una flecha no evidencia el cumplimiento de la Ley de Conservación de la masa.
Ajuste o balanceo
Ajustar o balancear una ecuación química es igualar el número y clase de partículas (átomos, moléculas o inoes) reaccionantes con los productos, con la finalidad de cumplir la Ley de Conservación de la masa.
Para ajustar o balancear una ecuación química, se debe considerar lo siguiente:
- Conocer las sustancias reaccionantes y productos.
- Revisar que la ecuación esté completa y escrita correctamente.
- Verificar si la ecuación se encuentra ya ajustada.
- Los subíndices indican la cantidad del átomo indicado en la molécula.
- Los coeficientes afectan a toda la sustancia que preceden.
- Se comienza ajustar por el elemento metálico, luego el no metal(excepto Oxígeno e Hidrógeno.
- El Hidrógeno y el Oxígeno se equilibran al final y en ese orden, porque generalmente forman agua (sustancia de relleno). Esto no altera la ecuación, porque toda reacción se realiza en solución acuosa o produce sustancias que contienen agua de cristalización.
- Usar números enteros y los menores posibles para balancear.
- Escribir el número como coeficiente de la fórmula pertinente; cuando el coeficiente es (1) no se escribe, se sobreentiende.
- No se deben cambiar los subíndices de las fórmulas, ni dividir la fórmula para colocar el coeficiente en medio de ella.
- Contar el número de átomos multiplicando el coeficiente por los respectivos subíndices de las fórmulas y sumando todos los átomos de un elemento que estén de un mismo lado de la ecuación.
- Verificar el balanceo final y reajustar, si es necesario.
Métodos para ajustar (Balancear) Ecuaciones
Existen diferentes métodos que se utilizan según convengan, de acuerdo al tipo de reacción, las cuales pueden ocurrir:
- Sin cambio de estados de oxidación en ningún elemento reaccionante:
- Ensayo y Error o Tanteo.
- Mínimo Común Múltiplo.
- Coeficientes Indeterminados o Algebraico.
- Algunos elementos cambian su valencia:
- Redox.
- Ion Electrón o Semirreacción: En medio ácido y básico.
Ajuste por Tanteo
Como su nombre lo indica, es una manera de ajustar una ecuación química buscando por tanteo. Se emplea para balancear ecuaciones sencillas. Se realiza al "cálculo" tratando de igualar ambos miembros. Para ello utilizaremos el siguiente ejemplo:
Ajustar la ecuación: Al(OH)3(ac) + H2SO4(ac) = Al2(SO4)3(ac)+ H2O
- Ajustamos el metal aluminio
- Seguimos con el no metal azufre
- Continuamos con el hidrógeno y el oxígeno
Ecuación ajustada: 2Al(OH)3(ac) + 3H2SO4(ac) = Al2(SO4)3(ac) + 6H2O
Interpretación de una ecuación química
Existen dos puntos de vista o criterios a la hora de interpretar una ecuación química. Estas interpretaciones reciben el nombre de Cualtativa y Cuantitativa.
Cualitativa
Desde el punto de vista cualitativo, expresan la naturaleza de las sustancias que reaccionan y se producen.
Cuantitativa
Desde el punto de vista cuantitativo, expresan la relación entre el número de partículas (átomos, moléculas, iones) que intervienen en una reacción química.
Enlaces externos
Fuentes
- Química Web Ecuación Química
- Adolfo PonJuan y Blanco. Química Inorgánica Tomo I.
- Hutchinson, E. Química.
- León, R. Química General Superior.