Enlace químico
| ||||||
Sumario
Historia
ez de la masa de los constituyentes, y en especial del electrón, hace que solamente les sea aplicable la mecánica cuántica y, por tanto, la descripción matemática del enlace es generalmente complicada. La teoría cuántica del enlace es la base de la teoría moderna de la valencia.
Definición de enlace químico
Características principales del enlace químico
En cualquier sustancia, independientemente del tipo de partículas que la constituyan, átomos, moléculas o iones, hay varios parámetros que permiten caracterizar su estructura, de forma tal que coincida ésta en muchos casos pueden predecirse con gran certeza sus propiedades. Los parámetros fundamentales del enlace químico los constituyen la longitud o distancia, la solidez o energía de enlace y la dirección o ángulo del mismo. [[Image:Energ en el nitrogeno.JPG|thumb|left|151x101px
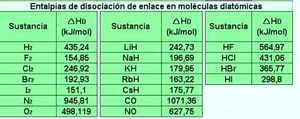
Energía de enlace
Usualmente la energía del enlace viene dada en Kj.mol1 de enlace rotos, o sea, que para disociar en átomos al estado gaseoso,Un mol de moléculas de hidrógeno, es decir para romper 6,02.1023enlaces se requieren 435, 2 Kj.
Entre los haluros de hidrógeno el valor de la
Energía de enlace en moléculas poliatómicas
En las moléculas poliatómicas
– De un solo tipo de enlace:
por ejemplo en moléculas ABn, la energía media de enlace es igual a 1/n de la energía total requerida en la disociación completa de un mol del compuesto con formación de un atg. De A y n atg. De B.
- En moléculas poliatómicas en que existen más de un enlace,
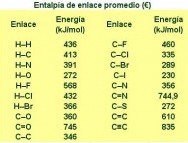
es posible caracterizar cada enlace, por una entalpía de enlace promedio (ε), que es la energía aproximada que se necesita para romper el enlace en cualquier compuesto en el cual existe dicho enlace. La disociación puede referirse a la división de una molécula:
A. En un átomo y un radical:
H2O(g) = H(g) + OH(g) ε = 497 Kj.mol-1 (1)
B. En dos radicales &nb
sp;
H2O2 (g) = OH(g) + OH(g) ε =201Kj.mol-1 (2)
También puede ocurrir la ruptura de un enlace entre dos átomos dados, pero en diferentes compuestos, y es interesante observar el efecto sobre la energía de enlace, de las diferentes agrupaciones próximas al enlace. Se conoce que el ε (H-OH) = 497 Kj.mol-1, y otros experimentos muestran que
OH(g) = O(g) + H(g) ε (O-H) = 462,9 Kj.mol-1 (3)
HOOH = HOO(g) + H(g) ε (HOO-H) = 497 Kj.-1 (4)
Al observar las ecuaciones (1)
, (3), y (4), estas se refieren a la ruptura de un mismo enlace (O-H) y es claro que la diferencia entre los tres valores se debe, no a los átomos enlazados, sino a las diferentes estructuras de las agrupaciones próximas al enlace. Eso no obstante, las diferencias en los valores, no son muy grandes en los 3 casos. Cada enlace en cada molécula tiene su propia energía de disociación de enlace específica. Por ello no es sorprendente que los enlaces entre los mismos tipo de átomos tengan usualmente energía de disociación similar. Por ejemplo, los enlaces Carbono-carbono (C-C) tienen un valor de de aproximadamente 350-380 kJ.mol-1 independiente de la estructura exacta de la molécula. Igual sucede en una serie de enlaces C-H.
CH4(g) = CH3(g) + H(g) ε (H-CH3) = 431.055Kj.mol-1
CH3CH3(g) = H3CH2(g) + H(g) ε (H-C2H5) = 361.760 Kj.mol-1
(CH3)3(g) = (CH3)3C(g) + H(g) ε (H-C-(CH3)3 = 336.650 Kj.mol-1
Es evidente que todos los valores aun cuando diferentes se encuentran entre 336,650 y 431,055 Kj.mol</sup>-1</sup> y la constante aproximada de estas energías, es muy significativa ya que sugiere que el factor principal para determinara la energía de un enlace particular, es la naturaleza de los átomos enlazados y en menor extensión las estructuras de las agrupaciones próximas al enlace. Debido a que enlaces similares tienen energía de disociación similares, es posible construir una tabla de valores promedios que permite comparar diferentes clases de enlaces. Hay que tener en cuanta no obstante que el valor real en una molécula específic
Ejemplo
3(H(g) + C(g)) + Cl(g) = CH3-Cl(g).
El signo menos en las entalpías de enlace promedio se relaciona con el hecho de que la formación del enlace libera energía.
La importancia de los valores de las energías de formación o de disociación de los enlaces, se debe a que pueden relacionarse con la fortaleza o solidez del enlace.
Un enlace es tanto más fuerte, cuanto mayor es la energía que se libera en su formación: aunque no es solo el factor energía de enlace entre dos átomos.
En moléculas poliatómicas, en que existen más de un enlace, el análisis de la energía de cada enlace se complica por la influencia de los otros átomos y enlaces en la molécula.
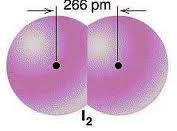
Longitud o distancia de enlace
Ángulo de enlace
Como quiera que los átomos están en constante movimiento de vibración, los ángulos de enlace no tienen valores definidos al igual que no lo tienen las distancias de enlace.
Sin embargo, si tiene un valor definido el ángulo medio según el cual tres átomos vibran y este valor corresponde a la magnitud del denominado ‘ángulo de enlace.
En realidad para poder hablar de ángulos de enlace se requieren tres átomos, uno de los cuales constituye el vértice de dicho ángulo.
Los ángulos de enlace no son del todo invariables, sino que pueden sufrir ligeras deformaciones (hasta unos 10 grados) según varíen los requerimientos espaciales de los sustituyentes unidos al átomo central.

Tipos principales de enlace químicos y su relación con la posición en el sistema periódico de los elementos que lo forman
- el enlace Iónico
- el enlace Covalente
- el enlace Metálico o enlace entre los átomos de los elementos metálicos.
Referencias
- Blanco Prieto,J y J. Periera Simo: Química Inorgánica Parte I. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1986.
- Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Materiales Complementarios de Química para Ingenieros. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
- León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985.
- León, R: Química General Superior. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
Fuentes
- http://definicion.de/ley-periodica/
- http://www.portalplanetasedna.com.ar/mendeleiev.htm
- http://www.fq.uh.cu/dpto/qf/uclv/infoLab/infoquim/asig_programs/prog.lic.quimica/temas/estruc_atom_ley_period.htm
- http://quimica-general.net16.net/ley_periodica.html
- http://www.xtec.cat/~bnavarr1/Tabla/castellano/moseley.htm
- http://es.wikipedia.org/wiki/%C3%81ngulo_de_enlace