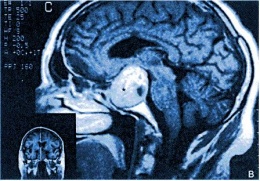
Tumores hipofisarios no funcionantes
| ||||||
Tumores hipofisarios no funcionantes. Las únicas manifestaciones endocrinas que producen son las de hipofunción por compresión del tejido hipofisario normal o una discreta hiperprolactinemia por compresión del tallo hipofisario. Estas manifestaciones endocrinas son tan leves que los tumores se presentan clínicamente por sus manifestaciones neurológicas, tras haber alcanzado el tamaño de macroadenomas extraselares.
Etiología y anatomía patológica
Algunos tumores sintetizan hormonas que pueden detectarse en el citoplasma, pero no son capaces de secretarlas o bien secretan fragmentos no detectables por los sistemas de análisis. A veces secretan activamente la subunidad a de las hormonas glucoproteicas, pero como esta subunidad no tiene acción biológica, no existen manifestaciones clínicas. Mediante técnicas de biología molecular, en alrededor del 80% de los tumores no funcionantes se puede detectar RNA mensajero de alguna de las gonadotropinas o de sus subunidades. De hecho, se ha sugerido que los tumores no funcionantes forman un continuum con los productores de gonadotropinas, que sólo se diferenciarían en la capacidad para ensamblar las subunidades y secretarlas a la circulación.
En el momento del diagnóstico suelen ser macroadenomas con un grado variable de expansión supraselar, algunos muy invasivos. Pueden presentar quistes y necrosis. Por inmunohistoquímica, en algunos casos se detectan hormonas hipofisarias intracitoplasmáticas, pero en general son gonadotropinas y un número importante presentan la subunidad a. Muy raras veces se descubren moléculas de la familia POMC y, en una proporción elevada, estos tumores corresponden a los denominados oncocitomas (null cell adenomas).
Cuadro clínico
Los tumores hipofisarios no secretores comprenden el 20-25% del total, siendo casi tan frecuentes como los secretores de GH y sólo superados por los prolactinomas. Son más frecuentes en la década de los 40-50 años y no tienen preferencia por sexo alguno. Su incidencia es de 4,5 casos por millón y año, y su prevalencia, de 50 casos por millón.
Clínicamente suelen presentarse con manifestaciones neurológicas. Las manifestaciones endocrinológicas más comunes son grados variables de hipopituitarismo que son evidentes en el 10% de los pacientes. La discreta hiperprolactinemia por sección funcional del tallo raras veces ocasiona manifestaciones clínicas en el varón y se presenta como galactorrea en la mujer. En ocasiones, la presentación clínica es debida a una hemorragia súbita en un tumor previamente desconocido. Ocasionalmente, pueden presentarse como hipotiroidismo secundario o como fracaso suprarrenal agudo en una situación de estrés.
Diagnóstico
Ante la sospecha de un tumor hipofisario no secretor debe realizarse la exploración por técnicas de imagen. La RM muestra, en la mayoría de los casos, un macroadenoma con afección variable de los tejidos próximos y áreas de necrosis frecuentes. No se observan elevaciones bioquímicas de las hormonas hipofisarias, con excepción de un leve aumento de la PRL en el 50% de los pacientes. Es muy frecuente la disminución de las concentraciones de gonadotropinas, testosterona y otras hormonas hipofisarias. En el 10-20% de los casos se detectan concentraciones elevadas de la subunidad a, dato muy útil para el seguimiento ulterior del paciente tratado.
El diagnóstico diferencial con otros tumores hipofisarios puede realizarse por la ausencia de clínica sugestiva y de hipersecreción hormonal. Estos tumores se diferencian de los prolactinomas por la presencia de concentraciones moderadamente elevadas de PRL con respecto a la masa tumoral, que se reducen muy rápidamente tras tratamiento con bromocriptina, sin que se modifique prácticamente el tamaño tumoral.
Tratamiento
El tratamiento de elección es la resección quirúrgica del adenoma por vía transesfenoidal, incluso en algunos casos que presentan extensión supraselar. Dejados a su evolución espontánea, estos tumores crecen con mucha lentitud, por lo que en pacientes de edad avanzada o con riesgo operatorio una actitud expectante puede ser la apropiada. Tras la cirugía, la recidiva es muy frecuente, por lo cual los pacientes deben ser sometidos a radioterapia.
En el 10% de los pacientes, la bromocriptina induce una ligera reducción del tumor o puede estabilizar su crecimiento, por lo que este fármaco puede ser una alternativa en pacientes que no son candidatos a la cirugía. En adenomas con receptores de somatostatina se han comunicado efectos beneficiosos tras el tratamiento con lanreótido u otros análogos de esta hormona. Este tratamiento no reduce de forma evidente el tumor, pero sí puede descomprimir el quiasma óptico. Tras la terapia quirúrgica, la mayoría de estos pacientes requiere tratamiento continuado de sustitución hormonal en relación con el déficit hipofisario.
Fuente
- Ciril Ferreras Rozman, Medicina Interna, Ediciones Harcourt, 14 Edición, 2000.
- Chandrasekharappa SC, Guru SC, Manickam P, Olifemi S-E, Collins P, Emmert-Buck MR et al. Positional cloning of the gene for multiple endocrine neoplasia-Type 1. Science 1997; 276:404-407.
- Gagel RF, Tashjian AH, Cummings T, Papathanasopoulos N, Kaplan MM, De Lellis RA et al. The clinical outcome of prospective screening for multiple endocrine neoplasia type 2s. N Engl J Med 1988; 318: 478-484.
- Marsh DJ, Mulligan LM, Eng CH. RETProto-oncogene mutations in Multiple Endocrine Neoplasia Type 2 and Medullary thyroid carcinoma. Horm Res 1997; 47:168-178.