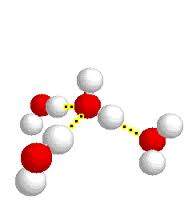
Enlace por puente de hidrógeno
Enlace por puente de hidrógeno: Es una atracción que existe entre un átomo dehidrógeno (carga positiva) con un átomo pequeño muy electronegativo, como flúor(F), oxígeno (O) o nitrógeno (N) ( F-H, O-H, N-H ), que posee un par de electrones libres (carga negativa), de ahí el nombre de "enlace de hidrógeno", que no debe confundirse con un enlace covalente a átomos de hidrógeno). Un puente de hidrógeno es en realidad una atracción dipolo-dipolo entre moléculas que contienen esos tres tipos de uniones polares.
Este tipo de atracción tiene solamente una tercera parte de la fuerza de los enlaces covalentes, pero tiene importantes efectos sobre las propiedades de las sustancias en que se presentan, especialmente en cuanto a puntos de fusión y ebullición en estructuras de cristal.[1]
Sumario
Historia
En su libro The Nature of the Chemical Bond (en español: La Naturaleza del Enlace Químico), Linus Pauling concede los créditos a T.S. Moore y T.F. Winmill de la primera mención del enlace de hidrógeno, en 1912.
Postuló a partir de observaciones de las transiciones moleculares (i.e. el movimiento de los átomos con respecto a aquellos a los que están unidos) de los átomos participantes en la molécula D2O (el deuterio forma parte de la pléyade de Hidrógeno), que el puente de Hidrógeno es la interacción más importante que juega un papel crítico no solo en la estructura del agua sino en la estructura y función de las macromoléculas biológicas.
Moore y Winmill usaron el enlace de hidrógeno para justificar el hecho que el hidróxido de trimetilamonio es una base más débil que el hidróxido de tetrametilamonio. La descripción del enlace de hidrógeno en su forma más conocida, en el agua, vino algunos años después, en 1920, por Latimer y Rodebush (JACS, 42, 1419). .
Enlace
Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados entre átomos pequeños muy electronegativos, cuando un átomo de Hidrógeno está unido covalentemente, a un átomo electronegativo, Oxígeno, Nitrógeno o Flúor, el átomo con mayor electronegatividad atraerá hacia si los electrones del enlace, formándose un dipolo negativo, mientras que el átomo de hidrógeno, al ceder parcialmente sus electrones, genera un dipolo de carga positiva en su entorno. Estas cargas opuestas se atraen. Esta deficiencia parcial en electrones, hace a los átomos de Hidrógeno susceptibles de atracción por los electrones no compartidos en los átomos de Oxígeno, Nitrógeno o Flúor.
A continuación se detallan algunos valores de la fuerza de puentes de hidrógeno: .
- F—H...F (155 kJ/mol)
- O—H...N (29 kJ/mol)
- O—H...O (21 kJ/mol)
- N—H...N (13 kJ/mol)
- N—H...O (8 kJ/mol)
- HO—H...:OH3+ (18 kJ/mol) .
El puente de Hidrógeno es un caso especial de la interacción dipolo-dipolo, es relativamente débil entre -20 y -30 kJ mol -1la fuerza de enlace aumenta al aumentar la electronegatividad y disminuye con el tamaño de los átomos participantes.
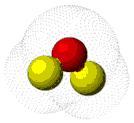
[2] En el caso del oxígeno, con un total de 8 electrones, se presentan DOS pares de electrones solitarios, tanto en el caso de la hibridación sp3 como de la sp2:
| Sin hibridar | 1s22s22p2x2p1y2p1z | Agua | |
|---|---|---|---|
| 1s22sp22sp12sp1 | 
|
| |
| Hibridación sp2 | 1s22sp22sp12p1z |
Los dos pares de electrones solitarios se muestran en rojo; los orbitales en verde, ocupados por un electrón cada uno, son los que van a participar en los enlaces. En el caso de la hibridación sp2, trigonal, como en el C=O (no mostrada la figura), también hay dos pares de electrones solitarios. En resumen, un átomo de oxígeno puede actuar como aceptor de dos puentes de hidrógeno.
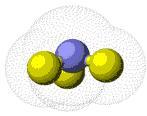
El nitrógeno tiene un electrón menos y por consiguiente presenta sólo un par de electrones solitarios, pero tiene tres electrones en orbitales que pueden participar en enlaces. Un átomo de nitrógeno puede actuar como aceptor de un solo puente de hidrógeno.
| Sin hibridar | 1s22s22p1x2p1y2p1z | Amoníaco | |
|---|---|---|---|
| 1s22sp22sp12sp12sp1 | 
|
|
Otros aceptores de puentes de hidrógeno de importancia son los aniones monovalentes, principalmente el F-1
Propiedades
El enlace de hidrógeno presenta un cierto carácter covalente. O, lo que es lo mismo, podemos considerar que el enlace resuena entre estas dos posibles estructuras:
En condiciones óptimas esto supone un 10% de carácter covalente. Una consecuencia importante de esta resonancia es que se pueden intercambiar los hidrógenos de una molécula con los hidrógenos del agua disolvente. Este fenómeno se aprecia fácilmente si la molécula se disuelve en agua pesada D2O; si los hidrógenos son accesibles al disolvente, se intercambian por deuterio:
La distancia interatómica entre el hidrógeno y el aceptor es menor que la suma de sus radios de Van der Waals, (0,27 nm, aprox. para un par Oxígeno-Hidrógeno), aunque están más separados que si estuvieran unidos por un enlace covalente puro:
La energía del enlace de hidrógeno depende del ángulo de enlace; es máxima cuando los tres átomos (dador-hidrógeno-aceptor) están alineados y disminuye cuando se disponen en ángulo. Es un enlace muy direccional aunque pequeñas variaciones de hasta 20º no tienen demasiada importancia. Por último, la energía de un enlace de hidrógeno depende de los aceptores y dadores. De mayor a menor energía de enlace tenemos las siguientes posibilidades:
En condiciones óptimas la energía de un enlace de hidrógeno puede alcanzar unos 23 kJ/mol (unas 15 veces más que la energía de las fuerzas de dispersión de London.
Puente de hidrógeno intermolecular
De las fuerzas intermoleculares, el puente de hidrógeno es la de mayor entidad, su fuerza es de entre 5 y 30 kJ por mol, pero existen casos en los que llega a 155 kJ por mol. El puente de hidrógeno intermolecular es el responsable de muchas de las cualidades de la sustancia.
Una molécula de agua, se forma entre un átomo de Oxígeno con seis electrones de valencia (sólo comparte dos y le quedan dos pares de electrones libres) y dos hidrógenos con un electrón de valencia cada uno (ambos le ceden su único electrón al oxígeno para que complete el octeto), por ser una molécula polar los electrones que intervienen en sus enlaces, están más cerca del oxígeno que de los de hidrógenos y por esto se generan dos cargas parciales negativas en el extremo donde está el oxígeno y dos cargas parciales positivas en el extremo donde se encuentran los hidrógenos. La presencia de cargas parciales positivas y negativas hace que las moléculas de agua se comporten como imanes en los que las partes con carga parcial positiva atraen a las partes con cargas parciales negativas.
De tal suerte que una sola molécula de agua puede unirse a otras 4 moléculas de agua a través de 4 puentes de hidrógeno. Esta multitud de enlaces por puente de hidrógeno es lo que brinda cualidades especiales al agua.
Estudios de difracción de rayos X indican que la distancia entre los átomos de Oxígeno que intervienen en el puente de Hidrógeno, están separados por 0.28 nm lo que indica un arreglo tetraédrico de las moléculas de agua.
La estructura del agua favorece las interacciones para formar puentes de Hidrógeno, el arreglo siempre es perpendicular entre las moléculas participantes, además, es favorecido por que cada protón unido a un Oxígeno muy electronegativo encuentra un electrón no compartido con el que interactúa uno a uno. De lo anterior se concluye que cada átomo de Oxígeno en el agua puede formar, mediante su par libre de electrones, dos puentes de hidrógeno, y además, los dos átomos de hidrógeno de la molécula forman dos puentes más. Esta característica es la que hace al agua un líquido muy especial, sus puntos de ebullición, fusión y la viscosidad de la misma son sorprendentemente altos.
El elevado punto de ebullición del agua se debe al gran número de enlaces de hidrógeno que cada molécula tiene, en relación a su baja masa molar, y a la gran fuerza de estos enlaces de hidrógeno. El agua tiene puntos de ebullición, fusión y viscosidad muy altas, comparadas con otras sustancias no unidas entre sí por enlaces de hidrógeno. La razón para estos atributos es la dificultad, para romper estos enlaces. El agua es única porque sus átomos de oxígeno tiene dos pares libres y dos átomos de hidrógeno, significando que el número total de enlaces de una molécula de agua es cuatro.
La colinealidad de los puentes es muy importante, un alejamiento de 10° ocasiona la que el puente se rompa.
Los puentes de hidrógeno entre moléculas de agua tienen especial importancia para la vida en nuestro planeta. Sin puentes de hidrógeno, el agua se fundiría a unos –100° C y haría ebullición a cerca de –90° C. Los puentes dan pie a otra propiedad muy poco común del agua: la fase liquida es más densa que la fase sólida. Las moléculas de la mayor parte de las sustancias están "apretadas" en la fase sólida que en la líquida, por lo que el sólido es más denso que el líquido.
Por ello, un sólido casi siempre se hunde al fondo cuando comienza a cristalizarse a partir de la fase líquida. Si esto ocurriera con el agua, los lagos, ríos y mares de las regiones en las que las temperaturas bajan de cero, se congelarían desde el fondo hacia arriba. Es poco probable que los peces y otros organismos acuáticos pudieran sobrevivir en un entorno así.
Puente de hidrógeno intramoleculares
Puede darse dentro de una misma molécula, intervienen en la formación de las estructuras secundarias, terciarias y cuaternarias de las proteínas y en la estabilidad de los ácidos nucleicos. En éstos últimos, los puentes de hidrógeno son los que unen los pares de bases de las dos cadenas de ADN, formando la doble hélice.
En estas macromoléculas, el enlace de hidrógeno entre partes de la misma molécula ocasiona que se doble en una forma específica, que ayuda a determinar el rol fisiológico o bioquímico de la molécula. Por ejemplo, la estructura de doble hélice del ADN se debe primordialmente a los enlaces de hidrógeno entre los pares de bases, que unen una cadena complementaria a la otra y permiten la replicación.
En las proteínas, los enlaces de hidrógeno se forman entre átomos de oxígeno esqueletales y átomos de hidrógeno amida. Cuando el espaciamiento de los residuos de aminoácido que participan en un enlace de hidrógeno es regular entre las posiciones i e i + 4, se forma una hélice alfa. Cuando el espaciamiento es menor, entre las posiciones i e i + 3, se forma una hélice 310. Cuando dos cadenas se unen por enlaces de hidrógeno que involucran residuos alternantes de cada cadena participante, se forma una lámina beta. Los enlaces de hidrógeno también toman parte en la formación de la estructura terciaria de las proteínas, a través de la interacción de los grupos R.
Puente de hidrógeno simétrico
Es un subtipo de enlace de hidrógeno en el que el núcleo de hidrógeno está exactamente a mitad de camino entre dos átomos del mismo elemento.. Es un enlace mucho más fuerte que los puentes de hidrógeno comunes, con orden de enlace 0.5. Se ha observado este tipo de puente en hielo a altas presiones, y también en la fase sólida de muchos ácidos anhidros, como el fluoruro de hidrógeno y el ácido fórmico a altas presiones.
Es un subtipo de enlace de hidrógeno en el que el núcleo de hidrógeno está exactamente a mitad de camino entre dos átomos del mismo elemento.. Es un enlace mucho más fuerte que los puentes de hidrógeno comunes, con orden de enlace 0.5. Se ha observado este tipo de puente en hielo a altas presiones, y también en la fase sólida de muchos ácidos anhidros, como el fluoruro de hidrógeno y el ácido fórmico a altas presiones. También se le ha visto en el anión bifluoruro [F-H-F]− .
Los enlaces de hidrógeno simétricos han sido observados recientemente espectroscópicamente en el ácido fórmico a presión alta (>GPa). Cada átomo de hidrógeno forma un enlace covalente parcial con dos átomos, en vez de con uno. Se ha postulado la existencia de enlaces de hidrógeno simétricos en el hielo a altas presiones (Hielo X). Se forman bajas barreras de enlace de hidrógeno cuando la distancia entre dos heteroátomos es muy pequeña.
Anomalías debidos al enlace de hidrógeno
- Punto de ebullición dramáticamente alto del NH3, H2O y HF, en comparación a los análogos más pesados PH3, H2S, y HCl.
- Viscosidad del ácido fosfórico anhidro y del glicerol.
- Formación de dímeros en ácidos carboxílicos y de hexámeros en el fluoruro de hidrógeno, que ocurre incluso en la fase gaseosa, resultando en grandes desviaciones de la ley de los gases ideales.
- La alta solubilidad en agua de muchos compuestos como el amoníaco es explicada por el enlace de hidrógeno con las moléculas de agua.
- La azeotropía negativa de mezclas de HF y agua.
- La delicuescencia del NaOH es causada, en parte, por la reacción de OH- con la humedad para formar especies H3O2- enlazadas por hidrógeno. Un proceso análogo sucede entre NaNH2 y NH3, y entre NaF y HF.
- El hecho de que el hielo es menos denso que el agua líquida se debe a una estructura cristalina estabilizada por enlaces de hidrógeno.
- La presencia de enlaces de hidrógeno puede causar una anomalía en la sucesión normal de los estados de agregación para ciertas mezclas de compuestos químicos, con el incremento o disminución de temperatura. Estos compuestos pueden ser líquidos hasta una cierta temperatura, luego son sólidos incluso con el incremento de temperatura, y finalmente líquidos cuando la temperatura se eleva sobre el "intervalo anómalo".
- La goma inteligente utiliza enlaces de hidrógeno como su única forma de enlace, así que puede "sanarse" cuando se pincha, debido a que puede aparecer nuevos enlaces de hidrógeno entre las dos superficies del mismo polímero.
Referencias
- ↑ «monografías». Consultado el 21 de diciembre de 2011.
- ↑ «la guía de química». Consultado el 21 de diciembre de 2011.
Fuentes
- Biomol culas1: Puentes de hidrógeno. Available at: http://www.maph49.galeon.com/biomol1/hbonds.html [Accedido Febrero 2, 2012a].
- El puente de hidrógeno es un enlace que se establece entre moléculas capaces de generar cargas parciales. Available at: http://laguna.fmedic.unam.mx/~evazquez/0403/puente%20de%20hidrogeno.html [Accedido Febrero 2, 2012b].
- Hidrógeno - Monografias.com. Available at: http://www.monografias.com/trabajos34/hidrogeno/hidrogeno.shtml [Accedido Febrero 2, 2012c].