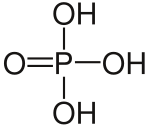
Ácido fosfórico
| ||||||||
Ácido fosfórico. De fórmula química (H3PO4), ácido que constituye la fuente de compuestos de importancia industrial llamados fosfatos. A temperatura ambiente, el ácido fosfórico es una sustancia cristalina con una densidad relativa de 1,83. Tiene un punto de fusión de 42,35 °C. Normalmente, el ácido fosfórico se almacena y distribuye en disolución.
Obtención
Se obtiene mediante el tratamiento de rocas de fosfato de calcio con ácido sulfúrico, filtrando posteriormente el líquido resultante para extraer el sulfato de calcio. Otro modo de obtención consiste en quemar vapores de fósforo y tratar el óxido resultante con vapor de agua.
Aplicaciones
El ácido es muy útil en el laboratorio debido a su resistencia a la oxidación, a la reducción y a la evaporación. Entre otras aplicaciones, el ácido fosfórico se emplea como ingrediente de bebidas no alcóholicas, como pegamento de prótesis dentales, como catalizador, en metales inoxidables y para fosfatos que se utilizan, como ablandadores de agua, fertilizantes y detergentes.
Fosfatos
Son productos formados por la sustitución de parte o todo el hidrógeno del ácido fosfórico por metales. Según el número de átomos de hidrógeno sustituidos, el compuesto obtenido se define como fosfato primario, secundario o terciario. Así, NaH2PO 4, con un átomo de hidrógeno sustituido, se denomina fosfato primario de sodio (también dihidrogenofosfato de sodio), y Na 3PO4, con tres átomos de hidrógeno sustituidos, fosfato terciario de sodio. También conocido como fosfato de sodio, el fosfato terciario de sodio se usa como detergente y ablandador del agua. Los fosfatos primarios y secundarios contienen hidrógeno y son sales ácidas. Los fosfatos secundarios y terciarios son insolubles en agua, a excepción de los de sodio, potasio y amonio; los primarios son más solubles.
Los fosfatos son importantes para el metabolismo de animales y plantas. Los huesos contienen fosfato de calcio, Ca3(PO4)2, y el primer paso en la oxidación de la glucosa en el cuerpo es la formación de un éster de fosfato. Para aportar fosfatos al ganado, se usa el hidrogenofosfato de calcio hidratado, CaHPO4 · 2H2O, como suplemento alimenticio. El fosfato primario de calcio, Ca(H 2PO4)2, se emplea como ingrediente en fertilizantes para plantas.
En los últimos tiempos se ha incrementado la preocupación por los efectos medioambientales perjudiciales de los fosfatos contenidos en los detergentes domésticos. Los detergentes que contienen fosfatos contribuyen a la contaminación del agua, ya que son un medio nutriente para las algas. Si crecieran en exceso, dificultarían la vida acuática de lagos y ríos por la falta del oxígeno.
Referencias
- Baddeley, G. y otros. Química moderna. Madrid: Alianza Editorial, 2ª ed., 1986. Recopilación de trabajos sobre estructura atómica y molecular, estereoquímica, cinética química, alotropía, ácidos y bases, elementos químicos y mecanismos de reacciones orgánicas. Son temas avanzados, que requieren conocimientos previos sobre la materia.
- Breuer, Hans. Atlas de química. Madrid: Alianza Editorial, 1988. Introducción a los fundamentos de la química moderna.
- Fernández, R. M. y otros. Química General. Madrid: Editorial Everest, 1995. Obra de carácter didáctico dirigida a un público con ciertos conocimientos de química.
- Speight, James G.(2002). Chemical Process and Design Handbook. Ed. McGraw-Hill