Diferencia entre revisiones de «Butano»
(→Véase también) |
m (Texto reemplazado: «<div align="justify">» por «») |
||
| (No se muestran 18 ediciones intermedias de 7 usuarios) | |||
| Línea 1: | Línea 1: | ||
| − | |||
{{Elemento_químico | {{Elemento_químico | ||
|nombre=Butano | |nombre=Butano | ||
| − | |imagen= | + | |imagen= Butano123.jpeg |
|nombre,simbolo,numero= C<sub>4</sub>H<sub>10</sub>. | |nombre,simbolo,numero= C<sub>4</sub>H<sub>10</sub>. | ||
| − | |serie_quimica= | + | |serie_quimica= [[Hidrocarburo]] perteneciente a la familia de los [[Alcanos]]}} |
| − | + | ||
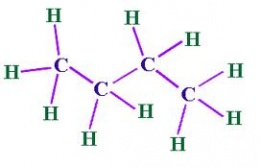
| − | '''Butano'''. | + | '''Butano'''. Es un [[Hidrocarburo]] perteneciente a la familia de los [[Alcanos]] formado por 4 [[átomos]] de [[carbono]] y 10 átomos de [[hidrógeno]], su fórmula semidesarrollada es CH<sub>3</sub>-CH<sub>2</sub>-CH<sub>2</sub>-CH<sub>3</sub>. También es conocido como '''n-butano'''. |
== Propiedades físicas y químicas== | == Propiedades físicas y químicas== | ||
| Línea 15: | Línea 14: | ||
* Punto de ebullición: -1 °C | * Punto de ebullición: -1 °C | ||
* Punto de fusión: -138 °C | * Punto de fusión: -138 °C | ||
| − | + | * Poder calorífico superior: 49.608 kJ/kg | |
| − | * Poder calorífico superior: 49.608 kJ/kg | ||
* Entalpía de combustión= -687,4 kcal/mol (el signo indica que cede energía) | * Entalpía de combustión= -687,4 kcal/mol (el signo indica que cede energía) | ||
== Obtención == | == Obtención == | ||
| − | + | El butano es obtenido mediante destilación fraccionada del [[petróleo]], estando presente en este y el [[gas natural]]. | |
| − | El butano es obtenido mediante destilación fraccionada del [[petróleo]], estando presente en este y el [[gas natural]] | ||
== Aplicaciones == | == Aplicaciones == | ||
| − | + | *Combustible en hogares para la cocina | |
| − | * Combustible en hogares para la cocina | + | *Combustible para el calentamiento de agua. |
| − | * Combustible para el calentamiento de agua. | + | *[[Quemador de gas]]. |
| − | * | + | |
| + | == Riesgos del gas Butano== | ||
| + | Si se produce una fuga de gas butano, y no se actúa con determinación y precaución, este puede producir una defragación o explosión terminando en incendio, en el caso de incendio provocado por gas butano o este sea el principal combustible deberá utilizarse para su extinción [[Dióxido de carbono]] (CO<sub>2</sub>), polvo químico o niebla de agua para enfriar y dispersar vapores. | ||
| + | |||
| + | ===Inhalación=== | ||
| + | La inhalación de gas butano provoca, somnolencia y posible pérdida de conocimiento, estos sintomas no deben confundirse con los provocados por la inhalación de [[Monoxido de Carbono]] (CO), la denominada muerte dulce, mucho mas peligroso y provocado por la mala combustión de los aparatos a gas. | ||
| + | |||
| + | ===Contacto con la piel=== | ||
| + | El contacto del gas butano con la [[piel]] y [[líquido]]s provoca congelación. | ||
| − | == | + | ===Contacto con los ojos=== |
| − | + | Si el gas butano entra contacto con los ojos provocaría la congelación de estos. | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
== Fuentes == | == Fuentes == | ||
| − | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones | + | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones Eneva]]. |
| − | * Rodger W. Griffin "Química orgánica moderna". [[1981]]. [[ | + | * Rodger W. Griffin "Química orgánica moderna". [[1981]]. [[Editorial Reverté]], S.A. |
| − | * | + | * Artículo [http://www.gasbutano.org/2008/09/04/historia-y-origenes-del-gas-butano/ Historia y orígenes del gas butano]. Disponible en "www.gasbutano.org". Consultado: 3 de Agosto de 2011. |
| − | [[ | + | [[Categoría:Hidrocarburos_alifáticos]] |
última versión al 15:33 28 jul 2019
| ||||||||||
Butano. Es un Hidrocarburo perteneciente a la familia de los Alcanos formado por 4 átomos de carbono y 10 átomos de hidrógeno, su fórmula semidesarrollada es CH3-CH2-CH2-CH3. También es conocido como n-butano.
Sumario
Propiedades físicas y químicas
- Color: incoloro.
- Olor: sustancia inodora cuando es pura.
- Densidad relativa de vapor (aire=1): 2,1
- Solubilidad en agua: 3,25 ml/100 ml a 20 °C
- Punto de ebullición: -1 °C
- Punto de fusión: -138 °C
- Poder calorífico superior: 49.608 kJ/kg
- Entalpía de combustión= -687,4 kcal/mol (el signo indica que cede energía)
Obtención
El butano es obtenido mediante destilación fraccionada del petróleo, estando presente en este y el gas natural.
Aplicaciones
- Combustible en hogares para la cocina
- Combustible para el calentamiento de agua.
- Quemador de gas.
Riesgos del gas Butano
Si se produce una fuga de gas butano, y no se actúa con determinación y precaución, este puede producir una defragación o explosión terminando en incendio, en el caso de incendio provocado por gas butano o este sea el principal combustible deberá utilizarse para su extinción Dióxido de carbono (CO2), polvo químico o niebla de agua para enfriar y dispersar vapores.
Inhalación
La inhalación de gas butano provoca, somnolencia y posible pérdida de conocimiento, estos sintomas no deben confundirse con los provocados por la inhalación de Monoxido de Carbono (CO), la denominada muerte dulce, mucho mas peligroso y provocado por la mala combustión de los aparatos a gas.
Contacto con la piel
El contacto del gas butano con la piel y líquidos provoca congelación.
Contacto con los ojos
Si el gas butano entra contacto con los ojos provocaría la congelación de estos.
Fuentes
- Requena, L. Vamos a Estudiar Química Orgánica. (2001). Ediciones Eneva.
- Rodger W. Griffin "Química orgánica moderna". 1981. Editorial Reverté, S.A.
- Artículo Historia y orígenes del gas butano. Disponible en "www.gasbutano.org". Consultado: 3 de Agosto de 2011.