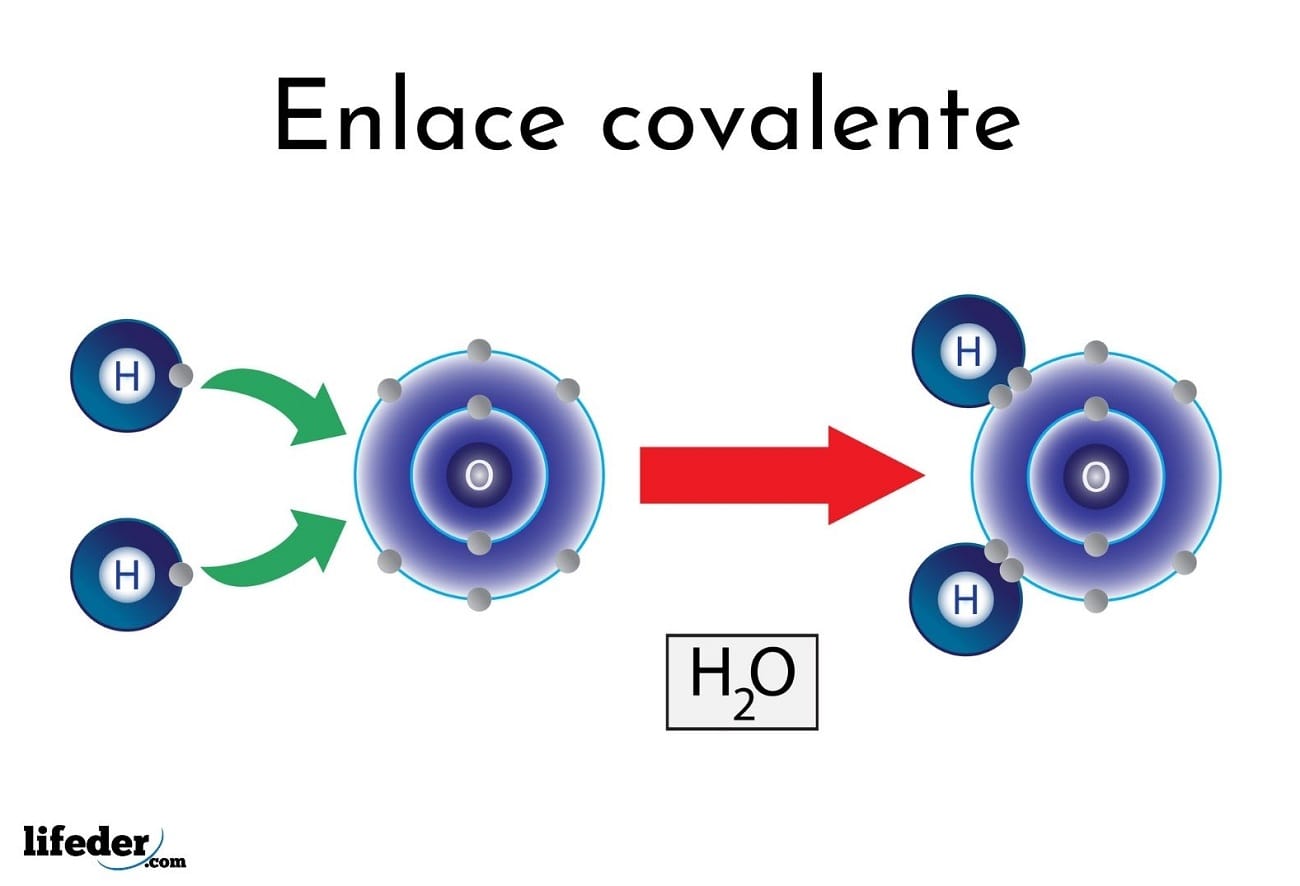
Enlace covalente
Revisión del 16:41 7 oct 2011 de Mariaantonia.jc.scu (discusión | contribuciones)
| ||||||
Sumario
Estructura de las sustancias
El enlace covalente es característico de la unión de los elementos químicos no metálicos entre si, que no difieren grandemente en sus energías de ionización y electrafinidades.
sustancias moleculares
Archivo:Sustancia covalente.jpg
Estructura de la molécula de diflúor y la de cloruro de hidrógeno
====Propiedades====.
- Son las habituales de los enlaces covalentes:
- Temperaturas de fusión bajas. A temperatura ambiente se encuentran en estado gaseoso, líquido (volátil) o sólido de bajo punto de fusión.
- La temperaturas de ebullición son igualmente bajas.
- No conducen la electricidad en ningún estado físico dado que los electrones del enlace están fuertemente localizados y atraídos por los dos núcleos de los átomos que los comparten.
- Son muy malos conductores del calor.
- La mayoría son poco solubles en agua. Cuando se disuelven en agua no se forman iones dado que el enlace covalente no los forma, por tanto, si se disuelven tampoco conducen la electricidad.
conducen la electricidad.
Sólidos covalentes o redes covalentes
Archivo:Sustanc covalente atomica.jpg
Estructura del sólido covalente Silicio
====Propiedades====
Algunas son similares a las de las sustancias moleculares
* No conducen el calor ni la electricidad
- Son insolubles en agua.
A diferencia de las sustancias moleculares:
- Presentan temperaturas de fusión y ebullición muy elevadas.
* Son sólidos a temperatura ambiente.
- Son muy duros (resistencia a ser rayado).
Tipos de enlace
Dependiendo de la diferencia de electronegatividad, el enlace covalente puede ser clasificado en covalente puro o apolar y covalente polar. Si la diferencia de electronegatividad es inferior a 0,4 es covalente apolar , y si está entre 0,4 y 1,7 es un enlace covalente polar.
Referencias
- Colectivo de autores: Química. Tomo I. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1969.
- Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Materiales Complementarios de Química para Ingenieros; Ed. Pueblo y Educación. . Ciudad de La Habana, Cuba. 1987.
- León Ramírez, R.: Química General. Ed. Pueblo y Educación. . Ciudad de La Habana, Cuba. 1985.
- Mahan, B.H: Química Universitaria. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1975.
Fuentes
- http://www.unalmed.edu.co/~cgpaucar/ENLACES.html
- http://www.visionlearning.com/library/module_viewer.php?mid=55&l=s
- http://www.sabelotodo.org/materia/enlaces.html
- http://usuarios.multimania.es/ptro2/fourphotogalery.html
Enlace relacionado