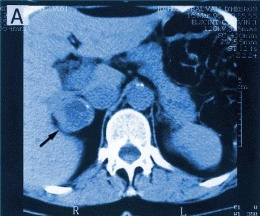
Feocromocitoma
Feocromocitoma. Estos tumores en el 85% de los casos se localizan en la médula suprarrenal y el 15% restante son extrasuprarrenales (paragangliomas) que asientan por orden de frecuencia en: cadena simpática retroperitoneal, órgano de Zuckerkandl, mediastino posterior, vejiga y cuello. El 90% de los feocromocitomas son esporádicos y el 10% pueden formar parte de la neoplasia endocrina múltiple (MEN) tipo 2A o 2B, o bien asociarse a otros síndromes neuroectodérmicos (neurofibromatosis, enfermedad de von Hippel-Lindau, esclerosis tuberosa, enfermedad de Sturge Weber). También se han descrito asociados a tumores carcinoides, tumores pancreáticos endocrinos y como componente de la tríada de Carney (paragangliomas, leiomiosarcomas gástricos y condromas pulmonares).
La incidencia y prevalencia reales del feocromocitoma son desconocidas. Se ha estimado que lo presentan menos del 0,05-0,1% de los sujetos hipertensos. Sin embargo, en el 0,1% de las autopsias se descubre la presencia de un feocromocitoma.
Sumario
Anatomía patológica
Los feocromocitomas son tumores total o parcialmente encapsulados, muy vascularizados y, en general, mayores de 3 cm de diámetro en el momento del diagnóstico. En los de mayor tamaño pueden observarse áreas de degeneración quística, hemorragia y necrosis. En un 10% son bilaterales, aunque cuando forman parte de una MEN tipo 2 se afectan de modo habitual ambos lados (en forma de tumor o de hiperplasia nodular contralateral) y es también más frecuente la localización múltiple. Los feocromocitomas están formados por una proliferación de células pleomórficas de gran tamaño con citoplasma basófilo o eosinófilo, dispuestas en nidos y que con frecuencia muestran atipias nucleares y mitosis. Con el microscopio electrónico se observan gránulos de secreción electrodensos que contienen catecolaminas y otros péptidos que pueden ser demostrados mediante inmunofluorescencia y/o técnicas inmunohistoquímicas.
Aproximadamente el 10% de los casos diagnosticados en edad adulta y el 60% de los diagnosticados en la infancia son malignos. En los niños también es más frecuente la presentación bilateral multicéntrica y ectópica. Los tumores malignos suelen tener mayor tamaño que los benignos. El 30-50% de los paragangliomas son malignos. Se han descrito datos histológicos sugestivos de malignidad de los que quizá sea el más relevante la alteración del patrón de DNA (aneuploidía o poliploidía) detectado mediante citometría de flujo. Sin embargo, en sentido estricto, no existen criterios histológicos fiables de malignidad y únicamente pueden considerarse malignos los casos que presentan invasión local o metástasis de los órganos en los que no existe normalmente tejido cromafín. Los principales lugares de metástasis son los ganglios linfáticos, hígado, pulmones y huesos.
Cuadro clínico
La clínica del feocromocitoma puede ser muy variada y no guarda una clara relación con el tamaño, localización o aspecto histológico del tumor. El diagnóstico puede efectuarse a cualquier edad, aunque es más frecuente entre los 30-50 años y existe un ligero predominio por el sexo femenino. Las manifestaciones son generalmente uniformes en cada paciente y consisten en dos o más síntomas que pueden variar en duración y aumentar en frecuencia e intensidad con el tiempo. Los síntomas más comunes son la cefalea, la diaforesis y las palpitaciones. De los tres, la cefalea es el más relevante y habitualmente es bilateral, pulsátil, de inicio rápido y de menos de una hora de duración, ocurre por la mañana temprano y se asocia a un rápido incremento de la tensión arterial. De forma característica, las manifestaciones clínicas son paroxísticas en la gran mayoría de los pacientes. El inicio de las crisis es repentino y el acmé se alcanza a los pocos minutos con una duración total de menos de una hora. Pueden existir otras manifestaciones como la intolerancia hidrocarbonada, arritmias cardíacas, cardiomiopatía, ictus, rabdomiólisis, edema pulmonar neurogénico o choque.
La HTA está presente en el 80-90% de los casos y puede ser mantenida, mantenida con paroxismos o puramente paroxística. La hipotensión ortostática aparece en menos del 50% de los casos. La hipotensión sostenida o paroxística acompañada de taquicardia debe hacer sospechar un feocromocitoma predominantemente secretor de adrenalina.
Todos los síntomas pueden ocurrir de forma espontánea o precipitarse con ejercicio, presión abdominal, maniobra de Valsalva, coito, defecación, micción –feocromocitoma vesical–, inducción anestésica, cirugía, parto, o bien tras la administración de diversos fármacos tales como: b-bloqueantes, antidepresivos tricíclicos, fenotiacinas, metoclopramida, glucagón y fármacos citotóxicos, entre otros.
El feocromocitoma puede tener poca expresividad clínica o ser totalmente asintomático. Esta circunstancia ocurre en aproximadamente un 20% de los casos diagnosticados en vida, pero hay que tener en cuenta que más del 50% de los feocromocitomas se descubren en el examen autópsico. Se ha estimado que un 5-10% de los incidentalomas suprarrenales son feocromocitomas que pueden permanecer clínicamente silentes durante años, aunque no son inactivos desde el punto de vista bioquímico y una situación de estrés como la inducción anestésica, parto, cirugía o la punción biópsica suprarrenal puede precipitar una crisis hipertensiva. Por tanto, ante una masa suprarrenal, a pesar de no existir HTA ni sintomatología acompañante, debe descartarse siempre la presencia de un feocromocitoma. Dentro del contexto de las MEN tipo 2, los feocromocitomas presentan escasa sintomatología o son totalmente asintomáticos en un 50% de los casos.
Diagnóstico y diagnóstico diferencial
Las manifestaciones clínicas que puede adoptar el feocromocitoma son tan variadas que se le conoce como el "gran simulador". Por tanto, la lista del diagnóstico diferencial es impresionante. Sin embargo, desde el punto de vista práctico, la situación que más frecuentemente puede confundirse con un feocromocitoma es la HTA asociada con crisis de ansiedad. También pueden simular la existencia de un feocromocitoma la ingestión de cocaína, anfetaminas y otros agentes simpaticomiméticos. Las situaciones en las que se considera obligado proceder al diagnóstico de exclusión de feocromocitoma mediante las pruebas de laboratorio.
Diagnóstico bioquímico
Cuando se intenta excluir una enfermedad como el feocromocitoma, en la que su omisión diagnóstica puede ser fatal, pero si se diagnostica es casi siempre curable, es crucial disponer de un método de cribado lo más sensible posible. La determinación de los metabolitos de las catecolaminas en orina, el ácido vanililmandélico y las metanefrinas, mediante técnicas colorimétricas, fueron los primeros métodos de laboratorio empleados que no son muy fiables debido a que muchos fármacos y alimentos pueden alterar sus resultados. Aunque son más modernos y sensibles, los métodos fluorimétricos, que permiten determinar las catecolaminas libres en orina, presentan un problema similar. Para intentar solventar éste y aumentar la precisión diagnóstica, se han desarrollado otras técnicas como el análisis radioenzimático y especialmente la cromatografía líquida de alta resolución, que no presenta interferencias farmacológicas.
La sensibilidad para el ácido vanililmandélico, metanefrinas y catecolaminas libres en orina dependerá del método empleado, umbral de decisión diagnóstica, experiencia del laboratorio y características de los pacientes estudiados. La determinación de ácido vanililmandélico, aunque específica, es la que proporciona mayor cantidad de falsos negativos y, por tanto, no es un buen método de cribado. Por contra, la determinación de las metanefrinas tiene una sensibilidad alta (96-99%) y una especificidad, en cambio, más baja (80-90%). La determinación de las catecolaminas libres en orina fraccionadas mediante cromatografía líquida de alta resolución posee una sensibilidad superior al 95% cuando se consideran patológicos valores marginalmente elevados (p. ej., suma de noradrenalina y adrenalina mayor de 100 µg/24 h). Sin embargo, a este nivel de decisión diagnóstica, la especificidad es relativamente baja. Niveles de decisión más elevados (más de 200 µg/24 h) proporcionan una especificidad superior al 95%, manteniendo la misma sensibilidad. Hay que tener en cuenta que la orina siempre debe recogerse en medio ácido (30 mL, 6M de CLH) para evitar su oxidación y las muestras deben conservarse a 4 ºC hasta su determinación.
En la mayoría de los feocromocitomas, la excreción de catecolaminas y metabolitos en orina también será elevada en los intervalos libres de síntomas. No obstante, si las crisis están muy separadas en el tiempo pueden obtener resultados normales. En estos casos, puede ser útil recoger la orina después de lo que el paciente considera una crisis típica y expresar el resultado en µg/mg de creatinina.
Pruebas farmacológicas
En la mayoría de los casos, las determinaciones basales, asociadas a las técnicas de imagen, son suficientes para descartar o confirmar el diagnóstico de feocromocitoma. Las únicas pruebas vigentes son la de estimulación con glucagón y la de frenación con clonidina. La primera se empleará cuando los hallazgos clínicos sean altamente sugestivos pero la presión arterial sea inferior a 160/100 mm Hg y la producción de catecolaminas, casi normal (catecolaminas plasmáticas: 500-1.000 ng/L). Se administran 1-2 mg de glucagón por vía endovenosa y se considera una respuesta positiva la obtención de unas concentraciones de catecolaminas plasmáticas superiores a 2.000 ng/L o bien un incremento de tres veces el valor basal a los 1-3 min de la administración. La especificidad es del 100%, pero la sensibilidad de sólo un 80%. La prueba de la clonidina se puede emplear cuando las catecolaminas plasmáticas son de 1.000-2.000 ng/L. Este agonista central a2-adrenérgico inhibe la liberación de catecolaminas y disminuye la concentración de catecolaminas plasmáticas tanto en los sujetos sanos como en los hipertensos. Se consideran diagnósticos de feocromocitoma concentraciones de catecolaminas plasmáticas superiores a 500 ng/L a las 2-3 h después de la administración de 0,3 mg de clonidina. La sensibilidad es del 97% y la especificidad, del 67%.
Diagnóstico de localización
Tras el diagnóstico bioquímico es obligado proceder al diagnóstico de localización del feocromocitoma, para el que en la actualidad se dispone de tres métodos incruentos altamente eficaces: la tomografía computarizada (TC), la gammagrafía con 131I o 123I-metayodobencilguanidina (MIBG) y la resonancia magnética (RM).
La ecografía ha sido desplazada por estas técnicas, aunque aún desempeña un papel importante en casos urgentes, durante la gestación y en la edad pediátrica. Las técnicas cruentas como la angiografía y el muestreo venoso con determinación de catecolaminas se consideran exploraciones de segunda línea y en la mayoría de los centros ya se han abandonado.
Típicamente, los feocromocitomas son mayores de 2-3 cm en el momento de su presentación clínica, por lo que, generalmente, pueden ser detectados por TC sin necesidad de contrastre endovenoso. En un 10% de los casos pueden observarse calcificaciones. La sensibilidad de la TC es de un 92-100% para detectar feocromocitomas suprarrenales y de un 70-80% en los ectópicos y en los recurrentes. Su principal problema, especialmente en los pacientes con diagnóstico bioquímico dudoso, es su falta de especificidad.
Diagnóstico genético
Ante cualquier feocromocitoma, debe recordarse la posibilidad de que no se trate de un tumor aislado. Hasta el 19% de los feocromocitomas supuestamente aislados pueden formar parte de una enfermedad de von Hippel-Lindau y el 4% de una MEN 2A. Además, el feocromocitoma –a menudo bilateral y asintomático– puede ser el único hallazgo tanto del MEN 2A (24%) como de la enfermedad de von Hippel-Lindau (38%). El avance de la biología molecular ha facilitado enormemente este procedimiento diagnóstico ya que el estudio en línea germinal (p. ej., leucocitos) de las mutaciones descritas en el protooncogén RET (situado en la región pericentromérica del cromosoma 10) y en el oncogén del cromosoma 3 nos informará de si el paciente presenta una MEN 2 (A o B) o una enfermedad de von Hippel-Lindau, respectivamente. Una vez localizada la mutación, debe procederse al estudio familiar y efectuar únicamente el seguimiento clínico, bioquímico y/o radiológico en los portadores de la enfermedad.
Pronóstico
La supervivencia a los 5 años de los pacientes intervenidos por feocromocitomas supuestamente benignos es del 96% (similar a la población normal ajustada por edad). Sin embargo, pueden detectarse recurrencias locales, metástasis o una segunda lesión primaria después de un período de latencia de varios años. Por tanto, en todos los casos, se recomienda un seguimiento durante un mínimo de 5 años mediante la determinación anual de las catecolaminas y sus metabolitos en orina. Además debe efectuarse una anamnesis dirigida, examen físico y determinación de la presión arterial (cada mes tras el postoperatorio durante el primer año y, posteriormente, cada 6 meses). Sería aconsejable efectuar un seguimiento más estrecho y prolongado (incluso "de por vida") en caso de que las alteraciones histológicas o el estudio del DNA tumoral resultaran sugestivos de malignidad y para los tumores extrasuprarrenales y los diagnosticados en la infancia, aun en ausencia de metástasis demostrables por las técnicas de imagen. La mortalidad global a los 5 años de los feocromocitomas malignos es del 60%. La historia natural de las lesiones malignas es muy variable. Aproximadamente en el 50% de los casos se asiste a una rápida progresión con fallecimiento antes de 5 años, mientras que la otra mitad de los pacientes presenta un curso indolente con larga supervivencia, a pesar de la existencia de enfermedad metastásica.
Tratamiento
El tratamiento del feocromocitoma es la exéresis quirúrgica de la suprarrenal afecta y para ello es preciso disponer de un equipo formado por un endocrinólogo, anestesista y cirujano expertos. Antes de la intervención debe realizarse un bloqueo a-adrenérgico con el fin principal de impedir las crisis hipertensivas asociadas a la inducción anestésica o a la manipulación tumoral intraoperatoria. El fármaco más utilizado para este bloqueo es la fenoxibenzamina, que debe administrarse de forma paulatina desde 1-2 semanas antes de la cirugía electiva. La dosis inicial de 10 mg dos veces al día se aumenta 10-20 mg cada 2 días hasta alcanzar una dosis final de 40-120 mg/día (20-40 mg 2 o 3 veces al día), aunque se puede llegar a 160-200 mg/día. El objetivo es conseguir la normotensión con moderada pero asintomática hipotensión ortostática y eliminación o atenuación marcada de las crisis. El prazosín produce expansión del volumen intravascular sin taquicardia y tiene una acción más corta que la fenoxibenzamina, lo que permite un ajuste de dosis más rápido. La dosis inicial es de 1 mg/8 h y se aumenta hasta 2-5 mg 3 o 4 veces al día para conseguir los mismos objetivos que con la fenoxibenzamina. Otros bloqueantes a1 de acción sostenida (terazosín o doxazosina) pueden ser de utilidad, pero la experiencia clínica aún es limitada. Estos fármacos pueden utilizarse en combinación con la fenoxibenzamina. Los calcioantagonistas también pueden ser útiles y son seguros en los pacientes normotensos que presentan de forma ocasional episodios de HTA paroxística.
El bloqueo b-adrenérgico no es imprescindible y jamás debe realizarse antes que el bloqueo alfa. Está indicado cuando existe taquicardia persistente, taquiarritmias supraventriculares o angina y generalmente son suficientes pequeñas dosis de propranolol (80 mg/día, en varias tomas).
La a-metilparatirosina es un inhibidor de la tirosina hidroxilasa que ocasionalmente puede ser útil para reducir el excesivo nivel de catecolaminas y parece ser especialmente eficaz para tratar la cardiomiopatía inducida por catecolaminas. El tratamiento más adecuado de las crisis hipertensivas es la infusión intravenosa de nitroprusiato (dosis inicial de 200 mg seguida de 0,5-10 µg/kg/min según control de la presión arterial) o bien de fentolamina (10-20 mg disueltos en 250 mL de solución fisiológica en microgotero). En el preoperatorio, la administración de un calcio-antagonista (p. ej., 10 mg de nifedipina) por vía oral puede ser una buena alternativa.
La suprarrenalectomía se suele realizar por laparotomía media que permite la exploración de toda la cavidad abdominal con la finalidad de descartar la presencia bilateral, multicéntrica o metástasis. No obstante, con un buen diagnóstico de localización previo, puede practicarse la intervención por vía posterior (lumbotomía) e incluso por laparoscopia.
Fuente
- Ciril Ferreras Rozman, Medicina Interna, Ediciones Harcourt, 14 Edición, 2000.
- Chandrasekharappa SC, Guru SC, Manickam P, Olifemi S-E, Collins P, Emmert-Buck MR et al. Positional cloning of the gene for multiple endocrine neoplasia-Type 1. Science 1997; 276:404-407.
- Gagel RF, Tashjian AH, Cummings T, Papathanasopoulos N, Kaplan MM, De Lellis RA et al. The clinical outcome of prospective screening for multiple endocrine neoplasia type 2s. N Engl J Med 1988; 318: 478-484.
- Marsh DJ, Mulligan LM, Eng CH. RETProto-oncogene mutations in Multiple Endocrine Neoplasia Type 2 and Medullary thyroid carcinoma. Horm Res 1997; 47:168-178.