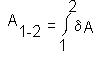Primera ley de la termodinámica
| ||||
Primera Ley e la termodinámica.
Explicación
La cantidad de calor cedida al sistema se invierte en variar la energía interna de este y en el trabajo que realiza el sistema contra las fuerzas exteriores. Para una cantidad de calor infinitesimal, un trabajo elemental y una variación infinitesimal de la energía interna la primera ley de la termodinámica tiene la forma:
Si la variación infinitesimal de la cantidad de calor es mayor que cero, al sistema se le cede calor. Si la variación infinitesimal de la cantidad de calor es menor que cero del sistema se extrae calor. En un proceso finito de transformación del estado 1 al estado 2, las cantidades infinitesimales de calor pueden ser de ambos signos y la cantidad de total de calor en el proceso de transformación es igual a la suma algebraica de los calores en todos los tramos de esta transformación.
Cuando el sistema realiza trabajo sobre los cuerpos externos se considera que la variación infinitesimal del trabajo mayor que cero. Si las fuerzas externas realizan trabajo sobre el sistema se admite que el infinitésimo de trabajo es menor que cero. El trabajo realizado por el sistema en el proceso finito de pasar del estado 1 al estado 2 es igual a la suma algebraica de los infinitésimos de trabajo realizado por el sistema en todos los tramos de este proceso, es decir:
Es imposible construir un motor de acción periódica capaz de realizar un trabajo mayor que la energía que reciba del exterior. Este motor se conoce con el nombre de Móvil perpetuo de primera especie. La imposibilidad de crear el móvil perpetuo de primera especie es también un enunciado de la primera ley de la termodinámica.
Fuentes
- Yavorski, B.M y Detlaf, A.A. Prontuario de Física. Editorial Mir. 1983. Pág 136.