Diferencia entre revisiones de «Tabla periódica de 18 columnas»
(→17 elementos no metálicosthumb|left) |
(→17 elementos no metálicosthumb|left|649×407px|No metales.JPG) |
||
| Línea 33: | Línea 33: | ||
# Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones<br> | # Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones<br> | ||
| − | === | + | === 17 elementos no metálicos[[Image:No metales.JPG|thumb|left|No metales.JPG]]<br> === |
| + | 11 son gases a presión y temperatura normales <br> 6 son gases nobles monoatómicos <br> | ||
| − | + | === Observaciones generales<br> === | |
| − | + | Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17. | |
| + | |||
| + | === Algunas propiedades de los no metales === | ||
| + | |||
| + | En general, pueden presentar todos los estados de agregación a temperatura y presión estandar ambiente (TPEA) | ||
| + | |||
| + | *El dicloro (Cl2) es un gas, el dibromo (Br2) es líquido, el diyodo(I2) es sólido | ||
| + | *Generalmente son malos conductores del calor. | ||
| + | *Generalmente son malos conductores de la electricidad. | ||
| + | *Muchos de ellos existen como moléculas diatómicas | ||
| + | *Las sustancias simples que forman al reaccionar con las sustancias simples metálicas captan electrones | ||
| + | *Las sustancias simples que forman al reaccionar con sustancias simples no-metálicos comparten electrones. | ||
=== Períodos <br> === | === Períodos <br> === | ||
Revisión del 16:49 19 abr 2011
| ||||||
Sumario
- 1 Tabla Periódica de 18 columnas
- 2 Características de la tabla periódica
- 3 información que brinda la tabla periódica
- 4 Elementos químicos conocidos en la actualidad
- 5 Grupos
- 6 Ventajas e inconvenientes del sistema periódico de 18 columnas.
- 7 Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
- 8 Fuente
Tabla Periódica de 18 columnas
Características de la tabla periódica
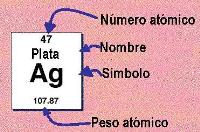
información que brinda la tabla periódica
|imagen=588 × 251
Elementos químicos conocidos en la actualidad
se conocen 148 elementos
elementos químicos
De ellos tenemos:
131 elementos metálicos
87 elementos son metales
26 elementos radioactivos
16 elementos han sido fabricados por el hombre (radioactivos todos)
2 elementos son líquidos
Algunas propiedades de los metales
En general, la mayoría de los metales tienen las propiedades siguientes:
- Son dúctiles y maleables.
- Presentan brillo (lustre)
- Son buenos conductores del calor
- Son buenos conductores de la electricidad
- Todos excepto el Hg son sólidos a temperatura ambiente
- Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones
17 elementos no metálicosArchivo:No metales.JPG No metales.JPG
11 son gases a presión y temperatura normales
6 son gases nobles monoatómicos
Observaciones generales
Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17.
Algunas propiedades de los no metales
En general, pueden presentar todos los estados de agregación a temperatura y presión estandar ambiente (TPEA)
- El dicloro (Cl2) es un gas, el dibromo (Br2) es líquido, el diyodo(I2) es sólido
- Generalmente son malos conductores del calor.
- Generalmente son malos conductores de la electricidad.
- Muchos de ellos existen como moléculas diatómicas
- Las sustancias simples que forman al reaccionar con las sustancias simples metálicas captan electrones
- Las sustancias simples que forman al reaccionar con sustancias simples no-metálicos comparten electrones.
Períodos
Período 1
tiene sólo dos elementos químicos.
Período 2 y Período 3
Tienen ocho elementos químicos.
Período 4 y Período 5
Tienen dieciocho elementos químicos.
Período 6
Tiene treinta y dos elementos químicos.
Período 7
No tiene los treinta y dos elementos porque está incompleto.
Grupos
Grupo 1 (I A): los metales alcalinos
Grupo 2 (II A): los metales alcalinotérreos
Grupo 3 (III B): Familia del Escandio
Grupo 4 (IV B): Familia del Titanio
Grupo 5 (V B): Familia del Vanadio
Grupo 6 (VI B): Familia del Cromo
Grupo 7 (VII B): Familia del Manganeso
Grupo 8 (VIII B): Familia del Hierro
Grupo 9 (VIII B): Familia del Cobalto
Grupo 10 (VIII B): Familia del Níquel
Grupo 11 (I B): Familia del Cobre
Grupo 12 (II B): Familia del Zinc
Grupo 13 (III A): los térreos
Grupo 14 (IV A): los carbonoideos
Grupo 15 (V A): los nitrogenoideos
Grupo 16 (VI A): los calcógenos o anfígenos
Grupo 17 (VII A): los halógenos
Grupo 18 (VIII A): los gases nobles
Ventajas e inconvenientes del sistema periódico de 18 columnas.
Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
Fuente
http://html.rincondelvago.com/la-tabla-periodica_1.html
http://exa.unne.edu.ar/quimica/quimgeneral/UnidadIIINumerosCuanticos.pdf
Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985