Diferencia entre revisiones de «Tabla periódica de 18 columnas»
(→17 elementos no metálicosthumb|left|649×407px|No metales.JPG) |
(→Observaciones generales) |
||
| Línea 37: | Línea 37: | ||
11 son gases a presión y temperatura normales <br> 6 son gases nobles monoatómicos <br> | 11 son gases a presión y temperatura normales <br> 6 son gases nobles monoatómicos <br> | ||
| − | === Observaciones generales<br> === | + | === Observaciones generales<br> === |
| − | Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17. | + | |
| + | *Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17. | ||
| + | *Una '''línea quebrada''' que pasa entre el boro (B) y el aluminio(Al) y desciende hasta el polonio(Po) y el astato(At) señala '''la separación entre metales y no metales'''. Esta separación no debe ser considerada como un limite absoluto entre metales y no metales: cerca de este límite arbitrario, hay elementos que presentan características t'''anto de los metales como de los no metales,''' y por ello a veces reciben el nombre de metaloides (Al(Aluminio), Si(Silicio), Ge(Germanio), As(Arsénico), etc.) | ||
=== Algunas propiedades de los no metales === | === Algunas propiedades de los no metales === | ||
Revisión del 16:53 19 abr 2011
| ||||||
Sumario
- 1 Tabla Periódica de 18 columnas
- 2 Características de la tabla periódica
- 3 información que brinda la tabla periódica
- 4 Elementos químicos conocidos en la actualidad
- 5 Grupos
- 6 Ventajas e inconvenientes del sistema periódico de 18 columnas.
- 7 Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
- 8 Fuente
Tabla Periódica de 18 columnas
Características de la tabla periódica
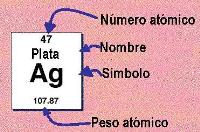
información que brinda la tabla periódica
|imagen=588 × 251
Elementos químicos conocidos en la actualidad
se conocen 148 elementos
elementos químicos
De ellos tenemos:
131 elementos metálicos
87 elementos son metales
26 elementos radioactivos
16 elementos han sido fabricados por el hombre (radioactivos todos)
2 elementos son líquidos
Algunas propiedades de los metales
En general, la mayoría de los metales tienen las propiedades siguientes:
- Son dúctiles y maleables.
- Presentan brillo (lustre)
- Son buenos conductores del calor
- Son buenos conductores de la electricidad
- Todos excepto el Hg son sólidos a temperatura ambiente
- Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones
17 elementos no metálicosArchivo:No metales.JPG No metales.JPG
11 son gases a presión y temperatura normales
6 son gases nobles monoatómicos
Observaciones generales
- Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17.
- Una línea quebrada que pasa entre el boro (B) y el aluminio(Al) y desciende hasta el polonio(Po) y el astato(At) señala la separación entre metales y no metales. Esta separación no debe ser considerada como un limite absoluto entre metales y no metales: cerca de este límite arbitrario, hay elementos que presentan características tanto de los metales como de los no metales, y por ello a veces reciben el nombre de metaloides (Al(Aluminio), Si(Silicio), Ge(Germanio), As(Arsénico), etc.)
Algunas propiedades de los no metales
En general, pueden presentar todos los estados de agregación a temperatura y presión estandar ambiente (TPEA)
- El dicloro (Cl2) es un gas, el dibromo (Br2) es líquido, el diyodo(I2) es sólido
- Generalmente son malos conductores del calor.
- Generalmente son malos conductores de la electricidad.
- Muchos de ellos existen como moléculas diatómicas
- Las sustancias simples que forman al reaccionar con las sustancias simples metálicas captan electrones
- Las sustancias simples que forman al reaccionar con sustancias simples no-metálicos comparten electrones.
Períodos
Período 1
tiene sólo dos elementos químicos.
Período 2 y Período 3
Tienen ocho elementos químicos.
Período 4 y Período 5
Tienen dieciocho elementos químicos.
Período 6
Tiene treinta y dos elementos químicos.
Período 7
No tiene los treinta y dos elementos porque está incompleto.
Grupos
Grupo 1 (I A): los metales alcalinos
Grupo 2 (II A): los metales alcalinotérreos
Grupo 3 (III B): Familia del Escandio
Grupo 4 (IV B): Familia del Titanio
Grupo 5 (V B): Familia del Vanadio
Grupo 6 (VI B): Familia del Cromo
Grupo 7 (VII B): Familia del Manganeso
Grupo 8 (VIII B): Familia del Hierro
Grupo 9 (VIII B): Familia del Cobalto
Grupo 10 (VIII B): Familia del Níquel
Grupo 11 (I B): Familia del Cobre
Grupo 12 (II B): Familia del Zinc
Grupo 13 (III A): los térreos
Grupo 14 (IV A): los carbonoideos
Grupo 15 (V A): los nitrogenoideos
Grupo 16 (VI A): los calcógenos o anfígenos
Grupo 17 (VII A): los halógenos
Grupo 18 (VIII A): los gases nobles
Ventajas e inconvenientes del sistema periódico de 18 columnas.
Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
Fuente
http://html.rincondelvago.com/la-tabla-periodica_1.html
http://exa.unne.edu.ar/quimica/quimgeneral/UnidadIIINumerosCuanticos.pdf
Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985