Diferencia entre revisiones de «Tabla periódica de 18 columnas»
(→2. A partir de su ubicación en la tabla periódica se puede deducir la estructura atómica del elemento.) |
|||
| Línea 10: | Línea 10: | ||
== Características de la tabla periódica == | == Características de la tabla periódica == | ||
<div align="justify">La tabla periódica nos ayuda a comprender el comportamiento, las propiedades y la reactividad de los elementos.</div> <div align="justify">Las propiedades de los elementos tienden a reproducirse de manera regular (periódica) al ordenar a los elementos según su número atómico.</div> | <div align="justify">La tabla periódica nos ayuda a comprender el comportamiento, las propiedades y la reactividad de los elementos.</div> <div align="justify">Las propiedades de los elementos tienden a reproducirse de manera regular (periódica) al ordenar a los elementos según su número atómico.</div> | ||
| − | === '''1. A cada elemento químico le corresponde un casillero.''' === | + | === '''1. A cada elemento químico le corresponde un casillero.''' === |
| + | |||
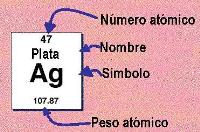
En este figuran el correspondiente nombre, símbolo, número atómico, la masa atómica(Peso atómico), y otros datos. [[Image:Inform de elemento qco.JPG|border|center|Inform de elemento qco.JPG]] | En este figuran el correspondiente nombre, símbolo, número atómico, la masa atómica(Peso atómico), y otros datos. [[Image:Inform de elemento qco.JPG|border|center|Inform de elemento qco.JPG]] | ||
=== '''2. A partir de su ubicación en la tabla periódica se puede deducir la estructura atómica del elemento.''' === | === '''2. A partir de su ubicación en la tabla periódica se puede deducir la estructura atómica del elemento.''' === | ||
| − | + | Se encuentran ubicados: <br> | |
| − | + | ==== '''2.1.''' '''elementos metálicos ''' [[Image:Elementos metalicos.JPG|thumb|right|312x146px|Elementos metalicos]]elementos químicos<br> ==== | |
| − | + | Los metales se encuentran a la izquierda de la tabla, de ellos:<br> | |
| − | |||
| − | |||
*87 elementos son metales | *87 elementos son metales | ||
| Línea 28: | Línea 27: | ||
*2 elementos son líquidos | *2 elementos son líquidos | ||
| − | + | El primer elemento de cada periodo (Li(Litio), Na(Sodio), K(Potasio), etc.) presenta carácter metálico muy evidente, el cual disminuye a medida que se avanza horizontalmente hacia la derecha, mientras se van manifestando las características propias de los no metales. Los elementos del grupo 17 son francamente no metales. | |
Los elementos situados después del uranio, reciben el nombre de transuránidos. Estos elementos no existen en la Naturaleza y han sido obtenidos artificialmente por reacciones nucleares. | Los elementos situados después del uranio, reciben el nombre de transuránidos. Estos elementos no existen en la Naturaleza y han sido obtenidos artificialmente por reacciones nucleares. | ||
| Línea 43: | Línea 42: | ||
# Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones<br> | # Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones<br> | ||
| − | === ''' | + | ==== '''2.2. Elementos no metálicos '''<br>[[Image:No metales.JPG|thumb|left|No metales]]<br> ==== |
| − | |||
| − | |||
| − | |||
| − | |||
| − | En | + | En la actualidad se conocen 17 elementos químicos que son no metales de ellos: <br>11 son gases a presión y temperatura normales <br> 6 son gases nobles monoatómicos <br> |
| − | + | ==== '''Algunas propiedades de los no metales''' <br> ==== | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | En general, pueden presentar todos los estados de agregación a temperatura y presión estandar ambiente (TPEA)<br>#El dicloro (Cl2) es un gas, el dibromo (Br2) es líquido, el diyodo(I2) es sólido<br>#Generalmente son malos conductores del calor.<br>#Generalmente son malos conductores de la electricidad.<br>#Muchos de ellos existen como moléculas diatómicas<br>#Las sustancias simples que forman al reaccionar con las sustancias simples metálicas captan electrones <br>#Las sustancias simples que forman al reaccionar con sustancias simples no-metálicos comparten electrones. | |
| − | *Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17. | + | '''Observaciones generales''' en los no metales<br>*Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17.<br>*Una línea quebrada que pasa entre el boro (B) y el aluminio(Al) y desciende hasta el polonio(Po) y el astato(At) señala la separación entre metales y no metales. Esta separación no debe ser considerada como un limite absoluto entre metales y no metales |
| − | *Una línea quebrada que pasa entre el boro (B) y el aluminio(Al) y desciende hasta el polonio(Po) y el astato(At) señala la separación entre metales y no metales. Esta separación no debe ser considerada como un limite absoluto entre metales y no metales | ||
| − | + | '''2.3. Metaloides '''<br>Elementos químicos que presentan características tanto de los metales como de los no metales,se encuentran ubicado cerca del límite de la línea quebrada, (Al(Aluminio), Si(Silicio), Ge(Germanio), As(Arsénico), etc.) [[Image:Metaloides.JPG|border|right|Metaloides]] | |
| − | *Actúan como sustancias simples no metálicas cuando reaccionan con sustancias metálicas | + | '''Algunas propiedades de los metaloides'''<br> En general, estos elementos tienen propiedades muy variadas y variables. Es decir dependiendo con quien anden, cambiaran de carácter.<br>*Actúan como sustancias simples no metálicas cuando reaccionan con sustancias metálicas<br>*Actúan como sustancias metálicas cuando reaccionan con las sustancias simples no metálicas<br>*Algunos de ellos presentan la propiedad eléctrica de ser semiconductores. |
| − | *Actúan como sustancias metálicas cuando reaccionan con las sustancias simples no metálicas | ||
| − | *Algunos de ellos presentan la propiedad eléctrica de ser semiconductores. | ||
| − | === ''' | + | === '''3.Períodos''' <br> === |
<div align="justify">Las filas horizontales de la tabla periódica son llamadas períodos. Contrario a como ocurre en el caso de los grupos de la tabla periódica, los elementos que componen una misma fila tienen propiedades diferentes pero masas similares: todos los elementos de un período tienen el mismo número de orbitales. Siguiendo esa norma, cada elemento se coloca según su configuración electrónica. El primer período solo tiene dos miembros: hidrógeno(H) y helio(He); ambos tienen sólo el orbital 1s -H 1s1, He 1s2- , y los dos periodos siguientes(2 y 3), cada uno con ocho elementos, se llaman periodos cortos. Los periodos restantes, llamados periodos largos, contienen 18 elementos en el caso de los periodos 4 y 5, o 32 elementos en el del periodo 6. El periodo largo 7 incluye el grupo de los actínidos, que ha sido completado sintetizando núcleos radiactivos más allá del elemento 92, el uranio.</div> <div align="justify">El periodo que ocupa un elemento coincide con su última capa electrónica. Es decir, un elemento con cinco capas electrónicas, estará en el quinto período.</div><div align="justify"></div> <div align="justify">La tabla periódica consta de 7 períodos:</div> | <div align="justify">Las filas horizontales de la tabla periódica son llamadas períodos. Contrario a como ocurre en el caso de los grupos de la tabla periódica, los elementos que componen una misma fila tienen propiedades diferentes pero masas similares: todos los elementos de un período tienen el mismo número de orbitales. Siguiendo esa norma, cada elemento se coloca según su configuración electrónica. El primer período solo tiene dos miembros: hidrógeno(H) y helio(He); ambos tienen sólo el orbital 1s -H 1s1, He 1s2- , y los dos periodos siguientes(2 y 3), cada uno con ocho elementos, se llaman periodos cortos. Los periodos restantes, llamados periodos largos, contienen 18 elementos en el caso de los periodos 4 y 5, o 32 elementos en el del periodo 6. El periodo largo 7 incluye el grupo de los actínidos, que ha sido completado sintetizando núcleos radiactivos más allá del elemento 92, el uranio.</div> <div align="justify">El periodo que ocupa un elemento coincide con su última capa electrónica. Es decir, un elemento con cinco capas electrónicas, estará en el quinto período.</div><div align="justify"></div> <div align="justify">La tabla periódica consta de 7 períodos:</div> | ||
| − | [[Image:Periodo.JPG|thumb|right| | + | [[Image:Periodo.JPG|thumb|right|'''Periodo''']] Período 1 Período 6 <br> tiene sólo dos elementos químicos. Tiene treinta y dos elementos químicos. <br> Período 4 y 5 Período 7 <br> Tienen dieciocho elementos químicos. Incompleto<br> Período 2 y Período 3<br> Tienen ocho elementos químicos. <br>Estos dos últimos periodos tienen catorce elementos separados, para no alargar demasiado la tabla y facilitar su trabajo con ella.<br>El número del período indica la cantidad de niveles energéticos (órbitas) que tienen los átomos de los elementos que se ubican en dicho período. Así, el H y el He que están en el período 1tienen una sola órbita; el Li al estar en el período 2cuenta con dos órbitas, etcétera.<br> |
| − | |||
| − | Estos dos últimos periodos tienen catorce elementos separados, para no alargar demasiado la tabla y facilitar su trabajo con ella. | ||
| − | |||
| − | El número del período indica la cantidad de niveles energéticos (órbitas) que tienen los átomos de los elementos que se ubican en dicho período. Así, el H y el He que están en el período 1tienen una sola órbita; el Li al estar en el período 2cuenta con dos órbitas, etcétera. | ||
| − | === ''' | + | === '''4. Grupos''' === |
<div align="justify">A las columnas verticales de la tabla periódica se les conoce como grupos, Está constituida por 18 columnas o familias, las cuales se ordenan en grupos;. 8 grupos A y 8 grupos B.</div> <div align="justify">Todos los elementos que pertenecen a un grupo tienen la misma valencia atómica, y por ello, tienen características o propiedades similares entre sí. | <div align="justify">A las columnas verticales de la tabla periódica se les conoce como grupos, Está constituida por 18 columnas o familias, las cuales se ordenan en grupos;. 8 grupos A y 8 grupos B.</div> <div align="justify">Todos los elementos que pertenecen a un grupo tienen la misma valencia atómica, y por ello, tienen características o propiedades similares entre sí. | ||
Por ejemplo: los elementos en el grupo IA tienen valencia de I (un electrón en su último nivel de energía) y todos tienden a ceder ese electrón al enlazarse como iones positivos de +1. | Por ejemplo: los elementos en el grupo IA tienen valencia de I (un electrón en su último nivel de energía) y todos tienden a ceder ese electrón al enlazarse como iones positivos de +1. | ||
Los elementos en el último grupo de la derecha son los gases nobles, los cuales tienen lleno su último nivel de energía (regla del octeto) y, por ello, son todos extremadamente no reactivos.</div> | Los elementos en el último grupo de la derecha son los gases nobles, los cuales tienen lleno su último nivel de energía (regla del octeto) y, por ello, son todos extremadamente no reactivos.</div> | ||
| − | [[Image:Gases Nobles.JPG| | + | [[Image:Gases Nobles.JPG|border|left|'''Gases_Nobles''']] |
| − | '''Algunas propiedades de los gases noble''' | + | ==== '''2.4 Algunas propiedades de los gases noble''' ==== |
#En general, estos elementos no reaccionan con casi nadie. | #En general, estos elementos no reaccionan con casi nadie. | ||
| Línea 91: | Línea 74: | ||
#El Rn es radiactivo. | #El Rn es radiactivo. | ||
| − | Los grupos '''se numeran de izquierda a derecha''', según la última recomendación de la IUPAC, asignándole a cada familia un número arábigo del 1 al 18 (y entre paréntesis según la antigua propuesta de la IUPAC, asignándole a cada grupo un número romano con una letra A o B), los grupos de la tabla periódica so[[Image:Grupo tp.JPG|thumb|right|Grupo]]n: | + | Los grupos '''se numeran de izquierda a derecha''', según la última recomendación de la IUPAC, asignándole a cada familia un número arábigo del 1 al 18 (y entre paréntesis según la antigua propuesta de la IUPAC, asignándole a cada grupo un número romano con una letra A o B), los grupos de la tabla periódica so[[Image:Grupo tp.JPG|thumb|right|'''Grupo''']]n: |
| − | Grupo 1 (I A): los metales alcalinos Grupo 10 (VIII B): Familia del Níquel <br> Grupo 2 (II A): los metales alcalinotérreos Grupo 11 (I B): Familia del Cobre <br> Grupo 3 (III B): Familia del Escandio Grupo 12 (II B): Familia del Zinc <br> Grupo 4 (IV B): Familia del Titanio Grupo 13 (III A): los térreos <br> Grupo 5 (V B): Familia del Vanadio Grupo 14 (IV A): los carbonoideos <br> Grupo 6 (VI B): Familia del Cromo Grupo 15 (V A): los nitrogenoideos <br> Grupo 7 (VII B): Familia del Manganeso Grupo 16 (VI A): los calcógenos o anfígenos <br> Grupo 8 (VIII B): Familia del Hierro Grupo 17 (VII A): los halógenos <br> Grupo 9 (VIII B): Familia del Cobalto Grupo 18 (VIII A): los gases nobles <br><br> | + | Grupo 1 (I A): los metales alcalinos Grupo 10 (VIII B): Familia del Níquel <br> Grupo 2 (II A): los metales alcalinotérreos Grupo 11 (I B): Familia del Cobre <br> Grupo 3 (III B): Familia del Escandio Grupo 12 (II B): Familia del Zinc <br> Grupo 4 (IV B): Familia del Titanio Grupo 13 (III A): los térreos <br> Grupo 5 (V B): Familia del Vanadio Grupo 14 (IV A): los carbonoideos <br> Grupo 6 (VI B): Familia del Cromo Grupo 15 (V A): los nitrogenoideos <br> Grupo 7 (VII B): Familia del Manganeso Grupo 16 (VI A): los calcógenos o anfígenos <br> Grupo 8 (VIII B): Familia del Hierro Grupo 17 (VII A): los halógenos <br> Grupo 9 (VIII B): Familia del Cobalto Grupo 18 (VIII A): los gases nobles <br><br> |
| − | En un grupo, las propiedades químicas son muy similares, porque todos los elementos del grupo tienen el mismo número de electrones en su última o últimas capas. | + | En un grupo, las propiedades químicas son muy similares, porque todos los elementos del grupo tienen el mismo número de electrones en su última o últimas capas. |
== Ventajas e inconvenientes del sistema periódico de 18 columnas. == | == Ventajas e inconvenientes del sistema periódico de 18 columnas. == | ||
Revisión del 12:12 16 may 2011
| ||||||
Tabla periódica de 18 columnas
Sumario
- 1 Características de la tabla periódica
- 2 Ventajas e inconvenientes del sistema periódico de 18 columnas.
- 3 Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
- 4 Fuente
Características de la tabla periódica
1. A cada elemento químico le corresponde un casillero.
En este figuran el correspondiente nombre, símbolo, número atómico, la masa atómica(Peso atómico), y otros datos.
2. A partir de su ubicación en la tabla periódica se puede deducir la estructura atómica del elemento.
Se encuentran ubicados:
2.1. elementos metálicos Archivo:Elementos metalicos.JPG Elementos metalicoselementos químicos
Los metales se encuentran a la izquierda de la tabla, de ellos:
- 87 elementos son metales
- 26 elementos radioactivos
- 16 elementos han sido fabricados por el hombre (radioactivos todos)
- 2 elementos son líquidos
El primer elemento de cada periodo (Li(Litio), Na(Sodio), K(Potasio), etc.) presenta carácter metálico muy evidente, el cual disminuye a medida que se avanza horizontalmente hacia la derecha, mientras se van manifestando las características propias de los no metales. Los elementos del grupo 17 son francamente no metales.
Los elementos situados después del uranio, reciben el nombre de transuránidos. Estos elementos no existen en la Naturaleza y han sido obtenidos artificialmente por reacciones nucleares.
Algunas propiedades de los metales
En general, la mayoría de los metales tienen las propiedades siguientes:
- Son dúctiles y maleables.
- Presentan brillo (lustre)
- Son buenos conductores del calor
- Son buenos conductores de la electricidad
- Todos excepto el Hg son sólidos a temperatura ambiente
- Al hacer reaccionar su sustancia simple con la sustancia simple no metálica ceden electrones
2.2. Elementos no metálicos
Archivo:No metales.JPG No metales
En la actualidad se conocen 17 elementos químicos que son no metales de ellos:
11 son gases a presión y temperatura normales
6 son gases nobles monoatómicos
Algunas propiedades de los no metales
En general, pueden presentar todos los estados de agregación a temperatura y presión estandar ambiente (TPEA)
#El dicloro (Cl2) es un gas, el dibromo (Br2) es líquido, el diyodo(I2) es sólido
#Generalmente son malos conductores del calor.
#Generalmente son malos conductores de la electricidad.
#Muchos de ellos existen como moléculas diatómicas
#Las sustancias simples que forman al reaccionar con las sustancias simples metálicas captan electrones
#Las sustancias simples que forman al reaccionar con sustancias simples no-metálicos comparten electrones.
Observaciones generales en los no metales
*Al hidrógeno no se lo ha encontrado una ubicación satisfactoria, pues por su estructura electrónica le corresponde el grupo 1, pero sus propiedades se asemejan más al grupo 17.
*Una línea quebrada que pasa entre el boro (B) y el aluminio(Al) y desciende hasta el polonio(Po) y el astato(At) señala la separación entre metales y no metales. Esta separación no debe ser considerada como un limite absoluto entre metales y no metales
2.3. Metaloides
Elementos químicos que presentan características tanto de los metales como de los no metales,se encuentran ubicado cerca del límite de la línea quebrada, (Al(Aluminio), Si(Silicio), Ge(Germanio), As(Arsénico), etc.)
Algunas propiedades de los metaloides
En general, estos elementos tienen propiedades muy variadas y variables. Es decir dependiendo con quien anden, cambiaran de carácter.
*Actúan como sustancias simples no metálicas cuando reaccionan con sustancias metálicas
*Actúan como sustancias metálicas cuando reaccionan con las sustancias simples no metálicas
*Algunos de ellos presentan la propiedad eléctrica de ser semiconductores.
3.Períodos
Período 1 Período 6
tiene sólo dos elementos químicos. Tiene treinta y dos elementos químicos.
Período 4 y 5 Período 7
Tienen dieciocho elementos químicos. Incompleto
Período 2 y Período 3
Tienen ocho elementos químicos.
Estos dos últimos periodos tienen catorce elementos separados, para no alargar demasiado la tabla y facilitar su trabajo con ella.
El número del período indica la cantidad de niveles energéticos (órbitas) que tienen los átomos de los elementos que se ubican en dicho período. Así, el H y el He que están en el período 1tienen una sola órbita; el Li al estar en el período 2cuenta con dos órbitas, etcétera.
4. Grupos
Por ejemplo: los elementos en el grupo IA tienen valencia de I (un electrón en su último nivel de energía) y todos tienden a ceder ese electrón al enlazarse como iones positivos de +1.
Los elementos en el último grupo de la derecha son los gases nobles, los cuales tienen lleno su último nivel de energía (regla del octeto) y, por ello, son todos extremadamente no reactivos.2.4 Algunas propiedades de los gases noble
- En general, estos elementos no reaccionan con casi nadie.
- Todos son gases monoatómicos en condiciones normales
- Son muy poco reactivos, de hecho He, Ne y Ar no reaccionan con nada
- El Kr y el Xe reaccionan con O y F y forman algunos compuestos.
- El Rn es radiactivo.
Los grupos se numeran de izquierda a derecha, según la última recomendación de la IUPAC, asignándole a cada familia un número arábigo del 1 al 18 (y entre paréntesis según la antigua propuesta de la IUPAC, asignándole a cada grupo un número romano con una letra A o B), los grupos de la tabla periódica so
n:
Grupo 1 (I A): los metales alcalinos Grupo 10 (VIII B): Familia del Níquel
Grupo 2 (II A): los metales alcalinotérreos Grupo 11 (I B): Familia del Cobre
Grupo 3 (III B): Familia del Escandio Grupo 12 (II B): Familia del Zinc
Grupo 4 (IV B): Familia del Titanio Grupo 13 (III A): los térreos
Grupo 5 (V B): Familia del Vanadio Grupo 14 (IV A): los carbonoideos
Grupo 6 (VI B): Familia del Cromo Grupo 15 (V A): los nitrogenoideos
Grupo 7 (VII B): Familia del Manganeso Grupo 16 (VI A): los calcógenos o anfígenos
Grupo 8 (VIII B): Familia del Hierro Grupo 17 (VII A): los halógenos
Grupo 9 (VIII B): Familia del Cobalto Grupo 18 (VIII A): los gases nobles
En un grupo, las propiedades químicas son muy similares, porque todos los elementos del grupo tienen el mismo número de electrones en su última o últimas capas.
Ventajas e inconvenientes del sistema periódico de 18 columnas.
Posibilidad que brinda la utilización del sistema periódico como instrumento de trabajo.
Fuente
http://html.rincondelvago.com/la-tabla-periodica_1.html
http://exa.unne.edu.ar/quimica/quimgeneral/UnidadIIINumerosCuanticos.pdf
Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985