Enfermedad hemolítica perinatal por isoinmunización Rh
| ||||
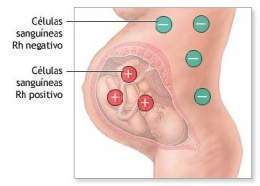
Enfermedad Hemolítica Perinatal por Isoinmunización Rh. Es una anemia que afecta al feto en el transcurso de su vida intrauterina, provocada al sensibilizarse la embarazada por diferentes antígenos existentes en la sangre fetal y que están ausentes en la madre.
Sumario
Características
Estos antígenos estimulan la formación de anticuerpos IgG en la madre, que por su bajo peso molecular atraviesan la barrera placentaria y provocan una anemia hemolítica en el feto. Por tanto, esta enfermedad es un trastorno inmunológico, en el cual el mecanismo inmunitario de la madre es estimulado a producir anticuerpos que destruyen los eritrocitos fetales. La severidad de la anemia resultante dependerá de diversos factores tales como, títulos de anticuerpos desarrollados por la madre, la afinidad de éstos por las células rojas fetales y la habilidad del feto, haciendo uso de la eritropoyesis compensadora, para soportar la destrucción de sus hematíes. Por eso el cuadro clínico en el niño estará en relación con la magnitud de la anemia,que puede resultar desde una anemia ligera que no requiere tratamiento, hasta ictericia grave en el reciénnacido, querníctero y fetohidrópico.
Sistema de grupos sanguíneos Rh
De los diferentes antígenos de grupos sanguíneos existentes en los glóbulos rojos,los agrupados en las familias ABO y Rh respondenpor una gran parte de los fenómenos de isoinmunización y de la enfermedad hemolítica perinatal (EHP).Elsistema o familiaRh descubierto por Landsteineen 1940 es el causante de las formas más graves de enfermedad.Existen 3 pares de antígenos de esta familia (Dd, Cc, Ee) que son heredados en 2 grupos de 3 antígenos, un grupo de 3 de cada progenitor. La presencia del antígeno D determina que el individuo sea Rh positivo, y su ausencia lo hace Rh negativo.
Aproximadamente 45 % de los individuos Rh positivos son homocigóticos DD y los restantes (55 %) heterocigóticos Dd. El D es heredado de uno solo de los progenitores. Si el esposo Rh positivo de una paciente negativa es homocigótico, todos sus hijos serán D positivo, y si es heterocigótico, en cada embarazo existe la misma posibilidad de que el feto sea D ó d. La distinción entre padres homocigóticos y heterocigóticos es complicada, porque el antígeno d no ha sido aislado y, por tanto, no existe suero anti d; por lo que el verdadero genotipo del padre tieneque determinarse por tablas de frecuencia de genotipos en la población general.
El d se incluye gráficamente en los genotiposcomo completamiento de las fórmulas. En la actualidad se piensa que ser d significa ausencia de D. Algunos hematíes reaccionan débilmente con los anticuerpos anti D, porque contienen un gen que produce sólo una parte del antígeno D; esta variante es la Du y debido a esta débil reacción, estos individuos con muchafrecuencia son clasificados como Rh negativos erróneamente, o sea, que el Du tiene que estar ausente para considerar al individuo negativo.Existe una condiciónmuy rara donde el individuo no tiene ningún antígeno de la familia y son llamados Rh nulos. El sistema Rh es un verdadero mosaicoantigénico: son mucopolisacáridos con propiedades antigénicas, unidos a fosfolípidos en las superficies de los hematíes.
El locus genético del antígeno Rh está en el brazo corto del cromosoma 1. El productofinal del locusRh es una pequeña proteína con PM 1 000-10 000 y múltiples determinantes antigénicas. El antígeno Rh está presenteen la membrana del hematíe desde la sexta semana de vida fetal. La frecuencia en la población de los antígenos de la familia. Los símbolos R y r indican la presencia o ausencia del antígeno D en el eritrocito. Se debe recordarque la expresión d se hace gráfica con un criterio de completamiento.
En la mayoría de las poblaciones blancas caucásicas, la incidencia de Rh negativo es de 15 a 16 %,pero es 35 % en la población vasca. En la población negra es de 4 a 7 % de Rh negativos y la incidencia es muy baja en asiáticos, de 1 % o menos. Nuestrapoblación, con un alto mestizaje, tiene frecuencias menores que la población blanca y, basados en publicaciones de bancos de sangre y otros, se acepta que 10 % de nuestra población es Rh negativo.
Fisiopatología
Antes de los trabajos de Zipursky sobrepasaje transplacentario de eritrocitos fetales a la circulación materna y la comprensión del concepto verdaderode transfusión fetomaterna, se pensaba que tenía que existir daño o enfermedad placentaria que permitiera la hemorragia transplacentaria (HTP).
Hoy se sabe que durante el embarazonormal, los hematíes del feto atraviesan la placenta aproximadamente en 5 % de las embarazadas duranteel primer trimestre y en 45 % de ellas al final del tercer trimestre. Existeevidencia de HTP en algún momento du-ranteel embarazo o en el momento del parto, aproximadamente en 75 % de las mujeres. El tamaño de la HTP generalmente es pequeña, de 0,1 mL en casi 50 % de los partos normales y en 1 % pueden pasar hasta 5 mL de sangre fetal. Cantidad es mayor que 30 mL o más de sangre fetal en la circulación de la madre sólo ocurren en 0,25 % de los nacimientos.
La HTP en el aborto es de 0,1 mL. La posibilidadde HTP se incrementa durante el embarazo, en el embarazo ectópico, aborto terapéutico, biopsiacoriónica, amniocentesis, versión externa, [[cesárea] o alumbramiento artificial. La reacción de elusión ácida de Kleihauer-Betkees muy sensible y exacta para demostrar la presencia y la cuantía de la HTP. Los eritrocitos D del feto, activan la formación de anticuerpos anti D IgG que atraviesan la placenta y cubren los eritrocitos D positivos del feto.
Este pasaje transplacentario de IgG de la madre al feto es facilitado por el trofoblasto, que no se comporta pasivamente, pues gobiernala producción de hormonas inmunosupresoras y protege al feto, que es un injerto, contra el rechazo del sistema inmunológico de la madre.
Los anticuerpos, por tanto, atraviesan la placenta por difusión,pero interactúan con receptores Fc de la superficiede lascélulas del sincitiotrofoblasto y son transportados activamente y liberados en la parte fetal. Los eritrocitos del feto cubiertos de anticuerpos Ig antiD primero son destruidos extravascularmente en el bazo fetal.
La anemia resultante estimula la producción de [[eritropoyetina[[ e incrementa la eritropoyesis y cuando la médula ósea fetal no puede compensarlos efectos de la hemólisis incrementada, se produce la eritropoyesis extramedular en el hígadoy el bazo. Se incrementa la producción de eritrocitos jóvenesanucleados (eritroblastos) que se liberan en la circulación para compensar la anemia. Estos eritrocitos jóvenesno están aptos para la transportación de oxígeno, y esto, unidoa la destrucción mantenida por la hemólisis, ocasiona una anemia de grado variabley, por lo tanto,con un amplio espectro de severidad.
Algunos fetos resultanlevemente afectados y al nacimiento muestran discreta anemia e ictericia ligera durante los primeros días de vida, lo que constituye una forma de anemia hemolíticadel recién nacido (RN).
Otros casos manifiestan una afección moderada, y durante la vida intrauterina desarrollan anemia importante, hepatoesplenomegalia y al nacimientodesarrollan hiperbilirrubinemia, que si no se trata,puede llegar al querníctero o impregnación de los núcleosgrises de la base;de sobrevivir, estos niños quedan con daño cerebral y otras secuelas. Esta es la forma de ictericia grave del RN.
Los casos más severos muestranprofunda anemia que se desarrolla en el útero muy precozmente, y que se complica con ascitis, hidrotórax y anasarca, hepatoesplenomegalia, eritroblastosis y una altamortalidad. Esta es la forma de feto hidrópico. Al nacimiento, estos niños desarrollan rápidamente insuficiencia cardíaca y su sobrevivencia es muy pobre.Este edema generalizado está muy relacionado con la obstrucción de la vena porta, por los islotes de la eritropoyesis extendidos, con producción de ascitis y disminución de la producción de albúmina.
La profunda hipoalbuminenia lleva a la ascitis y edemageneralizado, por tanto, la severidad dela enfermedad hemolítica en el niño dependerá de la severidad de la anemia y ésta, a su vez, de:
- La cantidadde Ig G de la madre (títulos) y que está relacionada con la cuantía de la HTP previa.
- La afinidad o avidez de los anticuerpos por la membrana del eritrocito fetal D.
- El momento en elcual se forman los anticuerpos.
- La habilidad del feto para luchar contrala anemia sin llegara convertirse en hidrópico.
Diagnóstico de la Enfermedad (EHRh)
Para el diagnóstico de la isoinmunización de la madre y, por tanto, del riesgo de un niño afectado por la EHRh, es necesario el estudio de la embarazada desde la primera consulta prenatal.
Durante la Atención Prenatal
La historia clínicatiene una gran importancia, y debeser realizada detalladamente; en ella se recogerán datosrelacionados con el posible conflicto.
- Antecedentes de transfusiones o heterohemoterapia y si han existido reacciones transfusionales.
- Número de gestaciones terminadas en partos, cesáreas y abortos espontáneos o provocados, analizados cronológicamente.
- Historia de niños afectados con anemia, ictericia, nacidos muertos o muertesneonatales.
- Historia neonatalde niños afectados que necesitaron transfusiones, exanguino transfusiones o foto-terapia.
- Especificar si los hijos fueron de distintas parejasy referencia de grupos sanguíneos del padre, si son conocidos.
Entre las investigaciones de laboratorio, indicada en el momento de la captacióndel embarazo, está el grupo sanguíneo y Rh a toda embarazada. De ser este Rh negativo, se indicará examen de grupo y Rh al esposo. Si el esposoes Rh negativo no debe existir conflicto, pero si esta pareja tiene antecedentes de EH, debe realizarse estudios de genotipos que puedan aclarar la posibilidadde sensibilización a otros antígenos o subgrupos.
Si la pareja resulta ser incompatible (pacienteRh negativo y esposoRh positivo) debeinvestigarse si éste es homocigótico DD o heterocigótico Dd, para conocer la posibilidad del grupo del niño y establecer el pronóstico. Desde el puntode vista práctico,la determinación de la cigocidad del esposo, puede reservarse para los esposos de pacientes sensibilizadas, en los que sí es necesario establecer un pronóstico certero y, además, por razones de costo beneficio. Una vez aclaradosestos hechos, la estrategia durante el embarazo está dirigida a la detección temprana de anticuerpos maternos.
Detección de anticuerpos maternos
En muchos laboratorios se realizan investigaciones de anticuerpos maternos por métodos manualesen medios salinos albuninoideos, test de antiglobulina indirecta o test de Coombs indirecto y en medios enzimáticos.
Dentro de los métodos manualesel más usado esel Coombsindirecto, para el cual cada laboratorio debe tener establecido su cifra crítica, que es aquéllapor debajo de la cual no han reportado morbilidad ni mortalidad del feto, por lo que el riesgo de éste es mínimo(la mayoría de los autores sitúanpor debajo de 1:16).Aunque el valor de los títulosde anti D por la prueba de Coombs indirecta tiene poco valor predictivo del gradode severidad de la enfermedad, sí se puedeorientar en cuanto al momento de ocurrencia de la sensibilización:
- Títulos elevadosal inicio de la gestación plantean que la sensibilización se produjo en la anteriorgestación.
- Cualquier elevaciónde títulos de 2 o más diluciones plantea que el feto debe estar afectadopor enfermedad hemolítica.
- Si existen títulos elevados al inicio, se mantienen en meseta o descienden a través del embarazo y el padre es heterocigótico, pueden explicarla presencia de un feto negativo.
- Títulos bajos al finalde la gestación podrían expli-carque éste fuera el embarazoprimosensibilizado.
- Títulos elevadosque descienden de forma muy brusca, para algunos autoresse deben a anemia fetal muy severa y riesgo de muerte.
Está aceptado que la tendenciade los títulos de Coombs tienenmás valor que el títuloen sí. Internacionalmente se prefiere la detección de anticuerpos por métodos más sofisticados, dado que la titulación por Coombs indirectoofrece sólo títulos o estimados semicuantitativos de la concentración de anti D. Por eso se usa el autoanalizador que parece establecer mejor correlación de la severidad de la enfermedad y otras técnicas como test radiométricos de antiglobulina, flujo citométrico, ELISA y otras técnicas para medir mecanismos de destrucción celular(ADCC)o que miden la habilidad del anti D de la embarazada para favorecer la adherencia y fagocitosis de las células rojas por monocitos(MMA).
La detección de anticuerpos maternosdebe realizarse durante el primer trimestre, después de las 18 semanas y de ese momento en adelante cada 4 semanas hasta el parto. Si todos los resultados se mantienen negativos, se indica de nuevo después del parto para administrar la profilaxis, y de nuevo a los 3 ó 6 meses alrecién nacido.
Cuando durante el embarazo se detecta Coomb sin directo positivo, aunque sea en título bajo, se definea la embarazada comoisoinmunizada, y su manejo y control en consulta es diferente y se realizará en consulta especializada del nivel secundario de atención. Los títulos de anti D deben medirsemensualmente y cuando éstos seelevan por encima de 1:16 o del valor crítico establecido por cada laboratorio, es necesario establecerel grado de afectación fetal estudiando el líquido amniótico.
Estudio del líquido amniótico
El líquido amniótico en pacientes sensibilizadas se estudia cuando los títulos de anti D se elevanpor encima de 1:16. En el líquido se busca la presenciade bilirrubina por espectrofotometría (EFT) que ofrece información segura del grado de enfermedad en el feto hasta 95 %.La sola observación del LA en el momentode la amniocentesis (ACT) permitever la coloración amarillenta, debidoa la tinción por la bilirrubina. La ACT debe realizarse localizando previamente la inserción placentaria por ultrasonografía, y se seleccionará, por tanto, el sitio idealpara la punción.
Los riesgos maternosy fetales asociadoscon la ACT son mínimos si se toman todas las precauciones. Se extraen 10 ó 15 mL de LA, se centrifuga, filtra (siempre protegido de la luz para evitarla decoloración de la bilirrubina) y se realizanlecturas de espectro-fotometría a diferentes longitudesde onda, para bus-car los cambios de densidad ópticaa 450 mm paramedirla concentración de la bilirrubina. Estas lecturas seploteanen papel semilogarítmico y comparadas con la lectura del LA normal, permitendeterminar la diferencia de densidad óptica (DDO) a 450 mm(fig. 19.1).Esta diferencia obtenida (DDO), siempre relacionada con la edad gestacional, se lleva e interpreta en gráficos diagnósticos-pronósticos conocidos que ayu-dan a determinar el grado de afectación fetal y orientanla conducta que se debe seguir.
Cuando las ACT se realizandespués de la semana 32, tambiénse estudia la madurez pulmonar. Las lecturas que caenen la zona 1 corresponden a niños no afectados o muy levemente afectados. Generalmente puede esperarse hasta el términode la gestación. Lecturas en la zona 2 indican enfermedad moderada que incrementa su severidad si se acercana la zona 3. En esta zona 2 suele ser necesario repetirelestudio 1 ó 2 semanas después, y los valores constantes o ascendentes se asocian con formas más graves de la EH y valoresdescendentes a casosmás leves. Generalmente hay que adelantar el parto.
En la zona superior o zona 3, las lecturas indican casos muy severos, frecuentemente con posibilidad de convertirse en recién nacidoshidrópicos en 7 a 10 días. Antes de la semana 32, requieren transfusión intrauterina y después terminación del embarazo para evitar la muerte fetal.
Los límites de laszonas tienen inclinación descendente, debido a las cantidades decrecientes de formación de bilirrubina, a medida que la gestación progresa. Cuando la placenta es anterior, la ACT debe realizarse bajo control ultrasonográfico, y realizar todos los esfuerzos para evitar atravesarla con la aguja, pues si se causa trauma placentario, se ocasiona HTP y elevacióndel título de anticuerpos. Si el líquido amniótico se mezcla con sangre, la EFTproduce elevaciones que oscurecen las lecturas deDDOa 450 mm e inutilizan la muestra.
La presencia de meconio distorsiona y aumenta la elevación a los 450 mm. Algunasmalformaciones que producen hidramnios, pueden dar lecturaserróneas deDDO 450 mm. La primera espectrofotometría generalmente se realiza a las 28 ó 30 semanas, a no ser que la historia obstétrica o el título de anticuerpos obligue a realizarla antes. Este procederse repite de 1 a 3 semanas después en dependencia de la severidadde la enfermedad.
Ultrasonografía diagnóstica
La ultrasonografía diagnóstica ha desempeñado un papelimportante en el diagnóstico y tratamiento de la EHRh. Además del establecimiento de la edad gestacional, sitio de inserción placentaria para la ACT y diagnóstico de las características del feto hidrópico con el diagnóstico de ascitis, hidrotórax, edema subcutáneo, efusión pericárdica, etc., permitediagnosticar el grosor yextensión de la placenta o pérdida de su estructura por falta de definición del cotiledón. Tambiénpermite realizar mediciones de hígado y bazo fetaly ayuda a establecer el grado de severidad de la enfermedad. Nos aporta también los datos del perfil biofísicopara saber el grado de bienestarfetal.
Recientemente algunos autores relacionan las mediciones de flujometría Dopplercomo predictor de anemia fetal y para decidir el momento en que debe comenzarse la terapéutica intrauterina. Monitoreo fetal electrónico. Se presentan CTGcondesaceleraciones y trazadostípicos sinusoidales enfetos con extrema anemia o hidrópicos. Muestra de sangre fetal.En los últimos años se ha desarrollado la técnica de obtención de sangre fetal dela vena umbilical del feto, que permite determinar todos los parámetros que se miden después del nacimiento, o sea, hemoglobina, hematócrito, bilirrubina,conteo de plaquetas, leucocitos, proteínas séricas y, por supuesto grupo y Rh. Es, por lo tanto, el medio más seguro para determinar el grado de severidadde la EH.
Este proceder no está exento de riesgos,y aun en manos expertas, el riesgo de pérdida fetal es de 1 a2 %, así como el riesgo de HTP es alto, con estimulación de niveles de anticuerpos en la madre como presenta estos riesgos, se recomienda sólo para pacientes cuyas espectrofotometrías seriadas tienen lecturas ascendentes en la parte superior de la zona2, o cuando existe una placenta en cara anteriory títulos muy elevados. Se pueden obtener muestras desde las20 semanas. Recientemente un métodoconfiable para determinar grupo y Rh al feto se ha logrado con estudios de ADN de biopsiascoriónicas, que ha permitido no utilizar procederesinvasivos en niños D negativosy manejar precozmente a las madrescon niños D positivose historiade EH severa en embarazosanteriores.
Protección del Sistema abo en la Enfermedad
Trabajos de Levineen 1943 y posteriormente en 1958 reportaron que la incompatibilidad ABO entre la madrey el padre del niño afectados por EHRh era más baja que lo esperado. El efecto protector de la incompatibilidad ABO contra la sensibilización Rh fue demostrado experimentalmente cuando sólo 9 % de los individuos Rh negativo inyectados con hematíes positivos ABO incompatibles, desarrollaron anti D,comparados con 59 % alos que seles inyectócélulas ABO compatibles (Sterm,1956).
Este mecanismo de protección probablemente se debe a la rápida hemólisisintravascular de los eritrocitos fetalesABO incompatibles por los anticuerpos IgMA o IgMB de la madre o seguida de la extracción hacia el hígadodel producto destruido, donde no puede iniciar una respuesta de anticuerpos. Este efecto supresor natural llevó a la idea de que la administración de anti D a la madre podría tener el mismo efecto,que consiste en destruir las células positivasdel feto antes de que pudieran produciruna res-puesta inmunitaria.
Prevención de la Sensibilización por Rh
La prevención de la sensibilización por Rh es un logro muy importante en el manejo de la embarazada Rh positiva. Diversos autores que han tratadode imitar el efecto protectordel ABO sobre la inmunización por Rh, como planteamos anteriormente, experimentaron inyectando voluntarios con IgM y anti D y no lograron evitarla inmunización. Posteriormente, Finn, Clarke y Donohue en Liverpool logran el efectosupresor inyectando IgG anti D.Otrosinvestigadores como Freda (1964) demostraron que la inyección de gammaglobulina anti D en lugar de plasma, era un método más seguro y eficaz.
Finalmente se concluyóque la inyección intramuscular de Ig anti D a las mujeres Rh negativo, despuésdel parto de un niño Rh positivo, preveníala inmunización y que es necesario repetirla cada vez que se produzcaun nuevo parto con niño Rh positivo. Durante todos estos años, se ha investigado con diferentes dosis y vías, y actualmente es aceptado que una dosis estándar de 100mg resulta adecuada para la mayoría de estos casos, excepto cuando ha ocurrido una HTP grande. En algunos países, como en Estados Unidos, se usan dosis de 250 a 300 mg de anti D.
El aceptar dosis de 100 mg está basado en que esta dosis previene la inmunización causada por 4 ó 5 mLde eritrocitos positivos que representa aproximadamente 99 % de todas las HTP. Dosis menoresque 50 mgson suficientes para la profilaxisdespués del aborto. La Ig anti D cubana tiene una dosis de 250 mg.
Las recomendaciones y requisitos para la administración de inmunoglobulina anti D en el puerperioson las siguientes:
- Madre Rh negativa Du negativa.
- Coombs indirecto negativo en el posparto.
- Recién nacidoRh positivo.
- Coombs directoen el niño negativo.
- Administrar antes de las 72 horas de haberse producido el parto.
Esta administración es independiente del grupoABO de madre y niño. Si existe dificultad para la administración antes de las 72 horas, podría aplicarsehasta los 28 días despuésdel parto, por supuesto con una eficacia mucho menor.
En muchos centros de diferentes paísesse complementa la profilaxis puerperal con administración deI g anti D durante el embarazo a las 28 semanas, y también a las 32 ó 34 semanas para prevenir la sensibilización de una parte de las embarazadas duranteel último trimestre.
Los problemas principales relacionados con la profilaxis Rh pueden observarse en la relación siguiente. En su conjunto son el motivo por el cual, a pesar demás de 20 años de aplicación del programa de profilaxis, todavía no se ha eliminado la inmunización porRh totalmente. Los problemasresiduales de la profilaxis son:
1. Ineficacia del programa:
a) Asistenciales:
- [No administración de Ig anti D constantemente en el puerperio.
- [Administración tardía.
- [No administración de la Ig anti d en abortosespontáneos o provocados.
- [No administración de Ig antiD en otros eventos sensibilizantes como: biopsia coriónica, amniocentesis, sangramiento en inserción baja placentaria, etc.
b) Diagnósticos:
- [No se diagnostica la cuantía de la hemorra-gia feto-materna (Kleihauer).
- [No se diagnostica el grupo y Rh en las inte-rrupciones de embarazo y otros eventos sensibilizantes.
En generalno existen suficientes sueros clasificadores y de Coombs para el diagnóstico de esta entidad. Estosproblemas permiten plantearde forma explícitalas recomendaciones para la profilaxis Rh en:
- Toda mujer Rh negativa no sensibilizada, después del parto de un niño Rh positivo.
- Toda mujer Rh negativa no sensibilizada, con esposo Rh positivo después del aborto espontáneo o provocado.
- Toda mujer Rh negativa no sensibilizada, con es-poso positivo, y que sufrieracualquier evento durante el embarazo posiblemente sensibilizante, como amenaza de aborto o versión por maniobras externas, etc.
- Toda mujer Rh negativo no sensibilizada con espo-so positivoa las 28 semanas y después a las 34 ó36 semanas,que no necesitaser repetido en el puer-perio si el parto ocurre 3 semanas después de la últimadosis.
- En cualquier momento que se diagnostique http masiva, pueden administrarse dosis repetidas variables, basadas en el diagnóstico de la cuantía de la HTP si ha podido realizarse el testde Kleihauer—Betke.
En estos casos deben administrarse dosis de 250 a 300 mg por cada 25 mL de sangre fetal a la circulación materna.
Tratamiento de la Enfermedad Hemolítica por Rh
Durante el embarazo,el tratamiento de la isoinmunización adopta 2 formas fundamentales basadas en la edad gestacional y posible madurez pulmonar fetal: la interrupción de la gestación y la transfusión intraútero.
Considerando la historiaobstétrica anterior, los antecedentes transfusionales, la cigocidad del esposo y los títulos de anticuerpos de la madre, según detallamos en el subtítulo de diagnóstico de las EHRh, los resultados del estado del líquido amniótico para EFT orientan finalmente la conducta obstétrica, y la interrupción de la gestación será la decisión cuando se demuestre afectación fetal, por resultados de DDO a450 mm en la zona 3 con más de 34 semanas de gestación.
Resultados en la zona 2 que plantean un niño moderadamente afectado, si tienen tendencia descendente, permiten acercarse al término e incluso alcanzar las 37 semanas. Generalmente hay que adelantar el parto cuando existe evidencia de madurez pulmonaro utilizar inductores de ésta antes de la semana 34.
Resultados en la zona 2, pero con tendencia ascendente acercándose a la zona 3, plantean enfermedadgrave y obligaa la interrupción de la gestación previa inducción de madurez pulmonar. Los resultados de EFT en la zona 3 plantean casos muy graves que antes de la semana 32 son candidatosa transfusión intraútero.
Transfusiones intraútero. Técnica intraperitoneal (TIP)
Antes del desarrollo de la ultrasonografía, esta técnica requeríaque se realizara amniografía con medio de contraste para que el feto se delineara bien y poder verlo radiológicamente con ayuda de intensificadores de imágenes. Actualmente el feto se visualiza en la US y la técnica inicial es idéntica a la de la ACT, pero con aguja fina y de 18cm de longitud, que se introduce en el saco amniótico yse dirige a la pared abdominal del feto, atravesándola en dirección a las asas intestinales, tratando de evadir los órganos fetales (hígado, bazo, vejiga, etc.).
Con la confirmación ultrasonográfica de que la aguja se halla en la cavidadperitoneal del feto, se inyecta lentamente la sangre preparadapara la transfusión en un tiempopromedio de 20 a 30 min.
La sangre ideal es un preparado de glóbulos O-,con hematócrito elevado de 70 a 80 % y hemoglobina de 20 a 25 %. La cantidad de sangre varía de acuerdocon la edad gestacional y se basa en tablas confeccionadas a este fin. Si no existe hidrops fetal, la absorción de la sangre suele ser más lenta.
Si es necesariocontinuar con TIP, la segunda debe realizarse 10 ó 12 días después para esperar la absorción totalde la anterior. Despuéspuede espaciarse cada2 ó 3 semanas, hasta las 32 semanas.
Lo deseable sería la interrupción de la gestación aproximadamente 2 semanas después de la última transfusión y no rebasar la semana 34. Debe tenerse presenteque después que una paciente es seleccionada para TIP y éstas comienzan, el seguimiento ya no se realizapor EFT del líquido, pues siempre la muestra obtenidaestaría contaminada con sangre del proceder anterior. Se realizaría por parámetros clínicosy estudios de bienestar fetal.
En la actualidad después que se desarrolló la técnica de muestra de sangre fetal por cordocentesis,en la mayoría de los centros de nivel terciario de países desarrollados se realiza la transfusión intraútero con técnica intravascular directa (TIV) y que, por lo tanto, al transfundir al feto directamente se puede obtener mejor respuesta y el embarazopuede avanzar hastael término.
Estos procederes brindanuna posibilidad de supervivencia a aquellos fetos que por lo precoze intenso dela enfermedad hemolítica, sucumbirían irremisiblemente, tanto si se extrajeran como si se dejarán evolucionar. La TIV tiene riesgos, sobre todo para el feto. Entre ellos,el desencadenamiento del trabajo de parto pretérmino, traumas fetales diversos, traumas placentarios con posible desprendimiento de placenta, muerte fetal, etc. Los riesgos maternos son mínimos, si se respetan todos los pasosdel proceder. La infección siempre es un riesgo potencial.
Plasmaféresis
La plasmaféresis, por medio de la cual se extraen grandes cantidades de anticuerpos, es un método costoso y con determinados riesgos.Logra reducir los anticuerpos maternos en un porcentaje importante, pero transitoriamente. Quizás su valor radique en retardar la necesidad de TIV por 2 ó 3 semanas. Estaría,sobre todo, indicada en mujeres muy sensibilizadas con esposos homocigóticos, que tienen historia de fetos hidrópicos muy precoces antes de las 24 semanas.
Administración de Inmunoglobulina Endovenosa
La administración de altas dosis de inmunoglobulina endovenosa ha demostrado ser efectiva en el tratamiento de casos severos de isoinmunización a D y C por diferentes autores. Es un tratamiento extremadamente costoso, que impide su uso de rutina
Fuentes
Rigol Ricardo, Orlando. Obstetricia y Ginecología, La habana 2004.Cap 19.pp 183-188