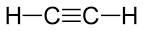Acetileno
| ||||||
Acetileno es el nombre comercial del Etino, el alquino más sencillo. Es un gas, altamente inflamable, un poco más ligero que el aire, incoloro y que posee un olor característico a ajo. Produce una llama de hasta 3000ºC.
- Fórmula General: C2H2
- Fórmula semidesarrollada: HC≡CH
Sumario
Descubrimiento
Edmund Davy fue quien descubrió accidentalmente el acetileno mientras intentaba aislar potasio. En 1836, Davy calentó carbonato de potasio con carbono, generando el residuo que hoy se denomina carburo de potasio. El carburo de potasio, a su vez, libera este gas al reaccionar con el agua.
Pese al hallazgo, pasaron más de dos décadas hasta que volvió a prestarse atención al acetileno. Fue el químico francés Marcellin Berthelot quien, en 1860, redescubrió este gas y lo bautizó como acetileno.
Obtención
Se obtiene mediante la reacción del agua con el y Carburo de Calcio, la cual libera un gas volátil que es capaz de producir hasta 3000 ºC, la mayor temperatura por combustión conocida hasta el momento.
En petroquímica se obtiene el acetileno por quenching (enfriamiento rápido) de una llama de gas natural o de fracciones volátiles del petróleo con aceites de elevado punto de ebullición. El gas formado en esta reacción a menudo tiene un olor característico a ajo debido a trazas de fosfina. Es utilizado directamente en plantas como producto de partida en síntesis de acetaldehído por hidratación, viniléteres por adición de alcoholes, etc., o vendido en bombonas disuelto en acetona. Así se baja la presión necesaria para el transporte ya que a altas presiones el acetileno es explosivo.
Composición
Estructura
H : C ::: C : H
Es el hidrocarburo insaturado con estructura más simple.
Propiedades físico-químicas
- Gas
- Incoloro
- Inodoro
- Más ligero que el aire
- Punto de Ebullición -57ºC
- Punto de Fusión -81ºC
- Presión de Vapor 4460 kPa a 20ºC
- Densidad Relativa 0.907
- Solubilidad en Agua 1.66 g/ 100 mL a 20ºC
- Peso Molecular 26 uma
Reacciones
El acetileno se utiliza principalmente como compuesto químico intermedio. El acetileno reacciona con:
- Cloro, para formar tetracloruro de acetileno (CHCl2CHCl2) o dicloruro de acetileno (CHCl=CHCl)
- Bromo, para formar tetrabromuro de acetileno (CHBr2CHBr2) o dibromuro de acetileno (CHBr=CHBr)
- Cloruro de hidrógeno (bromuro de hidrógeno o yoduro de hidrógeno) para formar monocloruro de etileno (CH2=CHCl) (monobromuro, monoyoduro), y 1,1-dicloroetano (cloruro de etileno; CH2=CHCl) (dibromuro, diyoduro)
- Agua, en presencia de un catalizador tal como sulfato mercúrico (HgSO4), para formar acetaldehído (CH3CHO)
- Hidrógeno, en presencia de un catalizador de, como por ejemplo, níquel (Ni) finamente dividido y caliente, para formar etileno (CH2=CH2) o etano (CH3CH3)
- Metales tales como el cobre (Cu) o níquel (Ni) al estar húmedo; con plomo (Pb) o zinc (Zn) al estar húmedo y sin purificar.
- Con una solución salina amonio-cuprosa (o de plata), para formar acetilo cuproso (o plata) (HC≡CCu o HC≡CAg), el cual es explosivo cuando está seco, y rinde acetileno al ser tratado con ácido.
- Una solución de cloruro mercúrico (HgCl2), para formar acetaldehído tricloromercúrico [C(HgCl)3·CHO], el cual rinde acetaldehído (CH3CHO) más cloruro mercúrico al ser tratado con cloruro de hidrógeno.
Aplicaciones
El principal uso del acetileno se realiza en el corte y la soldadura de metales en combustión con el oxígeno.
Antiguamente el acetileno se utilizaba como fuente de iluminación. En la vida diaria el acetileno es conocido como gas utilizado en equipos de soldadura debido a las elevadas temperaturas (hasta 3.000 ºC) que alcanzan las mezclas de acetileno y oxígeno en su combustión.
El acetileno es además un producto de partida importante en la Industria Química. Hasta la Segunda Guerra Mundial una buena parte de los procesos de síntesis se basaron en el acetileno. Hoy en día pierde cada vez más en importancia debido a los elevados costos energéticos de su generación.
Precaución
El acetileno es un gas supremamente inflamable, por lo cual se debe tener cuidado en cercanía de una fuente de fuego.
Transportación
El acetileno se transporta en cilindros de acero, disuelto en acetona a una presión de 15 atmósferas y absorbido en un material poroso. Es necesario tomar estas precauciones al envasarlo porque el gas solo, sometido a presiones superiores a 2 atm, tiende a estallar violentamente.
Fuentes
- http://www.messergroup.com
- http://www.gruponitrox.com.ve
- http://www.canbus.galeon.com
- Speight, James G.(2002). Chemical Process and Design Handbook. Ed. McGraw-Hill