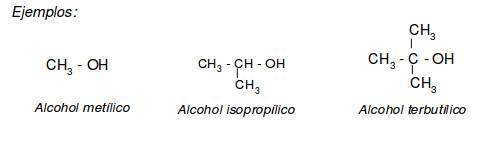Alcohol
Alcohol. Los alcoholes son un grupo de moleculas organicas caracterizadas por la presencia de uno o mas grupos -OH (hidroxilo) como grupo principal. Los alcoholes tienen de formula general: R-OH, estructuralmente son semejantes al agua, en donde uno de los hidrógenos se ha sustituido por un grupo alquilo. Su grupo funcional es el grupo hidroxilo, OH.
Sumario
Historia
La palabra Alcohol proviene del árabe al Kuhul que significa sutil. Sin embargo no se conoce con precisión cuando se usó por primera vez aunque se cree que es la droga más antigua y más usada del mundo.
El alcohol en estado puro no tiene color. Las bebidas alcohólicas contienen agua y etil alcohol y toman su color de acuerdo al ingrediente que se use para hacerlas. Los ingredientes utilizados con más frecuencia son frutas, vegetales o granos. También se pueden utilizar otras plantas.
La concentración de alcohol en las bebidas alcohólicas varía de unas a otras. Por ejemplo: la cerveza tiene una parte de etanol por cada 20 partes de agua, el vino es de 2 a 4 veces más fuerte que la cerveza y las bebidas destiladas como el whisky o el ron contienen aproximadamente la misma proporción de etanol que de agua, lo que las hace más potentes en cuanto a sus efectos.
El alcohol es considerado una droga porque cambia la forma en que las personas perciben el mundo, sienten, y se comportan.
Estructura
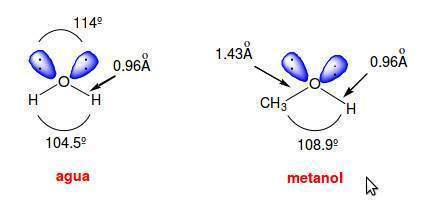
La estructura de un alcohol se asemeja a la del agua puesto que un alcohol procede de la sustitución formal de uno de los hidrógenos del agua por un grupo alquilo.
En el agua el ángulo del enlace H-O-H es de 104.5o y el ángulo que forman los dos pares de electrones no compartidos es de 114o. Estos ángulos de enlace se pueden explicar admitiendo una hibridación sp3 en el átomo de oxígeno. No hay ninguna razón para que un átomo (oxígeno, nitrógeno, carbono, etc) forme un conjunto de orbitales híbridos equivalentes cuando no todos los orbitales se van a utilizar del mismo modo. En el agua los orbitales híbridos sp3 que se van a emplear en los enlaces con los átomos de hidrógeno tienen un menor carácter s, lo que explica la disminución del ángulo de enlace tetraédrico desde 109.5o a 104.5o. Por otra parte, los dos orbitales híbridos sp3, que contienen a los dos pares de electrones no enlazantes, tienen un mayor carácter s, lo que explica el aumento del ángulo de enlace desde 109.5o a 114o. El aumento del ángulo de enlace entre los pares de electrones no compartidos tiene un efecto estabilizante al disminuir la repulsión electrónica entre los mismos.
En el metanol el ángulo del enlace C-O-H es de 108.9o. Este ángulo es mayor que en el agua debido a la presencia del grupo metilo, mucho más voluminoso que el átomo de hidrógeno, que contrarresta el efecto de compresión del ángulo de enlace que provocan los dos pares de electrones no enlazantes.
Las longitudes de enlace O-H son aproximadamente las mismas en el agua que en los alcoholes, pero la distancia de enlace C-O es bastante mayor (1.4 Å) debido al mayor radio covalente del carbono en comparación con el del hidrógeno.
Clasificación
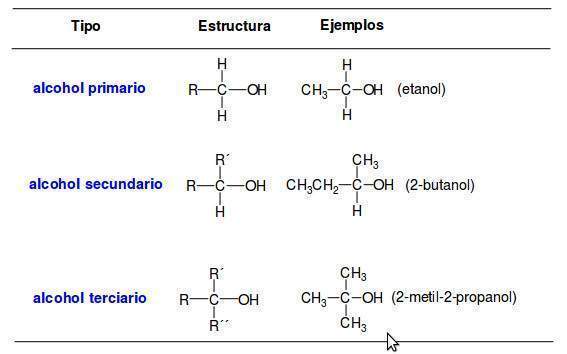
Una manera de organizar la familia de los alcoholes es clasificar a los alcoholes en primarios, secundarios o terciarios de acuerdo con el tipo de átomos de carbono enlazados al grupo OH. En la siguiente tabla se indican las estructuras de los alcoholes según su grado de sustitución:
Nomenclatura
En la nomenclatura de alcoholes se suelen emplear nombres vulgares para los términos más sencillos ( C1 - C4 ). Estos nombres se forman con la palabra alcohol.
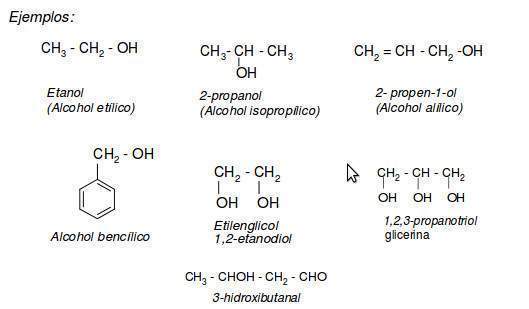
El sistema IUPAC nombra a los alcoholes de acuerdo a las siguientes reglas:
- Se busca la cadena más larga que incluya el Grupo Hidroxilo. La terminación o del hidrocarburo se cambia por -ol.
- La cadena se numera de forma que al grupo funcional le corresponda el menor número posible. Si hay mas de un grupo hidroxilo en la cadena, se emplean los prefijos di, tri, etc.
- Cuando el alcohol no es el grupo funcional principal se nombra como hidroxi, precedido de su número localizador.
Propiedades
En cuanto a sus propiedades, los alcoholes de baja masa molecular, están a temperatura ambiente en estado líquido y son incoloros, además de solubles en agua en mayor o menor medida.
A medida que aumenta el tamaño de la molécula también aumenta su punto de fusión y baja su solubilidad en el agua, llegando a poder estar en algunos casos en estado solido a temperatura ambiente. Aunque la mayoría de alcoholes tienen una densidad menor que la del agua, algunos, especialmente los que cuentan con anillos aromáticos, poseen una densidad mayor. La polaridad de los grupos -OH permite a estas moléculas establecer enlaces puente de hidrógeno con moléculas compañeras, o con aniones.
Aplicaciones
El etanol se utiliza ampliamente en muchos sectores industriales y en el sector farmacéutico, como excipiente de algunos medicamentos y cosméticos (es el caso del alcohol antiséptico 70º GL y en la elaboración de ambientadores y perfumes). Es muy utilizado con fines culinarios (bebida alcohólica).
Es un buen disolvente, y puede utilizarse como anticongelante. También es un desinfectante. Su mayor potencial bactericida se obtiene a una concentración de aproximadamente el 70%.
La industria química lo utiliza como compuesto de partida en la síntesis de diversos productos, como el acetato de etilo (un disolvente para pegamentos, pinturas, etc.), el éter dietílico y otros. También se aprovechan sus propiedades desinfectantes. Se emplea como combustible industrial y doméstico. En el uso doméstico se emplea el alcohol de quemar. Este además contiene compuestos como la pirovidos exclusivamente a alcohol. Esta última aplicación se extiende también cada vez más en otros países para cumplir con el protocolo de Kyoto. Estudios del Departamento de Energía de USA dicen que el uso en automóviles reduce la producción de Gases de Efecto de Invernadero en un 85%. En países como México existe la política del ejecutivo federal de apoyar los proyectos para la producción integral de etanol y reducir la importación de gasolinas que ya alcanza el 60%.
Ver además
- Ansiedad e Insomnio
- Alcoholismo en mujeres embarazadas
- Alcanfor
- Abstinencia alcohólica
- Destilación
- Alcohol Boricado
- Alcohorexia