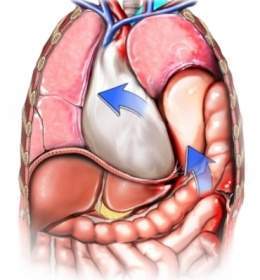
Hernia diafragmática congénita
| ||||
Hernia diafragmática congénita (HDC). Se define como un defecto de tamaño variable en el diafragma que permite que una parte del contenido del abdomen ascienda a la cavidad torácica comprimiendo los pulmones en mayor o menor grado. Se clasifican en congénitas (presentes en el nacimiento) y adquiridas. Estas últimas son muy raras y de ellas casi el 90% son secundarias a traumatismos (accidentes de tráfico). Las hernias congénitas se pueden observar a todas las edades y su sintomatología dependerá del tamaño del orificio herniario, del tipo de hernia y de la presencia de otras anomalías, la más importante de ellas la hipoplasia pulmonar (falta de desarrollo de los pulmones).
Sumario
Tipos de hernias congénitas
- Posterolaterales (en general son grandes, en el lado izquierdo, y se presentan en el recién nacido)
- Anterolaterales (son pequeñas y asintomáticas hasta que se produce la estrangulación de un segmento intestinal)
- Canal esofágico (se manifiestan como reflujo gastroesofágico).
En la actualidad las hernias congénitas se diagnostican con gran frecuencia durante la gestación mediante una ecografía (eco-doppler) en la que se aprecia contenido intestinal en la cavidad torácica junto a una disminución del aporte sanguíneo a los pulmones que será proporcional al grado de hipoplasia de los mismos y que tiene por tanto un valor pronóstico de la gravedad de la enfermedad. El diagnóstico antenatal es importante por que permite valorar la conveniencia de una intervención intraútero (aún hay hoy poca experiencia y una alta mortalidad) o lo que es más frecuente, estar preparados en el momento del parto, donde la reanimación del recién nacido requiere unas consideraciones especiales. Lo ideal es que el parto tenga lugar en el mismo complejo hospitalario donde luego ha de ser tratado por los equipos de Cirugía Pediátrica y Neonatología en estrecha coordinación. El traslado en ambulancia de estos niños presenta un alto riesgo añadido de mortalidad.
En las hernias congénitas graves el niño presenta dificultad respiratoria desde el nacimiento y es fundamental lograr su adecuada estabilización metabólica-respiratoria con anterioridad al imprescindible tratamiento quirúrgico que tiene por misión cerrar el defecto del diafragma. La tasa de mortalidad en este periodo inicial es cercana al 50%, aunque la utilización de mejores técnicas de ventilación pre y postquirúrgica (ECMO) han mejorado este dato. En las pequeñas hernias que debutan cuando se estrangula una porción del contenido intestinal o que suponen un hallazgo casual, el tratamiento es igualmente quirúrgico (cierre del orificio) pero como el desarrollo pulmonar es bueno la mortalidad es muy baja. Puede resumirse que el principal factor pronóstico en estos niños es el grado de desarrollo de los pulmones que se han visto comprimidos durante su periodo de desarrollo intrauterino en grado variable.
Generalidades
- Es la herniación de vísceras abdominales hacia la cavidad toráxica con el desarrollo incompleto del pulmón ipsilateral.
- Incidencia de 1 en 2000 - 5000 recién nacidos (RN) vivos.
- Asociación aproximadamente en el 50% de los casos a otras malformaciones (defectos del tubo neural, cardiopatías, etc) o cromosomopatias.
- El 90% de las HDC son izquierdas.
- Un 95% son de tipo Bochdalek (posterolateral),y 5% de tipo Morgagni (anterior).
- Sobrevida en distintos centros va desde un 40% a un 80%.
- Morbimortalidad está dada por los defectos asociados, grado de hipoplasia pulmonar e hipertensión pulmonar persistente (HPPN).
Embriología
En el embrión de las primeras semanas las cavidades torácica y abdominal se comunican libremente. La parte ventral del diafragma tiene su origen en el septum tranverso que separa el corazón de las visceras abdominales. Este tabique se une por detrás con una mesenterio dorsal, formando una barrera transversal en la cavidad celómica, pero quedan unas aberturas posteroexternas que reciben la denominación de conductos pleuroperitoneales. Estos conductos se cierran posteriormente por medio de una membrana doble formada por el peritoneo y la pleura. Entre ambas serosas se desarrolla una capa muscular estriada que completa y refuerza la separación entre las cavidades pleural y peritoneal.
Etiopatologìa
Las anomalías en la formación anatómica normal del diafragma explican la aparición de defectos congénitos. Si la detención del desarrollo diafragmático se produce precozmente en útero, el recién nacido presenta una amplia comunicación entre tórax y abdomen. Si la detención de la formación se produce después de formado el tabique membranoso pero antes de formarse la caja muscular, el niño presenta un saco herniario que contiene los órganos desplazados hacia arriba. Esta es en síntesis la etiología del padecimiento.
Clasificación
Son numerosas las clasificaciones emitidas por los diversos autores en relación con este padecimiento, pues cada uno lo clasifica a su manera y según la naturaleza de las hernias diafragmáticas, que se presenten.
- Hernia Posteroexterna de Bochdalek izquierda.
- Hernia Posteroexterna de Bochdalek derecha.
- Hernia del hiato esofágico.
- Hernia retroesternal de Morgagni.
Diagnóstico Prenatal y factores pronósticos
- La HDC se diagnostica por ecografía prenatal al encontrar vísceras abdominales en el tórax (estómago, asas intestinales, riñón, hígado y/o bazo). Una vez confirmado el diagnostico, debe realizarse ecocardiografía fetal para descartar cardiopatía congénita asociada.
- En caso de HDC derechas, el diagnóstico antenatal es más difícil debido a que el hígado y el pulmón fetal presentan similares características ecogénicas. Se sospecha al hallar una imagen sugerente de vesícula biliar en el tórax.
- Polihidroamnios está asociado en un 70% de los casos. Actualmente existe la posibilidad de realizar Resonancia Nuclear Magnética fetal, lo que permite precisar el grado de hipoplasia pulmonar y la posición de vísceras sólidas como el hígado.
- Las HDC diagnosticadas antes de las 25 semanas de gestación y/o que contienen hígado, condicionan un peor pronóstico.
- Otro factor pronóstico utilizado es el índice ecográfico LHR “lung to head ratio” (relación pulmón/cabeza), medido entre las 22 y 27 semanas de gestación. Valores de LHR bajos indican mayor hipoplasia pulmonar y peor sobrevida (valores 1).
- Menor sobrevida ante la presencia de malformaciones o síndromes asociados.
Cuadro Clínico
- Depende del grado de hipoplasia pulmonar e HPPN. Sus manifestaciones clínicas van desde insuficiencia respiratoria severa al nacer hasta el hallazgo casual en una radiografía de tórax a edades mayores (HDC anteriores pequeñas).
- En general, se manifiesta como SDR con abdomen excavado, insuficiencia respiratoria en grado variable, disminución, asimetría o ausencia de murmullo pulmonar, desplazamiento del latido cardiaco, auscultación de ruidos hidroaéreos en tórax, ausencia de excursión respiratoria del hemitórax comprometido.
- El diagnóstico se confirma con una radiografía de tórax que muestra contenido hidroaéreo (asas intestinales y/o estómago) en tórax o velamiento difuso de un hemitórax (si la intubación fue precoz), y desplazamiento del mediastino. El diagnóstico del contenido herniario se puede precisar con una ecografía.
Manejo médico
A. Corticoides prenatales. Existe evidencia (en animales) que el uso de corticoides prenatales mejora la madurez pulmonar en la HDC. Considerar el uso de un curso de corticoide prenatal. B. Parto.Idealmente al completar las 40 semanas de gestación, por vía vaginal o cesárea, y en un centro de alta complejidad que cuente con ventilación convencional, de alta frecuencia, óxido nítrico, cardiólogo infantil y ecocardiografía de urgencia. Además, debe existir coordinación con un centro quirúrgico. C. Posparto.
- Intubación endotraqueal al nacer, evitando la ventilación con ascarilla y bolsa, la cual puede distender el estómago e intestino, empeorando la función pulmonar.
- Sonda nasogástrica de doble lumen y aspiración continua suave (sonda Replogle).
- Línea arterial umbilical o radial derecha para monitoreo hemodinámica y de gases arteriales. Catéter venoso umbilical para apoyo hemodinámico con drogas vasoactivas (dopamima, dobutamina, epinefrina).
- Evaluación cardíaca precoz (ecocardiografía) para descartar cardiopatía congénita asociada, evaluar función miocárdica y grado de HPPN.
- Monitoreo hemodinámico y de saturación arterial pre y posductal.
- Poner en alerta al cirujano infantil.
- Nutrición parenteral total.
- Surfactante: no existe evidencia que apoye su uso en forma profiláctica.
- Ventilación mecánica:
a) En lo posible, permitir ventilación espontánea utilizando ventilación sincronizada. b) Utilizar frecuencias respiratorias altas con presiones bajas (PIM < 25 cm H2O) y tiempos inspiratorios cortos. c) PEEP bajo (2-3 cm H2O). d) Definir hipoxemia por saturación o PaO2 preductal. e) Corrección lenta de hipoxemia e hipercarbia en primeras horas de vida. f) Tolerar PaCO2 alta (45 a 65 mmHg), pH 7.30 a 7.45, PaO2 preductal 50 a 80 Hg. g) Bicarbonato en bolos según estado ácido-base. h) Sedación (fentanyl en infusión), evitar parálisis muscular. i) Presiones ventilatorias bajas (PIM y PEEP) posterior a cirugía. 10. Ventilación de alta frecuencia oscilatoria (VAFO). Se debe utilizar encasos graves que no responden al soporte habitual (índice de oxigenación > 20 - 25). 11. Oxido Nítrico Inhalatorio (ONi). La literatura actual NO apoya su uso rutinario por lo que en el Servicio no se usa en el manejo preoperatorio de HDC. 12. ECMO. En caso de no responder a los pasos anteriores, con índice de oxigenación > 30, se debe considerar el traslado a un centro que cuente con este recurso. 13. Corrección quirúrgica. Se debe considerar una vez estabilizado el paciente desde el punto de vista hemodinámica y respiratorio, en espera de una disminución significativa de la resistencia vascular pulmonar. No antes de 12 horas de vida, generalmente entre el día 2 y 6 de vida.