Monosacáridos
| ||||||
Monosacáridos. Constituyen la forma más simple, no pueden hidrolizarse a otra más sencilla. Ejemplo glucosa, fructosa y galactosa. Están formados por una molécula de ploihidroxialdehído y polhidroxicetonas, cuya fórmula empírica responde a (CH20)n donde n=3 a 7.
La cadena carbonada no es ramificada. Todos los átomos de carbono, excepto uno, se encuentran enlazados a un grupo hidróxilo (OH). El átomo de carbono no enlazado a grupo hidróxilo, lo está con un oxígeno y constituye el grupo funcional del monosacárido denominado grupo carbonilo.
Sumario
Clasificación
Los monosacacaridos se clasifican según el número de átomos de carbono y según la posición que ocupa en la molécula el grupo carbonilo. Según el número de átomos de de carbono, se dividen en:
- Triosas (3 átomos de carbono)
- Tetrosa (4 átomos de carbono)
- Pentosa (5 átomos de carbono)
- Hexosas (6 átomos de carbono)
- Heptosas (7 átomos de carbono)
Cuando el grupo carbonilo se encuentre en el extremo de la molécula, el monosacárido será una aldosa. Cuando el grupo carbonilo no se encuentre en el extremo, sino en una posición intermedia, el monosacárido será una cetosa.
Formas de representación
Los monosacáridos se estudian mediante dos formas de representar su molécula.
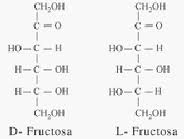
La fórmula e Fisher representa a la molécula de monosacárido de forma lineal, la cual no se ajusta a la realidad, pues no sirve para explicar muchas reacciones químicas , sin embargo, diversos autores la emplean para explicar algunas de sus propiedaes.
La fórmula de Haworth es actualmente reconocida como real, o sea, cuando el monosacárido está en disulución. Esta fórmula es ciclica, lo que hace que las moléculas tomen forma de figuras gemétricas, pentágonos, hexágonos, etc.
Propiedades físicas
Los monosacáridos son sólidos cristalinos de color blanco y de sabor dulce, solubles en agua e insolubles en disolventes no polares. Presentan isomería espacial o isómeria óptica.
El número de isómeros espaciales (estereoisómeros) de un monosacárido depende del número de átomos de carbono asimétricos que presente su molécula. Un carbono asimétrico es aquél cuyos cuatro enlaces están compartidos con cuatro grupos diferentes.
El gliceraldehído es el monosacárido más sencillo; es una aldotriosa y sólo presenta un átomo de carbono asimétrico, por tanto, sólo existirán dos estereoisómeros.
Los monosacáridos presentan isomería óptica; esto es que son ópticamente activos, ya que hacen rotar el plano de luz polarizada.
La luz polarizada se obtiene pasando un rayo de luz ordinariamente que vibra en los infinitos planos perpendiculares a la dirección de propagación, a través de los llamados prismas de Nicol, que no son más que un par de prismas de CaCO3 cortados según determinados ángulos. Los compuestos ópticamente activos se clasifican como dextrogiros y levogiros, de acuerdo con la dirección, que hacen rotar el plano de la luz polarizada. El poder rotatorio se mide, experimentalmente, con ayuda de un equipo de laboratorio llamado polarímetro.
Los isómeros ópticos se denominan enantiomorfos y para su rotación se utiliza un signo + para los que hacen rotar el plano de la luz polarizada hacia la derecha (dextrogiros), y un signo – para los que hacen rotar el plano de la luz polarizada hacia la izquierda (levogiros).
Una mezcla de cantidades iguales de isómeros dextro y levo de cualquier sustancia es ópticamente inactiva y se denomina mezcla racémica.
Los estereoisómeros varían en sus propiedades físicas y químicas, los enantiomorfos no, no aunque si varian notablemente en sus propiedades biológicas; por ejemplo, una capa de bacterias puede fermentar las formas dextro de un compuesto y no tener ningún efecto sobre la forma levo.
Propiedades químicas
La propiedades químicas más importantes de los monosacáridos son:
- Poder reductor.
- Formación de glicósidos.
El poder reductor se debe a las características reductoras del grupo carbonilo. La reacción frente a los reactivos Tollens, Benedict o Fehling, da como primer producto ácido glucónico. Esta propiedad química es utilizada en azúcares reductoras en orina.
La formación de glicósidos ocurre cuando reacciona un monosacárido con un alcohol. Este tipo de reacción puede ocurrir también entre dos monosacacaridos dando lugar a un disacárido.
Este enlace que es capáz de unir largas cadenas de monosacáridos, se denomina enlace glicosídico.
Un fenómeno interesante de los monosacáridos es el llamado mutarrotación, el cual se debe a libre rotación del hidróxilo (OH) e hidrógeno del grupo carbonilo, de forma que surgen dos compuestos isómeros α y β, los cuales se encuentran en equilibri en solución y solo se diferencian en la posición del OH del grupo carbonilo.