Alotropía
| ||||
Alotropía. Propiedad que poseen determinados elementos químicos de presentarse bajo estructuras moleculares diferentes, como el oxígeno, que puede presentarse como oxígeno atmosférico (O2) y como ozono (O3), o con características físicas distintas, como el fósforo, que se presenta como fósforo rojo y fósforo blanco (P4), o el carbono, que lo hace como grafito, diamante y fulereno. Para que a un elemento se le pueda denominar como alótropo, sus diferentes estructuras moleculares deben presentarse en el mismo estado físico.
El Azufre también puede manifestarse mediante estructuras moleculares diferentes bajo determinadas condiciones.
Sumario
Descubrimiento de su propiedad Alotrópica
A pesar que el azufre elemental es conocido desde tiempos de la prehistoria, no fue hasta hace apenas 20 años que se pudo aclarar la alotropía que poseía este elemento. El alótropo más común del azufre en la naturaleza es el S8, o ciclo octazufre, el cual con una temperatura superior a 95ºC es cristalino formando cristales aciculares, sin embargo, por debajo de dicha temperatura se forman cristales de tipo más grueso. Los cristales, se nombran como monocíclicos y rómbicos, según sus formas, diferenciándose tan solo en la forma en la que las moléculas se van empacando. Ambas formas son polimorfitas una de la otra, no alótropos propiamente dicho. Los polimorfos se pueden definir como distintas estructuras cristalinas en las cuales las unidades del compuesto, que son iguales, se van acomodando de diversa forma.
En 1891 se pudo sintetizar por vez primera un alótropo del azufre, el cual poseía unos anillos con un tamaño distinto de ocho. Dicho alótropo fue el S6, ciclo hexazufre, el segundo en ser descubierto de entre muchos alótropos reales del azufre. Para poder distinguir los alótropos y los polimorfos, se puede definir de forma más correcta a los alótropos como unas formas del mismo elemento que tienen unidades moleculares distintas. Se ha conseguido sintetizar alótropos del azufre con medidas de anillo de entre 6 y 20, y existen indicios de la posible existencia de alótropos con unos anillos bastante mayores. El más estable de todos, a parte del ciclooctaazufre, es el ciclo dodecazufre, o S12.
El ciclohexaazufre puede ser sintetizado mezclando tiosulfato de sodio y ácido clorhídrico en estado concentrado, a través de la reacción:
6 Na2S2O3 (ac) + 12 HCl (ac) → S6 (s) +6 SO2 (g) + 12 NaCl (ac) + 6 H2O (l)
Pero, sin embargo, existe ya una síntesis bastante lógica de los anillos con números de átomos pares, los cuales son más estables que los anillos de números impares. El método implica una reacción del polisulfuro de hidrógeno adecuado, H2Sx, con el dicloruro de poliazufre más adecuado, SyCl2, de manera que la x+y, de cómo resultado un tamaño igual al anillo que se desea. Así, el ciclo dodecazufre puede prepararse mezclando octasulfuro de dihidrógeno, H2S8, y dicloruro de tetrazufre, S4Cl2, en disolvente etoxietano:
H2S8 + S4Cl2 → S12 (s) + 2 HCl (g)
Pero el ciclo octazufre es el alótropo que se encuentra en la naturaleza, prácticamente en exclusiva, y el que se produce en la mayoría de las reacciones químicas, por lo cual hablaremos más detenidamente de él. En el punto de fusión, el ciclooctaazufre forma un líquido de un color ocre de baja viscosidad, pero cuando dicho líquido se calienta, se produce n cambio considerable en las propiedades, cuando llega a los 159ºC. Dicha transformación de las propiedades pasa con un aumento de la viscosidad de unas 10^4 veces. También, el líquido se torna mucho más oscuro. Estos cambios puedes explicarse en términos de ruptura de anillos. Así las cadenas de ciclooctaazufre se enlazan entre sí para dar lugar a la formación de polímeros que pueden llegar a contener un total de 20.000 átomos de azufre. Por lo cual, el aumento de la viscosidad se explica por la sustitución de las moléculas de S8, que se pueden mover libremente, por dichas cadenas, interactuando de manera intensa con las fuerzas de dispersión.
Según va aumentando la temperatura hacia el punto de ebullición del azufre, es decir 444ºC, la viscosidad inicia a bajar gradualmente pues las unidades poliméricas comienzas a partirse a causa del mayor movimiento térmico. Si dicho líquido es vertido en el agua fría, se conseguirá la formación de un sólido transparente y elástico de color marrón claro, conociendo a dicha sustancia como azufre plástico. Este material cambia lentamente a microcristales de azufre rómbico.
La ebullición del azufre provoca una fase de gas verde, que en la gran parte consiste en ciclooctaazufre. Cuando la temperatura aumenta aún mas, los anillos sufren una fragmentación; en torno a 700ºC se ve un gas de color violeta que contiene moléculas de diazufre, análogas a las de dioxígeno.
Aplicabilidad a partir de su Alotropía
Esta misma propiedad hace que el azufre tenga un amplio campo de aplicación. Se utilizan en la vulcanización del caucho, en atomizadores con azufre para combatir parásitos de las plantas, en la manufactura de fertilizantes artificiales y en ciertos tipos de cementos y aislantes eléctricos, en algunos ungüentos y medicinas y en la manufactura de pólvora y fósforos. Los compuestos de azufre se emplean en la manufactura de productos químicos, textiles, jabones, fertilizantes, pieles, plásticos, refrigerantes, agentes blanqueadores, drogas, tintes, pinturas, papel y otros productos.
Estructuras Alotrópicas comunes
Este no metal tiene un color amarillento, amarronado o anaranjado. Es blando, frágil, ligero, desprende un olor característico a huevo podrido al combinarse con hidrógeno y arde con llama de color azul, desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono. Es multivalente, y son comunes los estados de oxidación -2, +2, +4 y +6. En todos los estados (sólido, líquido y gaseoso) presenta formas alotrópicas cuyas relaciones no son completamente conocidas. Sus estructuras Alotrópicas comunes son:
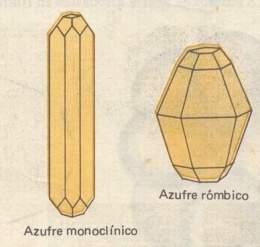
Azufre rómbico: Es conocido de la misma manera como azufre alfa. Se halla de la transformación estable del elemento químico por debajo de los 95.5ºC (204ºF, el punto de transición), y la mayor parte de las otras formas se revierten a esta modificación si se las deja permanecer por debajo de esta temperatura. El azufre rómbico posee un color amarillo limón, insoluble en agua, levemente soluble en alcohol etílico, éter dietílico y benceno, y es muy soluble en disulfuro de carbono. Posee una densidad de 2.07 g/cm3 (1.19 oz/in3), una dureza de 2.5 en la escala de Mohs y la fórmula molecular presenta es S8.
Azufre monoclínico: También es llamado azufre prismático o azufre beta. Viene siendo la modificación estable del elemento por encima de la temperatura de transición mientras que se encuentra por debajo del punto de fusión.
Azufre fundido: Se cristaliza en prismas en forma de agujas que son casi incoloras. Posee una densidad de 1.96 g/cm3 (1.13 oz/in3), un punto de fusión de 119.0ºC (246.7ºF) y la fórmula molecular que ostenta es S8.
Azufre plástico: Denominado también azufre gamma. Se produce cuando el azufre fundido en el punto de ebullición normal o cerca de él, es enfriado al estado sólido. Esta forma es amorfa y es sólo parcialmente soluble en disulfuro de carbono.
Azufre líquido: Posee la propiedad notable de aumentar su viscosidad si sube la temperatura. Su color cambia a negro rojizo oscuro cuando su viscosidad aumenta, y el oscurecimiento del color y la viscosidad logran su máximo a 200ºC (392ºF). Por encima de esta temperatura, el color se aclara y la viscosidad disminuye.
En el punto normal de ebullición del elemento químico (444.60ºC u 832.28ºF) el Azufre gaseoso presenta un color amarillo naranja. Cuando la temperatura aumenta, el color se torna rojo profundo y después se aclara, aproximadamente a 650ºC (202ºF), y adquiere un color amarillo paja.
Fuentes
- Bonner WA, Castro AJ. Química Orgánica Básica. 2 ed. La Habana; Editorial Pueblo y Revolución. 1979.
- Babor JA. Química General Moderna. 1ra reimpresión, Editorial Pueblo y Educación. 1978.
- Durán Rivas Yunior, Ing Químico. Apuntes de Química. Santiago de Cuba, Cuba, año 2000.