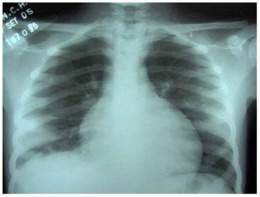
Hidrotórax hepático
| ||||
Hidrotórax hepático. El hidrotórax suele aparecer en pacientes cirróticos con historia previa de ascitis, aunque en ocasiones el acúmulo de fluido pleural
precede a la aparición de la ascitis debido al paso masivo de líquido ascítico hacia la cavidad pleural, favorecido por la presión inspiratoria negativa del tórax y un amplio defecto anatómico en el diafragma. En el 70% de los casos, el derra me pleural se localiza en el hemitórax derecho y en el resto de los casos, se produce en el izquierdo o es bilateral. El derrame pleural suele descubrirse, bien durante la exploración física o radiografía rutinaria de tórax, o bien como consecuencia de un estudio dirigido a aclarar el origen de síntomas como tos o disnea, los cuáles constituyen los únicos síntomas de esta com plicación.
Sumario
Criterios de diagnóstico
Cuando el derrame pleural coincide con la presencia de ascitis debe realizarse un estudio simultá neo de ambos fluidos. Las muestras de líquido pleural para el recuento celular deben ser recogidas en tubos con anticoagulante y analizadas de inmediato evitando así la agregación celular y la citolisis. El estudio inicial de ambos fluidos debe incluir, un recuento celular y la determinación de la concentración de albúmina, LDH y amilasas.
En los casos de derrame pleural no complicado, el nú mero de cé lulas debe ser inferior a 250/mm3 con predominio de linfocitos. La concentración de albúmina en el líquido pleural es de 0.5 a 1g.más alta que en la ascitis, diferencia debida a la mayor eficacia de la pleura para la absorción de agua, ya que la hiper tensión por tal limita la reabsorción peritoneal de agua.
En el diagnóstico diferencial con otras causas de derrame pleural es básico conocer la diferencia entre la concentración plasmá tica de albumina y la del líquido pleural. Cuando esta diferencia es superior a 1.1, debe sugerirnos que el hidrotórax es de origen hepático, por el contrario si este gradiente es inferior, debemos sospechar la existencia de un proceso subyacente de naturaleza inflamatoria o tumoral, en cuyo caso, se obser va también un nivel de LDH en el líquido pleural superior al plasmático. La determinación de amilasa en el estudio inicial del líquido pleural es aconsejable par ticularmente en pacientes con antecedentes de alcoholismo, dolor abdominal o traumatismo abdominal reciente.De esta forma evitaremos que en algunos casos un derrame pleural de origen pancreático quede enmascarado por la cirrosis.
Antes de aceptar que el hidrotórax es secundario a la cirrosis, es preciso descar tar otro posible origen, como es una insuficiencia cardíaca o un síndrome nefrótico, coincidentes con la enfermedad hepática. Ambas pueden también ocasionar un acúmulo de fluido, con características de tra sudado, a nivel peritoneal y pleural. Estas entidades son fácilmente recono cibles por su riqueza semiológica o bien a través de datos complementarios fácilmente accesibles. En pacientes cirróticos, también debemos tener en cuenta la posibilidad de que el derrame sea secundario a una sesión previa de escleroterapia de varices esofágicas, que ocasiona derrame pleural en casi la mitad de las ocasiones. En general, el derrame pleural postesclerosis es de escaso volumen, y cursa de forma asintomática y se resuelve en pocos días.
Una de las posibles complicaciones del hidrotórax hepático es el desarrollo de un empiema bacteriano espontáneo. Los gérmenes responsables son, en la mayoría de los casos, de origen entérico, lo que sugiere que la infección se produce por paso transdiafragmático de ascitis infectada. El empiema no asociado a peritonitis bacteriana es menos frecuente. En estos casos, el gérmen alcanza la pleura por vía hematógena. Es importante tener en cuenta el empiema pleural en el diagnóstico etiológico de un cuadro séptico en pacientes cirróticos, ya que prácticamente en la totalidad de los casos cursa sin dolor pleural, lo que le hace pasar desapercibido particu larmente en pacientes sin ascitis. El estudio del fluido pleural demostrará un incremento de leucocitos superior a 250/mm3 con predominio de polimorfonucleares. La toma de muestras para cultivo debe realizarse inoculando 10 cc de líquido pleural en un frasco de hemocultivo , inmediatamente después de la obtención de la muestra.
Tratamiento
Tratamiento farmacológico
El objetivo del tratamiento de los pacientes con hidrotórax de origen hepático es reducir o bloquear la formación de ascitis. El primer escalón terapéutico debe estar basado en el tratamiento médico capaz de conseguir un balance negativo de agua y sodio. La restricción salina y la administra ción de diuréticos de acción distal como la espironolactona sola o asociada a diuréticos de asa como la furosemida, es capaz de controlar el hidrotórax de escaso volumen.
Sin embargo, con relativa frecuencia, a pesar de admi nistrar altas dosis de diuréticos (300 mg de espironolactona y 120 mg de furosemida), no conseguimos evitar la persistencia o la reaparición del derrame pleural, incluso a veces, a pesar de conseguir el control de la asci tis. En estos casos, la capacidad funcional y calidad de vida del paciente se ve comprometida y es necesario recurrir a otras alternativas terapéuticas.
Tratamiento de urgencia
En ocasiones el paciente, sufre una dificultad respiratoria grave que precisa una solución urgente. En estas circunstancias, es necesaria la eva cuación inmediata del contenido pleural mediante toracocentesis. La decisión de practicar una toracocentesis, terapética de urgencia debe estar basada exclusivamente en la gravedad de la dificultad respiratoria que sufra el paciente y no en el resultado de los gases ar teriales.
De hecho, en algunos casos, tras la práctica de toracocentesis masivas, puede obser varse una ligera reducción de la presión ar terial de oxígeno, a pesar de conseguir una mejoría llamativa del bienestar del paciente. Estos hechos sugieren, por tanto, que la sensación de disnea no depende tanto de la presión parcial del oxígeno, sino de la alteración de la mecánica respiratoria.
Alternativas al tratamiento farmacológico
A pesar de que la toracocentesis alivia al paciente de sus síntomas, la toracocentesis repetida o el drenaje pleural continuo, no es una terapéu- tica adecuada y está formalmente contraindicada. Se han comunicado casos en la literatura tratados con drenaje pleural continuo, con extracción de más de un centenar de litros de fluido pleural, asociado a reposición plasmática simultánea de sustancias coloidosmóticas, sin que este proce dimiento haya modificado la situación del paciente, después de 40 días de hospitalización y coste económico total de 50.000 dólares.
La comunicació n peritoneo-venosa, diseñada por LeVeen para el tratamiento de la ascitis refractaria, ha sido utilizada en algunos casos ais lados como una alternativa terapé utica cuando fracasa el tratamiento mé di co del hidrotórax.
Teóricamente, esta prótesis constituye una vía de evacuación alternativa del fluido abdominal hacia el torrente circulatorio; sinembargo, este procedimiento además de producir complicaciones locales y siste máticas bien conocidas, se ha mostrado poco eficaz para evitar el hidrotórax. Su escasa eficacia terapéutica se debe a que la válvula encargada de mantener un flujo unidireccional desde la cavidad abdominal al torrente circulatorio, sólo se abre con presiones superiores a 3 o 4 cc de agua, por tanto el fluido abdominal pasa con mayor facilidad a la cavidad pleural donde la presión es inferior.
En los casos de derrame pleural sintomático persistente o recidivante es preciso tomar otras actitudes terapéuticas más eficaces. La reparación quirúrgica del defecto diafragmático asociada a pleurodesis ha sido una alternativa terapéutica útil en algunos casos, pero es una alternativa de escasa aplicabilidad, dado que la gran mayoría de pacientes que sufren hidrotórax de difícil control terapéutico, son por tadores de cirrosis avanzadas con alteración de la hemostasia, trastornos hemodinámicos y deterioro de la funció n renal, que hacen que el riesgo quirúrgico sea prohibitivo.
La pleurodesis química es la opción terapéutica más generalizada. Consiste en la instalación de un agente esclerosante en el espacio pleural después de evacuar su contenido. Entre los agentes esclerosantes , el más utilizado es el clorhidrato de tetraciclina.
Para llevar a cabo eficazmente la pleurodesis es preciso una evacuación total de la cavidad pleural mediante un tubo de toracotomía multiper forado de 18 a 22 F, colocado en el espacio intercostal más bajo posible el cual se conecta a un sistema de vacío (Pleu- revac). Una vez comprobamos radiológicamente la ausencia de fluido intra-pleural, se campla el drenaje y se inyectan 10.5 o 1 g de tetraciclina diluidos en 30 o 60 ml de suero salino en el espacio pleural a través del tubo del drenaje. Con el fin de purgar el tubo de drenaje se inyectan 10 ml de sue- rosalino, tras lo cual se cierra el drenaje. Se ha recomendado el cambio frecuente de la posición del paciente con el fin de asegurar un contacto amplio de la solución esclerosante con la totalidad de la super ficie pleural, pero se ha podido comprobar con soluciones de tetraciclina marcada con isótopos, que la posición del paciente no parece afectar su distribución por la super ficie pleural. Después de 6 horas se abre de nuevo el drenaje permitiendo la evacuación del contenido pleural.
La pleurodesis química es efectiva en una elevada proporción de pacientes con derrames pleurales de origen neoplá sico, pero en el caso del hidrotórax hepático los resultados son menos convincentes. Probablemen te, este hecho esté en relación con el flujo continuo de líquido desde la cavi dad abdominal al tórax que diluye el agente esclerosante y por tanto reduce su eficacia. Es aconsejable realizar el procedimiento después de con- seguir una evacuación máxima de la ascitis, mediante tratamiento diuré tico o con paracentesis evacuadora.
Existe una correlación directa entre el efecto esclerosante de la tetraciclina y la dosis administrada, lo que justificaría la reiteración del tratamiento en caso de no conseguir los efectos deseados tras una primera sesió n terapé utica. Clásicamente, se había atribuído el efecto esclerosante del clorhidrato de tetraciclina a su pH fuer temente áci do, pero se ha demostrado una eficacia terapéutica similar utilizando oxite traciclina que tiene un pH de 8. Se han utilizado diversas sustancias escle rosantes, en el tratamiento del hidrotórax de origen neoplásico, entre las que se incluyen quinacrina, thiotepa, bleomicina y mostaza nitrogenada.
Tienen el inconveniente de sus efectos indeseables sistémicos, además de provocar un dolor pleurítico más intenso. Algunas encuestas realizadas en el Reino Unido, demuestran que los cirujanos de tó rax consideran más efi caz la pleurodesis conseguida mediante suspensiones de 1-2 de talco, bien aplicado mediante pulverizació n ( spray ) a travé s del canal del mediasti-noscopio, con el fin de obtener una mejor diseminació n del talco. Esta tera péutica ha sido muy discutida debida al riesgo potencial de desarrollar un mesotelioma; sinembargo, en un estudio realizado entre 210 pacientes tra tados con talco entre 14 y 40 años antes, no se pudo demostrar el des arrollo de ningú n caso. Por tanto, esta es una opció n terapé utica que debe ser considerada en aquellos casos en los que no se consiga el control de esta complicación con el empleo de la tetraciclina.
Recientemente la derivación intrahepática por tosistémica percutá nea, universalmente denominado TIPS (Transjugular Intrahepatic Por tos ystemic Shunt), ha venido a incrementar el arsenal terapéutico disponible para el manejo de la hiper tensión por tal. Su empleo ha estado dirigido fun damentalmente al tratamiento de la hemorragia digestiva por varices esofá gicas, así como para el control de la ascitis refractaria. El TIPS reduce la presión hidrostática sinusoidal y aumenta la excreción urinaria de sodio. Estos efectos están asociados a una reducción de factores antinatriuréticos plasmáticos como la actividad de renina plasmática y aldosterona. El mayor inconveniente del TIPS es su tendencia a la estenosis, que precisa tratamiento frecuente mediante técnicas de radiología vascular inter vencionista, que encarecen su coste. A pesar de ello, teóricamente, esta podría ser la mejor opción terapéutica en pacientes que son candidatos a trasplante hepático.
En pacientes con insuficiencia hepática, la presencia de un hidrotórax de difícil manejo es un factor que debemos tomar en consideración para decidir un trasplante hepático ya que en ocasiones, ésta será la única opció n terapéutica capaz de resolver esta complicació n de la cirrosis.
Fuentes
Alber ts MW, Salem Aj, Solomon DA , et al. Hepatic hydrothorax. Cau- se and management. Ann Intern Med. 1.991.151: 2383-2388.
Anonymous. A sur vey of long-term ef fects of talc and kaolin pleuro- desis. Research Commitee of the British Thoracic Association and the Medical Research Council Pheumoconiosis Unit. Brit J Dis Chest.1979.73: 285-288.
Davila R. Masive hepatic hydrothorax without ascites: The complexi- ties and cost of management. Hepatology 1.988.83: 333-334.
Falchuk KR, Jacoby I, Colucci WS, et al. Tetracycline- induced pleural symphysis for recurrent hydrothorax complicating cirrhosis. Gastro- enterology 1.977.72: 319-3212.
Ikard RW , Sawyer JL. Persistent hepatic Hidrothorax after peritone- ojugular shunt. Arch Surg.1.980.115: 1125-1127.
Lieberman FL, Hidemura R, Peters RL, et al. Pathogenesis and tre- atment of hydrothorax complicating cirrhosis with ascities. Ann Intern Med 1.996.64: 341-351. HIDROTÓ RAX HEPÁ TICO 117
McAlipne LG, Hulks G, Thomson NC. Management of recurrent malignant pleural ef fusion in the United Kingdom: Sur vey of clinical practice. Thorax 1.990.45: 699-701.
Quiroga J, Sangro B, Nú ñez M, et al. Transjugular intrahepatic potos- ystemic shunt in the treatment of refractor y ascites : Ef fect on clini- cal, renal, humoral and hemodynamic parameters. Hepatology 1.995.21: 986-994.
Strauss RM, Mar tin LG, Kaufman SL, et al. Transjugular Intrahepatic Por tal Systemic Shunt for the management of symptomatic hydro- thorax. Am J Gastroenterol 1.994.89: 1520-1522.
Xiol X, Castellote J, Baliellas C, et al. Spontaneous bacterial empye- ma in cirrhotic patients: Analysis of eleven cases. Hepatology 1.990. 11: 365-370.