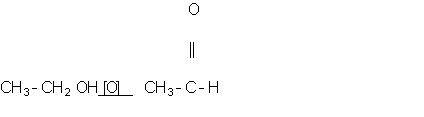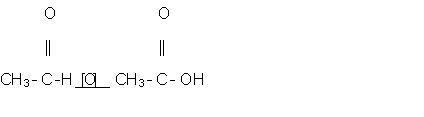Relación de transformación
La relación de transformación de las sustancias orgánicas: es la relación que se establece entre las sustancias orgánicas, en la cual se obtienen nuevos productos con propiedades y aplicaciones diferentes, perteneciendo a funciones químicas diferentes.
Sumario
Surgimiento
• Antiguamente la química se dividía en inorgánica o mineral y en orgánica, denominada así porque se encargaba del estudio de los compuestos elaborados dentro de los organismos vivientes. Para lo cual se necesitaba de una fuerza vital.
• En 1826 el químico alemán Federich Wholer elaboró el primer compuesto orgánico artificialmente que fue la úrea a partir de compuestos inorgánicos.
Química Orgánica
Cómo la química orgánica es la ciencia que estudia la estructura y propiedades de los compuestos del carbono que constituyen principalmente la materia viva, su aplicación a la industria y al desarrollo tecnológico.
Es llamada también Química de los Compuestos del Carbono, en esta rama de la Química se exceptúan a los compuestos: Carbonatos, Ferricianuros, etc. que contienen carbono pero forman parte de la Química Inorgánica.
Los compuestos Orgánicos están formados por:
Elementos Organógenos: C, H, O, N.
Elementos Secundarios : F, I, P, S, Ca, Na, As, Fe, etc.
• Los compuestos orgánicos en solución acuosa se ionizan muy débilmente.
• Según el numero de elementos primordiales los compuestos orgánicos pueden ser : Binarios, Terciarios , Cuaternarios.
• Presentan el fenómeno de la isomería es decir la misma formula global representa varios compuestos.
Clasificación de la Química orgánica
'Hidrocarburos': Alcanos, Alquenos, Alquinos.
Funciones oxigenadas: Alcohol, eter, aldehido, cetona, ester, ac. carboxilico, jabón
Funciones nitrogenadas: Amina, amida, nitrilo, imina, aminoacido.
Diferencias entre compuestos orgánicos e inorgánicos:
Compuestos Orgánicos:
- Están formado principalmente por : C, H, O, N
- El número de compuestos orgánicos excede considerablemente al número de compuestos inorgánicos.
- Entre los compuestos orgánicos prevalece el enlace covalente.
- Los compuestos orgánicos son generalmente insolubles en agua debido a su
- Baja polaridad.
- Los compuestos orgánicos son sensibles al calor, es decir, se descomponen fácilmente.
- Los cuerpos orgánicos reaccionan entre si lentamente debido al enlace covalente.
- Las sustancias orgánicas al disolverse no se ionizan, por lo tanto sus moléculas no conducen a la electricidad.
- Los cuerpos orgánicos son inestables aún a bajas temperaturas frente al calor y la luz.
Compuestos Inorgánicos:
Están constituidos por átomo de cualquier elemento.
- Resisten a la acción del calor.
- Los compuestos inorgánicos prevalece el enlace iónico.
- Los compuestos inorgánicos son solubles al agua debido a su elevada polaridad
- Pero insolubles en disolventes orgánicos.
- Los compuestos cuando se encuentran en solución son buenos conductores del calor y la electricidad.
- Los compuestos inorgánicos poseen reacciones instantáneas.
- Las moléculas inorgánicas son menos complejas que los compuestos de carbono, debido a su bajo peso molecular.
- Los compuestos inorgánicos son estables a las condiciones de temperaturas altas.
Hidrocarburos:
Los hidrocarburos constituyen la función fundamental de la química orgánica por la cual se le llama también Función Madre o Soporte, debido a que los demás compuestos orgánicos se consideran derivados de esta función. Los hidrocarburos son compuestos orgánicos binarios formados por átomos de carbono e hidrógeno , se podría decir que constituye la función química mas importante.
Clasificación de los hidrocarburos:
Alifáticos: La cual a su vez se subdivide en :
• H.C. Saturados: Alcanos.
• H.C. No Saturados: Alquenos, Alquinos, Dienos, Trienos, Diinos, etc.
• Ciclo Alifáticos: Ciclo alcano, ciclo alqueno, ciclo alquino, etc.
Aromáticos: Alquibencenos o arenos.
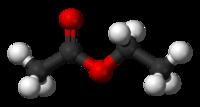
Esteres. Obtención a partir de hidrocarburos.
Los ésteres proceden de condensar ácidos con alcoholes y se nombran como sales del ácido del que provienen. La nomenclatura IUPAC cambia la terminación - oico del ácido por - oato, terminando con el nombre del grupo alquilo unido al oxígeno.
En química orgánica, compuesto formado (junto con agua) por la reacción de un ácido y un alcohol. Puesto que este proceso es análogo a la neutralización de un ácido por una base en la formación de una sal, antiguamente los ésteres eran denominados sales etéreas. Este término es incorrecto porque los ésteres, a diferencia de las sales, no se ionizan en disolución.
La trasformación desde el punto de vista químico que debe ocurrir para obtener un ester a partir de un hidrocarburo consiste en relacionar las diferentes reacciones químicas que permiten sintetizar estas sustancia química a partir de otra u otras.
Por ejemplo para obtener el etanoato de etilo a partir del etano debemos:
1-, etano + dicloro= cloruro de hidrógeno + cloroetano.
2-,cloroetano+ agua en medio básico= etanol + cloruro de hidrógeno.
3-, oxidación del etanol= aldehído
4-, oxidación del aldehído= ácido etanoico.
5- ácido etanóico + etanol= etanoato de etilo + agua
Otra forma de síntesis que puede emplearse es a través del alqueno o alquino correspondiente de igual cantidad de átomos de carbono, siempre que se utilice una moléculas de cloruro de hidrógeno.
Efecto en la salud del hombre de los esteres:
- Inhalación: Causa dolor de cabeza, náuseas e incluso pérdida de la conciencia y puede sensibilizar las mucosas, inflamándolas. En concentraciones altas causa convulsiones y congestión de hígado y riñones. Sin embargo, aún a concentraciones bajas causa anemia.
- Contacto con los ojos: Una exposición prolongada causa el oscurecimiento de las córneas.
- Contacto con la piel: El contacto constante o prolongado a este compuesto provoca resequedad, agrietamiento, sensibilización y dermatitis.
- Ingestión: Irrita las membranas mucosas. En experimentos con conejos se ha observado pérdida de coordinación, probablemente debido a la hidrólisis rápida a ácido acético y etanol.
- Carcinogenia: No se ha observado la generación de tumores en pulmón en animales de laboratorio expuestos a este producto.
- Mutagenia: No se ha observado incremento en la frecuencia de intercambio de cromátidas hermanas en trabajadores expuestos a este disolvente.
Fuente
- Compendio Preuniversitario de Química, Walter Cartolin Fernández
- Manual Teórico-Práctico de Química,Ana Medina C. - Nelva Rios H.
- Libro de Química,Carlos Emilio Vasquez Urday
Referencia Bibliográfica
Química Orgánica. Federich Akknann
Química General. Ignacio Puig
Química Elemental. Iacobucci Celso
Enlaces Externos