Diferencia entre revisiones de «Ácido fórmico»
(Página creada con ' {{desarrollo}} {{Elemento_químico |nombre=Ácido fórmico |imagen= Images_Acido_formico.jpg |nombre,simbolo,numero= H-COOH |serie_quimica= El '''ácidos fórmico''' pertenece...') |
m (Texto reemplazado: «<div align="justify">» por «») |
||
| (No se muestran 12 ediciones intermedias de 7 usuarios) | |||
| Línea 1: | Línea 1: | ||
| − | |||
| − | |||
{{Elemento_químico | {{Elemento_químico | ||
|nombre=Ácido fórmico | |nombre=Ácido fórmico | ||
| − | |imagen= | + | |imagen= Ácido_fórmicoP.jpeg |
|nombre,simbolo,numero= H-COOH | |nombre,simbolo,numero= H-COOH | ||
| − | |serie_quimica= El | + | |serie_quimica= El ácido fórmico pertenece al grupo de los ácidos carboxílicos}} |
| − | |||
| − | |||
| − | |||
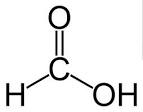
| − | + | '''Ácido fórmico'''. También llamado '''ácido metanoico''', es un [[ácido orgánico]] de un solo [[átomo]] de [[carbono]], siendo el más simple de los ácidos orgánicos. Su fórmula es [[Hidrógeno|H]]-[[Grupo carboxilo|COOH]] (CH<sub>2</sub>O<sub>2</sub>), el [[Grupo carboxilo|grupo carboxilo]] es el que le confiere las propiedades ácidas a la molécula. | |
| − | == Propiedades físicas | + | == Propiedades físicas== |
| − | == Propiedades químicas< | + | * Es un ácido líquido |
| − | == | + | * Incoloro |
| − | === | + | * Olor irritante |
| + | * Punto de ebullición de 100.7 °C | ||
| + | * Punto de fusión de 8,4 °C | ||
| + | |||
| + | == Propiedades químicas == | ||
| + | * La [[Constante de acidez|pK<sub>a</sub>]] del ácido fórmico es de 3,75. Teniendo en cuenta que el [[pH]] varía generalmente entre 0 y 14 (siendo 7 el pH neutro) podríamos decir que el fórmico, pese a ser un ácido de origen natural es relativamente fuerte. | ||
| + | * Soluble en agua, pues su [[cadena carbonada]] es muy corta y fácilmente ionizable. | ||
| + | * [[Momento dipolar]] de 3.79 [[Debye|D]] | ||
| + | |||
| + | == Aplicaciones == | ||
| + | * En industria farmacéutica. | ||
| + | * En la industria del pesticida como Triazolone, Disinfest. | ||
| + | * En la industria química. | ||
| + | * En la industria de cuero. | ||
| + | * En la industria de Textil. | ||
| + | * En la industria de goma. | ||
| + | * En la limpieza ácida de la producción de acero. | ||
| + | * Fabricación de la pulpa del papel. | ||
| + | * Como desinfectante. | ||
| + | |||
| + | == Riesgos == | ||
| + | ===Ingestión=== | ||
| + | * Dolor de garganta. | ||
| + | * Sensación de quemazón del tracto digestivo | ||
| + | * Dolor abdominal, diarrea, vómitos. | ||
| + | |||
| + | ===Inhalación=== | ||
| + | * Sensación de quemazón. | ||
| + | * Tos, dificultad respiratoria. | ||
| + | * Jadeo. | ||
| + | * Síntomas de efectos no inmediatos. | ||
| + | |||
| + | ===Piel=== | ||
| + | * Enrojecimiento, dolor. | ||
| + | * Quemaduras cutáneas graves. | ||
| + | |||
| + | ===Ojos=== | ||
| + | * Dolor. | ||
| + | * Enrojecimiento | ||
| + | * Visión borrosa. | ||
| + | * Quemaduras profundas graves. | ||
| + | |||
== Fuentes == | == Fuentes == | ||
| − | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). Ediciones ENEVA. | + | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones ENEVA]]. |
| − | * Ficha Información Técnica [http://spanish.caustic-soda-flakes.com/china-formic_acid_85-1086.html] Disponible en | + | * Ficha Información Técnica [http://spanish.caustic-soda-flakes.com/china-formic_acid_85-1086.html Ácido fórmico]. Disponible en "spanish.caustic-soda-flakes.com". Consultado: 12 de julio de 2011. |
| − | [[Category: Química]] | + | [[Category: Química]][[Category:Elementos químicos]] |
última versión al 01:14 14 ago 2019
| ||||||||||
Ácido fórmico. También llamado ácido metanoico, es un ácido orgánico de un solo átomo de carbono, siendo el más simple de los ácidos orgánicos. Su fórmula es H-COOH (CH2O2), el grupo carboxilo es el que le confiere las propiedades ácidas a la molécula.
Sumario
Propiedades físicas
- Es un ácido líquido
- Incoloro
- Olor irritante
- Punto de ebullición de 100.7 °C
- Punto de fusión de 8,4 °C
Propiedades químicas
- La pKa del ácido fórmico es de 3,75. Teniendo en cuenta que el pH varía generalmente entre 0 y 14 (siendo 7 el pH neutro) podríamos decir que el fórmico, pese a ser un ácido de origen natural es relativamente fuerte.
- Soluble en agua, pues su cadena carbonada es muy corta y fácilmente ionizable.
- Momento dipolar de 3.79 D
Aplicaciones
- En industria farmacéutica.
- En la industria del pesticida como Triazolone, Disinfest.
- En la industria química.
- En la industria de cuero.
- En la industria de Textil.
- En la industria de goma.
- En la limpieza ácida de la producción de acero.
- Fabricación de la pulpa del papel.
- Como desinfectante.
Riesgos
Ingestión
- Dolor de garganta.
- Sensación de quemazón del tracto digestivo
- Dolor abdominal, diarrea, vómitos.
Inhalación
- Sensación de quemazón.
- Tos, dificultad respiratoria.
- Jadeo.
- Síntomas de efectos no inmediatos.
Piel
- Enrojecimiento, dolor.
- Quemaduras cutáneas graves.
Ojos
- Dolor.
- Enrojecimiento
- Visión borrosa.
- Quemaduras profundas graves.
Fuentes
- Requena, L. Vamos a Estudiar Química Orgánica. (2001). Ediciones ENEVA.
- Ficha Información Técnica Ácido fórmico. Disponible en "spanish.caustic-soda-flakes.com". Consultado: 12 de julio de 2011.