Diferencia entre revisiones de «Concentración másica (unidad)»
(→Múltiplos) |
m (Texto reemplazado: «<div align="justify">» por «») |
||
| (No se muestran 6 ediciones intermedias de 4 usuarios) | |||
| Línea 1: | Línea 1: | ||
| − | |||
{{Definición | {{Definición | ||
|nombre= Concentración másica (unidad) | |nombre= Concentración másica (unidad) | ||
| − | |||
|imagen= Concentrac_masica.jpg | |imagen= Concentrac_masica.jpg | ||
|tamaño= 150 px | |tamaño= 150 px | ||
|concepto= Unidad de medida expresada en término de unidad base. | |concepto= Unidad de medida expresada en término de unidad base. | ||
}} | }} | ||
| − | + | '''Concentración másica (unidad)'''. Unidad de medida del [[Sistema Internacional de Unidades]] para expresar la relación constante entre la masa de cualquier soluto disuelto y el volumen de la disolución, su símbolo es P(X). <ref>«[Colectivo de autores: Química onceno grado. Editorial. Pueblo y Educación. Ciudad de [[La Habana]], [[Cuba]]. 1990. pág 33]» </ref>. </div> | |
Cualquiera sea la forma de expresar la concentración, esta referirá la cantidad de soluto disuelto en una determinada cantidad de disolvente o disolución. Dado que estas cantidades pueden expresarse en unidades de masa, cantidad de sustancia o volumen, la concentración de una disolución puede expresarse de diferentes formas. Las definiciones de estas son (en las expresiones se utiliza X- soluto; d- disolvente; D- disolución): | Cualquiera sea la forma de expresar la concentración, esta referirá la cantidad de soluto disuelto en una determinada cantidad de disolvente o disolución. Dado que estas cantidades pueden expresarse en unidades de masa, cantidad de sustancia o volumen, la concentración de una disolución puede expresarse de diferentes formas. Las definiciones de estas son (en las expresiones se utiliza X- soluto; d- disolvente; D- disolución): | ||
| + | |||
==Múltiplos== | ==Múltiplos== | ||
| + | |||
Los más utilizados de esta unidad de medida son los siguientes: | Los más utilizados de esta unidad de medida son los siguientes: | ||
{| class="wikitable" border="3" | {| class="wikitable" border="3" | ||
| Línea 25: | Línea 25: | ||
==Formulaciones y análisis de la unidad de medida== | ==Formulaciones y análisis de la unidad de medida== | ||
| − | [[Archivo: Formula_concentracion_masica.jpg|border|left| | + | [[Archivo: Formula_concentracion_masica.jpg|border|left|200px]] |
| − | + | ''' P(X) =m(X)/V(D) '''<br/> | |
| − | + | ''' P(X) = g/mol o g. L<sup>-1</sup>'''<br/> | |
Esta ecuación nos informa que es la que define a la concentración másica P(X), siendo una nueva magnitud física derivada de la masa m(X) y el volumen de la disolución V(D), y que, simplemente, corresponde a la masa del soluto expresada en gramos disuelto en un litro de disolución. | Esta ecuación nos informa que es la que define a la concentración másica P(X), siendo una nueva magnitud física derivada de la masa m(X) y el volumen de la disolución V(D), y que, simplemente, corresponde a la masa del soluto expresada en gramos disuelto en un litro de disolución. | ||
A partir de la ecuación de definición podrá calcularse la concentración másica de la disolución, conocida la masa de soluto disuelto en un volumen determinado de disolución; la masa de soluto que es necesario disolver para preparar un volumen de disolución dado a una concentración másica deseada, y el volumen de la disolución, si se conocen la masa de soluto y la concentración másica de esta. | A partir de la ecuación de definición podrá calcularse la concentración másica de la disolución, conocida la masa de soluto disuelto en un volumen determinado de disolución; la masa de soluto que es necesario disolver para preparar un volumen de disolución dado a una concentración másica deseada, y el volumen de la disolución, si se conocen la masa de soluto y la concentración másica de esta. | ||
| Línea 35: | Línea 35: | ||
Donde m(X) es el número de gramos de soluto y m(d) el número de gramos de disolvente. Como por lo general m(X) es muy pequeño comparado con m(d), esto se convierte en: | Donde m(X) es el número de gramos de soluto y m(d) el número de gramos de disolvente. Como por lo general m(X) es muy pequeño comparado con m(d), esto se convierte en: | ||
<center> ppm= m(X)/m(d) x10<sup>6</sup></center><br/> | <center> ppm= m(X)/m(d) x10<sup>6</sup></center><br/> | ||
| − | Como un litro de agua a temperatura ambiente pesa aproximadamente 106 mg, un mg de soluto en un litro de agua está en una concentración de alrededor de una ppm, o sea la concentración en ppm resulta equivalente a expresar la concentración en mg/L. | + | Como un litro de agua a temperatura ambiente pesa aproximadamente 106 mg, un mg de soluto en un litro de [[agua]] está en una concentración de alrededor de una ppm, o sea la concentración en ppm resulta equivalente a expresar la concentración en mg/L. |
De manera similar se pueden expresar las concentraciones en partes por billón. | De manera similar se pueden expresar las concentraciones en partes por billón. | ||
==Fuente== | ==Fuente== | ||
| − | + | ||
| − | *[http://lacomunidad.elpais.com/science/2010/12/18/los-calculos-estequiometricos-i-] | + | *[http://www.quimicabasica.cl/tema_17.pdf quimicabasica] |
| − | *[http://www.itescam.edu.mx/principal/sylabus/fpdb/recursos/r24448.DOC] | + | *[http://lacomunidad.elpais.com/science/2010/12/18/ los-calculos-estequiometricos-i-] |
| − | + | *[http://www.itescam.edu.mx/principal/sylabus/fpdb/recursos/r24448.DOC Recursos] | |
| + | |||
==Enlaces externos== | ==Enlaces externos== | ||
| + | |||
*[http://quimicaanaliticacualitativa.blogspot.com/2009_06_30_archive.html] | *[http://quimicaanaliticacualitativa.blogspot.com/2009_06_30_archive.html] | ||
| − | *[http://www.rimed.cu/index.php?option=com_content&view=article&id=5767&Itemid=94. ] | + | *[http://www.rimed.cu/index.php?option=com_content&view=article&id=5767&Itemid=94.] |
| − | *[http://www.utim.edu.mx/~navarrof/Docencia/QuimicaAnalitica/Disoluciones/Disoluciones3.htm. ] | + | *[http://www.utim.edu.mx/~navarrof/Docencia/QuimicaAnalitica/Disoluciones/Disoluciones3.htm.] |
| − | + | ||
==Referencias== | ==Referencias== | ||
<references/> | <references/> | ||
| − | [[Category: | + | [[Category:Unidades y constantes]] |
última versión al 15:12 1 ago 2019
| ||||||
Concentración másica (unidad). Unidad de medida del Sistema Internacional de Unidades para expresar la relación constante entre la masa de cualquier soluto disuelto y el volumen de la disolución, su símbolo es P(X). [1].
Cualquiera sea la forma de expresar la concentración, esta referirá la cantidad de soluto disuelto en una determinada cantidad de disolvente o disolución. Dado que estas cantidades pueden expresarse en unidades de masa, cantidad de sustancia o volumen, la concentración de una disolución puede expresarse de diferentes formas. Las definiciones de estas son (en las expresiones se utiliza X- soluto; d- disolvente; D- disolución):
Sumario
Múltiplos
Los más utilizados de esta unidad de medida son los siguientes:
| Símbolo | Nombre |
|---|---|
| kilogramo por metro cúbico | |
| g/dm3 |
gramo por decimetro cúbico |
La unidad de medida de la concentración másica, que se utiliza con más frecuencia, es el g/mol o g. L-1
Formulaciones y análisis de la unidad de medida
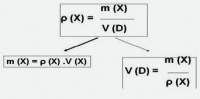
P(X) =m(X)/V(D)
P(X) = g/mol o g. L-1
Esta ecuación nos informa que es la que define a la concentración másica P(X), siendo una nueva magnitud física derivada de la masa m(X) y el volumen de la disolución V(D), y que, simplemente, corresponde a la masa del soluto expresada en gramos disuelto en un litro de disolución.
A partir de la ecuación de definición podrá calcularse la concentración másica de la disolución, conocida la masa de soluto disuelto en un volumen determinado de disolución; la masa de soluto que es necesario disolver para preparar un volumen de disolución dado a una concentración másica deseada, y el volumen de la disolución, si se conocen la masa de soluto y la concentración másica de esta.
Para soluciones muy diluídas resulta conveniente utilizar como manera de expresar la concentración de la solución en partes por millón, que definimos como:
Donde m(X) es el número de gramos de soluto y m(d) el número de gramos de disolvente. Como por lo general m(X) es muy pequeño comparado con m(d), esto se convierte en:
Como un litro de agua a temperatura ambiente pesa aproximadamente 106 mg, un mg de soluto en un litro de agua está en una concentración de alrededor de una ppm, o sea la concentración en ppm resulta equivalente a expresar la concentración en mg/L. De manera similar se pueden expresar las concentraciones en partes por billón.