Diferencia entre revisiones de «Propeno»
| Línea 43: | Línea 43: | ||
* [[Buteno]] | * [[Buteno]] | ||
* [[Penteno]] | * [[Penteno]] | ||
| − | |||
== Fuentes == | == Fuentes == | ||
* Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones Eneva]]. | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones Eneva]]. | ||
| − | *MORRISON, R. T. y BOYD, R. N.: | + | *MORRISON, R. T. y BOYD, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, E.U.A., 1990. |
| − | * SOTO, J. L.: Química Orgánica. | + | * SOTO, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996. |
| − | VOLLHARDT, K. P. C.: Química Orgánica. Ed. Omega. Barcelona, 1996. | + | * VOLLHARDT, K. P. C.: Química Orgánica. Ed. Omega. Barcelona, 1996. |
[[Category: Química]] | [[Category: Química]] | ||
Revisión del 19:43 4 ago 2011
| ||||||||||
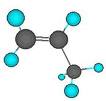
Propeno. También llamado Propileno, es un Alqueno formado por 3 átomos de carbono y 6 átomos de hidrógeno, su fórmula global es C3H6. Es un homólogo del etileno, presenta el doble enlace como grupo funcional.
Sumario
Propiedades físicas y químicas
- Masa molecular: 42,1 g/mol
- Punto de fusión: –185,3 °C
- Punto de ebullición: –48 °C
- Temperatura de ignición: 460 °C
- Presión de vapor a 20 °C: 10.200 hPa
- Concentración máxima permitida en los lugares de trabajo: 500 ppm
- Límites de explosividad: 2,0 - 11,1% de propeno en el aire.
Obtención
contituye uno de los productos de la termólisis del petróleo. Se separa de los demás productos como el etileno por destilación a baja temperatura.
Aplicaciones
- En la síntesis del polipropileno.
- La adición de agua en condiciones polares da iso-propanol que puede ser oxidado a la acetona.
- La adición de agua en condiciones condiciones radicalarias se obtiene n-propanol.
Reacciones
Hidrohalogenación
La hidrohalogenación ocurre al hacer burbujear un halogenuro de hidrógeno en un recipiente conteniendo propeno en éter. Como producto principal de la reacción se obtendrá el 2-halógenopropano. Ejemplo: utilizando HBr se obtiene el 2-bromopropano).
Halogenación
Al hace reaccionar el propeno con un halógeno en tetraclorometano como solvente se produce el 1,2-dihalógenopropano Ejemplo: utilizando I2 se obtiene el 1,2-diyodopropano.
Véase también
Fuentes
- Requena, L. Vamos a Estudiar Química Orgánica. (2001). Ediciones Eneva.
- MORRISON, R. T. y BOYD, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, E.U.A., 1990.
- SOTO, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996.
- VOLLHARDT, K. P. C.: Química Orgánica. Ed. Omega. Barcelona, 1996.