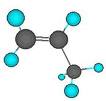
Propeno
| ||||||||||
Propeno. También llamado Propileno, es un Alqueno formado por 3 átomos de carbono y 6 átomos de hidrógeno, su fórmula global es C3H6. Es un homólogo del etileno, presenta el doble enlace como grupo funcional.
Sumario
Propiedades físicas y químicas
- Masa molecular: 42,1 g/mol
- Punto de fusión: –185,3 °C
- Punto de ebullición: –48 °C
- Temperatura de ignición: 460 °C
- Presión de vapor a 20 °C: 10.200 hPa
- Concentración máxima permitida en los lugares de trabajo: 500 ppm
- Límites de explosividad: 2,0 - 11,1% de propeno en el aire.
Obtención
contituye uno de los productos de la termólisis del petróleo. Se separa de los demás productos como el etileno por destilación a baja temperatura.
Aplicaciones
- En la síntesis del polipropileno.
- La adición de agua en condiciones polares da iso-propanol que puede ser oxidado a la acetona.
- La adición de agua en condiciones condiciones radicalarias se obtiene n-propanol.
Reacciones
Hidrohalogenación
La hidrohalogenación ocurre al hacer burbujear un halogenuro de hidrógeno en un recipiente conteniendo propeno en éter. Como producto principal de la reacción se obtendrá el 2-halógenopropano. Ejemplo: utilizando HBr se obtiene el 2-bromopropano).
Halogenación
Al hace reaccionar el propeno con un halógeno en tetraclorometano como solvente se produce el 1,2-dihalógenopropano Ejemplo: utilizando I2 se obtiene el 1,2-diyodopropano.
Adición de ácido sulfúrico
El ácido sulfúrico concentrado se adiciona al propeno por un mecanismo de adición electrofílica produciendo el sulfato ácido de isopropilo.
hidroformilación
La hidroformilación del propeno con monóxido de carbono, agua y un catalizador de cobalto a altas presiones y temperaturas produce butanal como principal producto.
Polimerización
La polimerización del propileno a polipropileno se puede llevar a cabo de forma radicalaria aunque en la polimerización catalítica se obtienen productos con mejores calidades que además son mejor controlables. Los catalizadores empleados eran originalmente del tipo Ziegler-Natta. En la actualidad se están sustituyendo por otros sistemas basados en zirconocenos.
Ozonólisis con clivaje reductivo
Por Ozonólisis con posterior clivaje oxidativo se obtiene como productos formaldehído y acetaldehído.
Clivaje oxidativo
La oxidación violenta del propeno con KMnO4 caliente produce por clivaje oxidativo, ácido acético y dióxido de carbono. También se obtendrían los mismos productos por ozonólisis con ozono (O3) a bajas temperaturas (-78 °C) y posterior clivaje oxidativo con peróxido de hidrógeno (H2O2) en medio alcalino
Fuentes
- Requena, L. Vamos a Estudiar Química Orgánica. (2001). Ediciones Eneva.
- Morrison, R. T. y Boyd, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, Estados Unidos, 1990.
- Soto, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996.
- Vollhardt, K. P. C.: Química Orgánica. Ed. Omega. Barcelona, 1996.