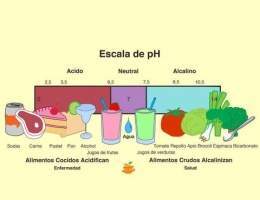
Equilibrio ácido-básico
| ||||||
Equilibrio ácido-básico. El pH es una medida del grado de acidez o basicidad de una sustancia o solución. Se determina según la fórmula, pH es igual a menos logaritmo de la concentración de hidrogeniones, por lo que es inversamente proporcional a dicha concentración o sea a mayor concentración de hidrogeniones menor será el pH y viceversa.
El pH normal de los líquidos corporales oscila entre 7.35 para la sangre venosa, por su mayor contenido en bióxido de carbono y 7.45 para la sangre arterial, con un menor contenido del mismo. Cuando el pH disminuye por debajo de 7.35 se produce una acidosis, mientras que si aumenta por encima de 7.45 se produce una alcalosis.
Cuando se incrementa el nivel de acidez, la sangre debe conservar este vital equilibrio a través del aporte de bases (álcalis) para neutralizan los ácidos. Por ello, para obtener un sano metabolismo celular, es preciso que la sangre tenga un constante flujo de sustancias de naturaleza alcalina, a fin de poder neutralizar el exceso de ácidos.
== Trastornos del equilibrio ácido – básico. Los trastornos del equilibrio ácido – básico se clasifican teniendo en cuenta el valor del pH en: Acidosis y Alcalosis; y según su origen, pueden ser: respiratorios, cuando son causadas por alteraciones de la ventilación alveolar; y metabólicos, cuando obedecen a alteraciones ajenas al funcionamiento del sistema respiratorio. Los desequilibrios ácido-básicos son alteraciones que ponen en peligro la vida, por lo que el dominio de los mecanismos reguladores del pH tiene gran importancia en la práctica médica.
Sumario
- 1 Mecanismos para la regulación del equilibrio ácido-básico
- 2 Sistema amortiguador
- 3 Sistema amortiguador de fosfatos.
- 4 Principio isohídrico.
- 5 Sistema respiratorio
- 6 Regulación respiratoria de la alcalosis metabólica.
- 7 Secreción de hidrogeniones en los tubos renales.
- 8 En una acidosis.
- 9 En una alcalosis
- 10 Importante conocer
- 11 Fuentes
Mecanismos para la regulación del equilibrio ácido-básico
Los sistemas amortiguadores, de bicarbonato, de fosfato y de proteínas; el sistema respiratorio y el sistema renal.
Sistema amortiguador
Un sistema amortiguador es una solución de dos o más sustancias cuya combinación se opone a los cambios de pH del medio en que se encuentre. Generalmente está constituido por un ácido débil y su sal correspondiente y su poder amortiguador está dado por la proximidad de su pK o constante de disociación al valor normal del pH y por la concentración de sus componentes. La pK es una medida de su capacidad para captar o ceder hidrogeniones.
Sistema amortiguador de bicarbonato.
El sistema amortiguador de bicarbonato está integrado por el bicarbonato de sodio y el ácido carbónico. Cuando al medio donde se encuentra este sistema se añade un ácido fuerte como el ácido clorhídrico, el cual reacciona con el bicarbonato de sodio, dando lugar a un acido débil, el ácido carbónico, que modifica muy poco el pH y una sal neutra, el cloruro de sodio. Por otra parte si se añade una base fuerte, como el hidróxido de sodio, ésta reacciona con el componente ácido del sistema, el ácido carbónico y se obtiene como producto el bicarbonato de sodio, base débil con poca incidencia sobre el pH, y agua. Este sistema amortiguador tiene una pK de 6.1, por lo que su poder amortiguador no es alto, sin embargo la abundancia de sus componentes en el líquido extracelular hace que sea el sistema amortiguador más importante en dicho medio.
Sistema amortiguador de fosfatos.
Está compuesto por una base débil, el fosfato dibásico de sodio, y un ácido también débil, el fosfato monobásico de sodio. Si se añade un ácido fuerte al medio donde se encuentre este sistema, reacciona con el componente básico del mismo, el fosfato dibásico de sodio, dando lugar al fosfato monobásico de sodio más cloruro de sodio. Cuando se añade una base fuerte al sistema, como el hidróxido de sodio, ésta reacciona con el componente ácido del mismo, el fosfato monobásico de sodio, dando lugar al fosfato dibásico de sodio y agua. Este sistema tiene una pK de 6.8, mucho más cercana a los valores normales del pH de los líquidos corporales, por lo que tiene mayor poder amortiguador que el sistema de bicarbonato; sin embargo la poca cantidad en que se encuentra en el líquido extracelular determina su poca importancia en este medio.
Poder amortiguador de las proteínas.
Este está dado por su carácter anfótero, que consiste en su capacidad de ceder o captar hidrogeniones de acuerdo a las características del medio en que se encuentren. Las proteínas poseen grupos que en un medio alcalino ceden hidrogeniones, mientras que cuando se encuentran en un medio ácido captan hidrogeniones. Su pK tiene un valor cercano a 7.4, por lo que tiene un gran poder amortiguador y es el más importante en el líquido intracelular. Existen varios sistemas amortiguadores de proteínas y dentro de ellos se destaca el sistema amortiguador de la hemoglobina tanto por su abundancia en la sangre, como por el hecho de circular a través de todos los tejidos del organismo.
Principio isohídrico.
La acción simultanea e integrada de los sistemas amortiguadores está determinada porque sus componentes se encuentran, todos a la vez en los líquidos corporales y tienen un denominador común que son los hidrogeniones. Cuando se produce un cambio del pH de los líquidos corporales, éste es regulado por la acción conjunta de todos los sistemas amortiguadores, así los sistema de bicarbonato, de fosfato y de proteínas actúan al unísono este hecho se conoce con el nombre de Principio Isohídrico.
Sistema respiratorio
El sistema respiratorio regula el pH por su capacidad para eliminar o retener el bióxido de carbono al aumentar o disminuir la ventilación alveolar respectivamente. Si aumenta el bióxido de carbono, se desplaza el equilibrio de la misma hacia la derecha y aumentan los hidrogeniones.
De forma similar, si aumentan los hidrogeniones, se desplaza el equilibrio de la reacción hacia la izquierda, aumentando el bióxido de carbono. Las alteraciones respiratorias que afectan la ventilación pulmonar constituyen causa de desequilibrios del pH y éstos no pueden ser regulados por el propio sistema respiratorio.
Regulación respiratoria de la acidosis metabólica.
En la acidosis metabólica, la causa primaria es una disminución del bicarbonato por lo que el equilibrio de la reacción se desplaza hacia la derecha aumentando los hidrogeniones y por tanto elbióxido de carbono disminuye, siendo entonces los hidrogeniones los que estimulan el centro respiratorio y éste incrementa la profundidad de la ventilación y la frecuencia respiratoria, aumentando la eliminación de bióxido de carbono lo que equivale a disminuir la cantidad de hidrogeniones. De esta forma, el sistema aumenta el pH tratando de llevarlo a su valor normal. Así una acidosis metabólica se compensa con una alcalosis respiratoria.
Regulación respiratoria de la alcalosis metabólica.
En una alcalosis metabólica la causa primaria es un aumento en la concentración de bicarbonato por lo que la reacción se desplaza hacia la izquierda, disminuyendo la concentración de hidrogeniones y aumentando la concentración de bióxido de carbono, pero este aumento del bióxido de carbono es en una proporción menor que la disminución de los hidrogeniones.
Ésta última produce una depresión del centro respiratorio el cual disminuye la profundidad y frecuencia de la ventilación con lo que aumentan el bióxido de carbono y los hidrogeniones.
Secreción de hidrogeniones en los tubos renales.
El riñón proporciona el mecanismo regulador del pH más eficaz por su alta ganancia, ya que elimina del organismo los excesos, tanto de hidrogeniones, como de bicarbonato, genera nuevo bicarbonato y su acción no tiene límite de tiempo. En condiciones de pH normal el riñón elimina el exceso de hidrogeniones en un proceso que se inicia con la entrada a la célula del bióxido de carbono, el cual se une al agua del citoplasma de la célula de la pared tubular dando lugar al ácido carbónico, que se disocia en bicarbonato e hidrógeno. Esta reacción es catalizada por la anhidrasa carbónica.
En el líquido tubular circula el bicarbonato de sodio que se disocia en iónes sodio y bicarbonato. El bicarbonato formado en el líquido intracelular pasa al intersticio para ser incorporado al capilar peritubular, mientras que el hidrógeno es secretado activamente por un mecanismo de co-transporte, que a la vez reabsorbe el ión sodio desde el líquido tubular. Este ión sodio se intercambia activamente con un ión potasio procedente del intersticio, en un mecanismo de co-transporte.
El hidrógeno secretado al líquido tubular es neutralizado uniéndose al bicarbonato para formar ácido carbónico en un proceso denominado de titulación, que en condiciones de normalidad es una titulación completa al ser suficiente la cantidad de bicarbonato de sodio que circula en los líquidos tubulares para neutralizar los hidrogeniones secretados. El ácido carbónico se disocia en bióxido de carbono y agua. El bióxido de carbono es reabsorbido al interior de la célula de la pared tubular y el agua se elimina con la orina.
En una acidosis.
En el caso de una acidosis se exacerban estos procesos y al no existir bicarbonato suficiente en los líquidos tubulares para titular los hidrogeniones, estos se eliminan con la orina.
En una alcalosis
En el caso de una alcalosis, al no secretarse hidrogeniones suficientes para titular el bicarbonato tubular, este se elimina con la orina.
Importante conocer
Además es importante conocer otros aspectos que tienen que ver con la preparación misma de las comidas. Por ejemplo: se ha demostrado que un 40-60% de los elementos minerales y un 95% de las vitaminas y bases se pierden en el agua de cocción de las verduras. Resulta entonces que el alto contenido de bases que poseen las verduras -y que resulta tan útil para el equilibrio sanguíneo- se desvaloriza. Incluso las verduras llegan a presentar naturaleza ácida cuando se tira el agua de cocción (es el ejemplo de acelga o espinacas).
De allí la importancia del sistema oriental de cocer las verduras al vapor en cestas de acero o bambú, o sea sin que estén en contacto directo con el agua. También comprendemos el alto valor terapéutico de los caldos, que conservan todo el contenido alcalino de las verduras y que resultan tan equilibrantes en, enfermos y convalecientes. Acción de los amortiguadores tubulares.
En el líquido tubular circula el sistema amortiguador de fosfatos, por lo que en él se encuentra el fosfato dibásico de sodio, el que se disocia. El exceso de hidrógeno secretado al líquido tubular es neutralizado, uniéndose al sistema amortiguador de fosfato formando el fosfato monobásico de sodio que se elimina con la orina. Los trastornos acido básicos respiratorios se inician con un aumento o una disminución de la presión parcial de dióxido de carbono, mientras que los metabólicos comienzan con un aumento o una disminución del bicarbonato o reserva alcalina.
Fuentes
- GUYTON A. C HALL J.E. Tratado de Fisiología Médica. Interamericana, Madrid , 9na edición:2000
- Inorganic Chemistry (2nd edición). Prentice Hall. 1991. ISBN0134656598. Capítulo 6: Acid-Base and Donor-Acceptor Chemistry.
- The Proton in Chemistry (2ª edición). Chapman & Hall. 1973. Incluye la discusión de muchos ácidos orgánicos de Brønsted].
- Inorganic Chemistry (3rd edición). Oxford University Press. 1999. ISBN 0198503318. Capítulo 5: Acids and Bases.
- Inorganic Chemistry (3rd edición). Prentice Hall. 2008. ISBN 0131755536. Capítulo 6: Acids, Bases and Ions in Aqueous Solution.
- http://www.fatigayfibromialgia.com